【摘要】:表征理想气体状态的三个基本参数压力、温度和比体积(或体积)的关系式,称为理想气体状态方程式。可以使气体压缩成液体的这个极限温度,称为该气体的临界温度。气体的临界温度越低,越难液化。如制冷剂中的甲烷,临界温度较低,故较难液化;而氟利昂134a的临界温度较高,就容易液化。
1.理想气体状态方程式
既不考虑气体分子占有的体积,也不考虑分子之间的引力,这种气体称为理想气体。表征理想气体状态的三个基本参数压力、温度和比体积(或体积)的关系式,称为理想气体状态方程式。
当气体质量为单位质量时,理想气体状态方程式为
pv=RT (1-6)
式中 p——绝对压力(Pa);
v——比体积(m3/kg);
T——热力学温度(K);
R——气体常数[J/(kg·K)]。
当气体质量为m时,理想气体状态方程式为
pV=mRT (1-7)
式中 V——气体总体积(m3);
m——气体总质量(kg)。(https://www.xing528.com)
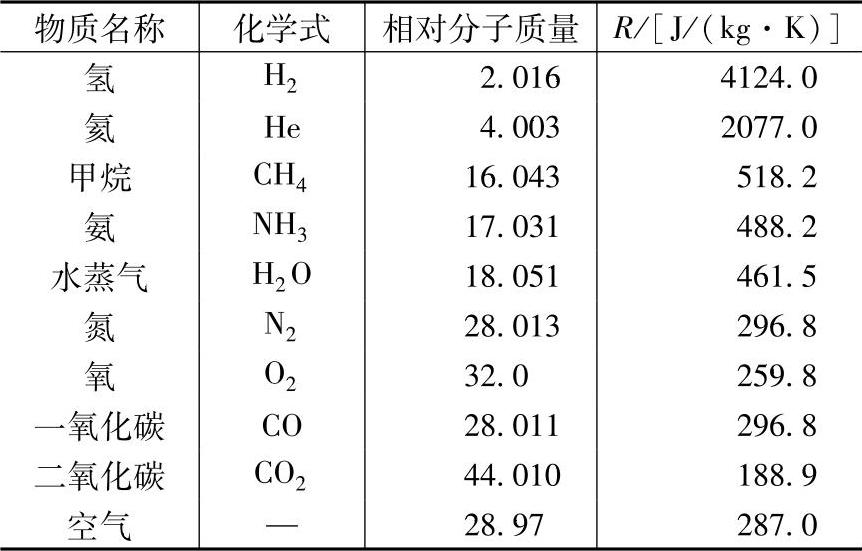
几种常见气体的气体常数R见表1-1。
表1-1 常见气体的气体常数R
2.气体的临界参数
任何气体在温度低于某一数值时,都可以等温压缩成液体;但当高于该温度时,无论压力增至多大,都不能使气体液化。可以使气体压缩成液体的这个极限温度,称为该气体的临界温度。当温度等于临界温度时,使气体压缩成液体的压力,称为临界压力。此时的状态称为临界状态,其比体积和密度分别称为临界比体积和临界密度。
气体的临界温度越低,越难液化。如制冷剂中的甲烷,临界温度较低(-161.49℃),故较难液化;而氟利昂134a的临界温度较高(101.1℃),就容易液化。
3.实际气体状态方程式
实际气体及蒸汽必须考虑气体分子占有的体积和分子之间的引力,对理想气体状态方程需进行修正。
在工程实践中,常用压缩系数Z加以校正,即
pV=ZmRgT (1-8)
压缩系数Z随温度和压力而变化,它的数值与对比压力p/pc及对比温度T/Tc有关。其中p与T分别代表工作压力和温度,pc和Tc分别代表临界压力和温度。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




