【摘要】:锌是一种两性金属,既容易溶于酸也容易溶于碱。但是锌中只要有微量超电势较低的金属,如Ag、Au、Co、Cu等存在,则反应极快。锌在空气中由于水气和CO的共同作用在表面常生成一层碱式碳酸锌ZnCO3·Zn2,它有保护锌的作用。钎焊时需要有效地除去这层膜和斑点。Zn2容易和氨的盐生成易溶于水的络合物,因此钎剂中含有氨的盐有利于去除氧化膜。Zn2+4NH4Cl=Zn4Cl2+2H2O+2HCl图19-1 锌在介质中的稳定区域 Fig.19-1 Stable area of zinc in water medium
锌是一种两性金属,既容易溶于酸也容易溶于碱。
在还原性的酸中,和酸反应生成相应酸的盐并放出氢气:
Zn+2HCl=ZnCl2+H2↑
Zn+H2SO4(稀)=ZnSO4+H2↑
锌的电极电位为-0.76V,但因氢在锌上的超电势很高,所以极纯的锌在酸中反应反而很慢。但是锌中只要有微量超电势较低的金属,如Ag、Au、Co、Cu等存在,则反应极快。
锌溶在氧化性的硝酸中并不能放出H2,而生成NH4+同时还有一些副反应生成棕色的气体NO2以及NO。
4Zn+10HNO3(稀)=4Zn(NO3)2+NH4NO3+3H2O
在碱中,和碱反应生成锌酸盐,也放出氢气:(https://www.xing528.com)
Zn+2NaOH=Na2ZnO2+H2↑
锌在水中及盐的溶液中稳定区域在pH=6~11之间(见图19-1)[18]。小于或大于这一区间都容易很快被腐蚀或溶解。锌在空气中由于水气和CO的共同作用在表面常生成一层碱式碳酸锌
ZnCO3·Zn(OH)2,它有保护锌的作用。但在潮湿和酸性的空气中腐蚀严重时,有时会生成白色的腐蚀斑点俗称“白锈”。钎焊时需要有效地除去这层膜和斑点。
Zn(OH)2容易和氨的盐生成易溶于水的络合物,因此钎剂中含有氨的盐有利于去除氧化膜。
Zn(OH)2+4NH4Cl=Zn(NH3)4Cl2+2H2O+2HCl
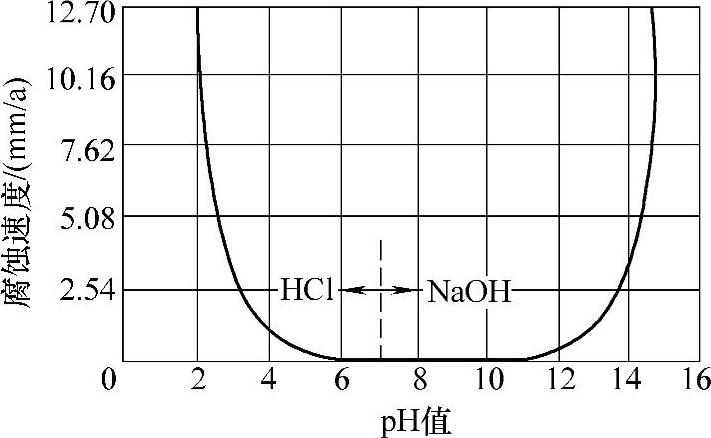
图19-1 锌在介质中的稳定区域 Fig.19-1 Stable area of zinc in water medium
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




