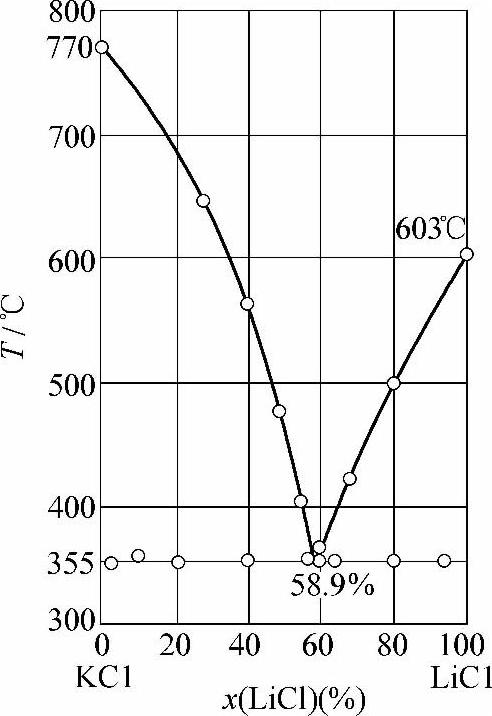
图2-4 LiCl-KCl系[13] Fig.2-4 System LiCl-KCl[13]
2.5.1.1 氯化物钎剂
氯化物钎剂由基质、去膜剂和界面活性剂三个功能部分组成[12]。
1.氯化物钎剂的基质是由碱金属或碱土金属的氯化物混合熔盐组成
基质的化学性质稳定,和铝基本不发生反应。它的作用是:融态基质熔盐覆盖在钎焊的接头上,隔离空气;调节基质的成分,使其熔化温度与钎料的熔化温度匹配;基质还是钎剂中其他成分的溶剂。
为配合Al钎料Al-Zn(381℃)、Al-Si(577℃)的熔化温度,钎剂基质的熔化温度应能从350℃至560℃做任意调整。最常用的基质是含LiCl的混合熔盐。KCl-LiCl二元系(见图2-4)的共晶温度只有355℃[13],是所有碱金属或碱土金属氯化物二元系中共晶温度最低的一个,适合搭配Al-Zn钎料用的钎剂。在其他钎料所使用的钎剂中,需要较高的熔化温度,通常应用LiCl-KCl-NaCl三元系的熔盐作基质。此三元系的相图[14]如图2-5所示。由图2-5可见,体系内存在两个三元包晶点P1和P2和一个三元共晶点E,系中无变点(nonvariant point)的温度与组成见表2-6。由于研究的作者不同,图2-4与图2-5所示的数据有稍许差别。图2-5中各无变点组成的熔盐用作基质最为理想,因为它们熔化时熔化温度区间为0,不会产生初熔至全熔之间时间拖沓的不爽。当基质熔化温度需要高于P1的406℃时,最好选择P1→m线上的某点,因为这时熔盐的熔化区间比其他液相面上各组成的熔化区间相对较小。
比较理想的基质熔盐系还有LiCl-SrCl2[15]系(e点475℃)、LiCl-KCl-SrCl2系[15](E1402℃、E2328℃、P1340℃、e2487℃)、LiCl-KCl-CaCl2系[16](E1340℃、E2425℃、e2475℃)。
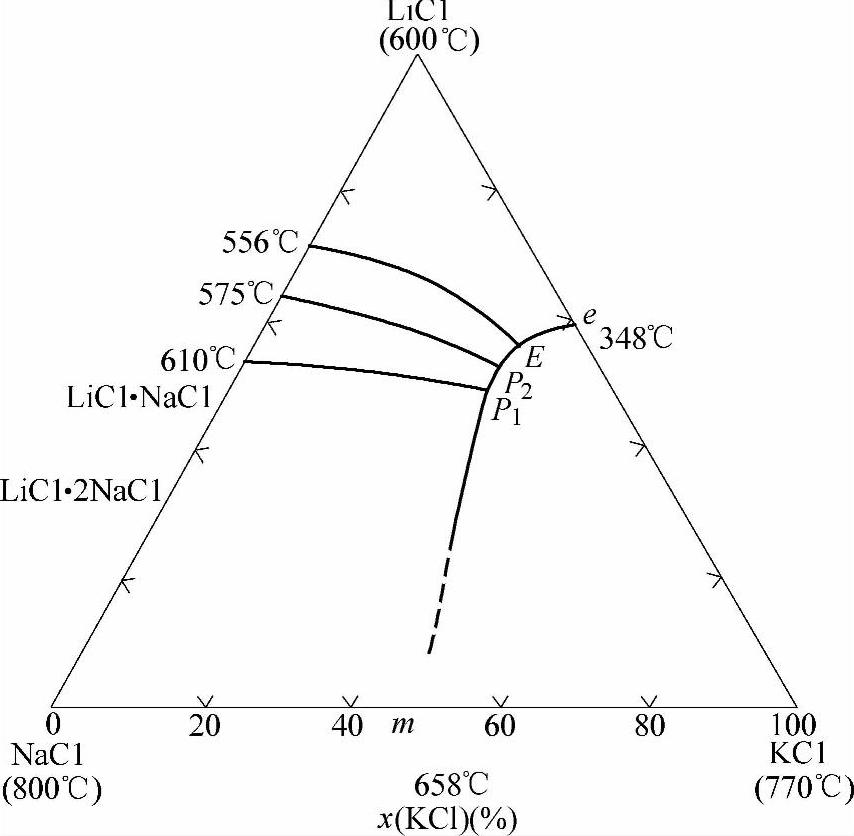
图2-5 LiCl-KCl-NaCl系相图[14] Fig.2-5 Phase diagram of LiCl-KCl-NaCl System[14]
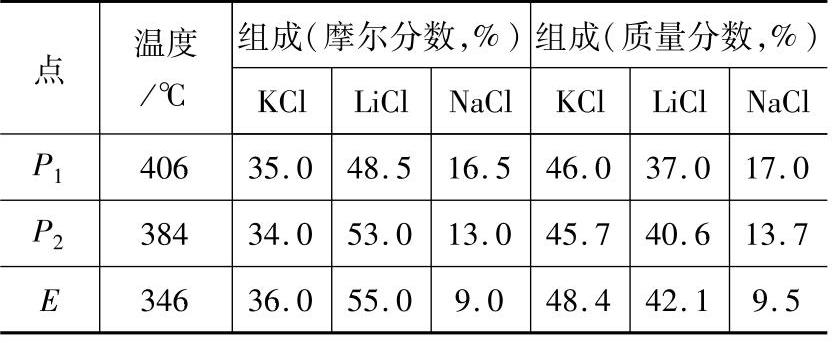
表2-6 LiCl-KCl-NaCl系无变点的温度与组成Table 2-6 Composition and temperature of nonvariant points in system LiCl-KCl-NaCl
含LiCl的基质有较高的活性(见2.6节),但最大的缺点是吸湿,在潮湿空气中能吸水最后完全变成溶液。吸水后的基质在加热脱水时,LiCl会水解产生Li2OHCl,提高了pH值,将大大影响钎剂的活性。不含LiCl的基质可选择的范围很窄,CaCl2-NaCl-KCl[17]系(e506℃、E1504℃)和SrCl2- NaCl-KCl[17]系(E1523℃、E2504℃)几乎是仅有可供选择的体系,并且熔化温度偏高,只适于配制高温的铝钎剂。
2.氯化物钎剂中的F-是破坏铝氧化膜的主要成分
多个研究者[18]已经证明,在上述基质中含F-浓度不大时,氧化膜在其中溶解量微不足道,而是松动、起皱、破裂、脱落或剥离。剥离的速度随氟化物浓度增加而加快。大沢直[19]认为,去膜的能力与氟化物的种类有关,碱金属和碱土金属氟化物的去膜能力比氟化铝和冰晶石的强。LiF有最强的去膜能力。他的试验是选用LiF、NaF、KF、CaF2、AlF3、Na3AlF6六种氟化物在LiCl-KCl共晶中的质量分数均为5%时做出的。显然他忽略了同重的氟化物,其氟离子浓度是不同的。LiF的相对分子质量最小,各种氟化物同重时,它含LiF分子的量最大,也就是F-浓度最大,当然会具有最佳的去膜效果。由此可见,去膜效果主要是和F-离子浓度有关,和化合物的种类并无重大的关系。
氟化物加入基质一般会提高基质的熔化温度[13],因此在确定钎剂的熔化温度时,应注意加入氟化物后的综合效果。通常,以LiF为例,其加入量很少超过3%~4%(质量分数),这是比较理想的,其他种类的氟化物要相应多加些。
3.氯化物钎剂中的界面活性剂主要是重金属离子
在表2-5中,凡在Al之后电位比Al正的金属离子原则上都可以作为界面活性剂。钎剂反应时,金属离子被还原沉积在铝母材表面上,Al则溶解进入钎剂成为Al3+。这种传质反应将显著降低钎剂和母材间的界面张力。为了使钎料最大限度地润湿母材,钎剂和熔化的钎料间也应该使之产生类似的传质反应(见1.2.2节)。由此可见,用铝基钎料时,可以用Zn2+作界面活性剂。但是当用锌基钎料时,钎剂中仅含Zn2+,虽能和Al母材产生传质,但不能和锌基钎料间产生传质,因此也就不可能最大限度地降低钎料和母材间的界面张力。在这种情况下,钎剂中至少应含一种在Zn2+以后,即比Zn更正电位的金属离子,如Sn2+、Pb2+等。
在表2-5的序列中,比Al电位正的元素列中,离Al越近的离子被Al还原的速度越慢,离得越远还原速度越快,这是因为它们之间组成电池的电动势越远越大,还原的动力越强的缘故。作为界面活性剂的重金属离子的被还原速度应和析出金属与母材合金化的速度相匹配,即还原析出的金属应能及时和母材润湿并合金化。如果析出速度过快,来不及合金化,则析出金属会呈微粒状悬浮在钎剂中,表现的征状是钎剂发黑。在用Bi3+等离子作界面活性剂时,常能看到这种现象。
在这种情况下,控制界面活性剂中的重金属离子,以减缓它在铝母材面上的析出速度有三种途径:一是选择靠Al稍近的重金属离子;二是降低重金属离子在钎剂中的含量;三是降低钎焊温度。
在铝母材上,重金属离子被还原析出成金属并和母材合金化后,在钎焊温度下应呈薄层的液态,这样才会具有更高的活性。欲达到这一点,可以选择析出金属本身熔点较低的金属的盐来作为界面活性剂,例如,在钎焊温度(≈600℃)下呈熔化态的金属有:Zn(419℃)、Cd(321℃),Sn(232℃)、Pb(328℃)、In(157℃)、Bi(271℃)、Tl(304℃)等。可以用它们的氯化物来作为界面活性剂。此外,也可以选择和母材合金化后在表面形成多元液态金属共晶的那些盐来作为界面活性剂,例如,K2SiF6(析出的Si形成Al-Si共晶577℃)、K2GeF6(Al-Ge共晶420℃)、CuCl2(Al-Cu共晶548℃)、AgCl(Al-Ag共晶567℃)等。
界面活性剂被还原析出的金属和母材的关系基本有两种类型:一种是和母材之间有相当的互溶度,析出的金属和母材润湿并铺展,而且和母材产生进一步的反应,例如,Zn2+→Zn↓后和铝母材互溶并向母材中渗透(见图1-21);另一种是和母材极难互溶,析出的金属在铝表面呈半润湿的液滴状。图2-6所示为LiCl-KCl-NaCl-LiF-CdCl2钎剂600℃与铝反应后的情况。析出的Cd虽与Al润湿但不能铺展,因此单独使用与Al互溶度极小的那些金属的盐作为活性剂是不适宜的,这包括Cd2+、Pb2+、Tl2+等。

图2-6 钎剂中仅含界面活性剂CdCl2时600℃析出的Cd呈液滴状 Fig.2-6 Flux containing only one surfactant CdCl2,the precipitated Cd(at 600℃)wetting on aluminum as a drop but no spreading
一项对钎剂中界面活性剂的浓度与等量钎料铺展面积的关系(见图2-7)的研究[12]表明,随着界面活性剂含量的增加,钎剂的活性随之增加,但有一最高点,过此点活性反而下降。对不同离子,此最高点含量不同,但换算成摩尔分数则几乎都为3%,说明钎剂的最大活性与析出金属的原子个数有关。因此使用不同的界面活性剂时,其所用的质量分数应该是不相同的。
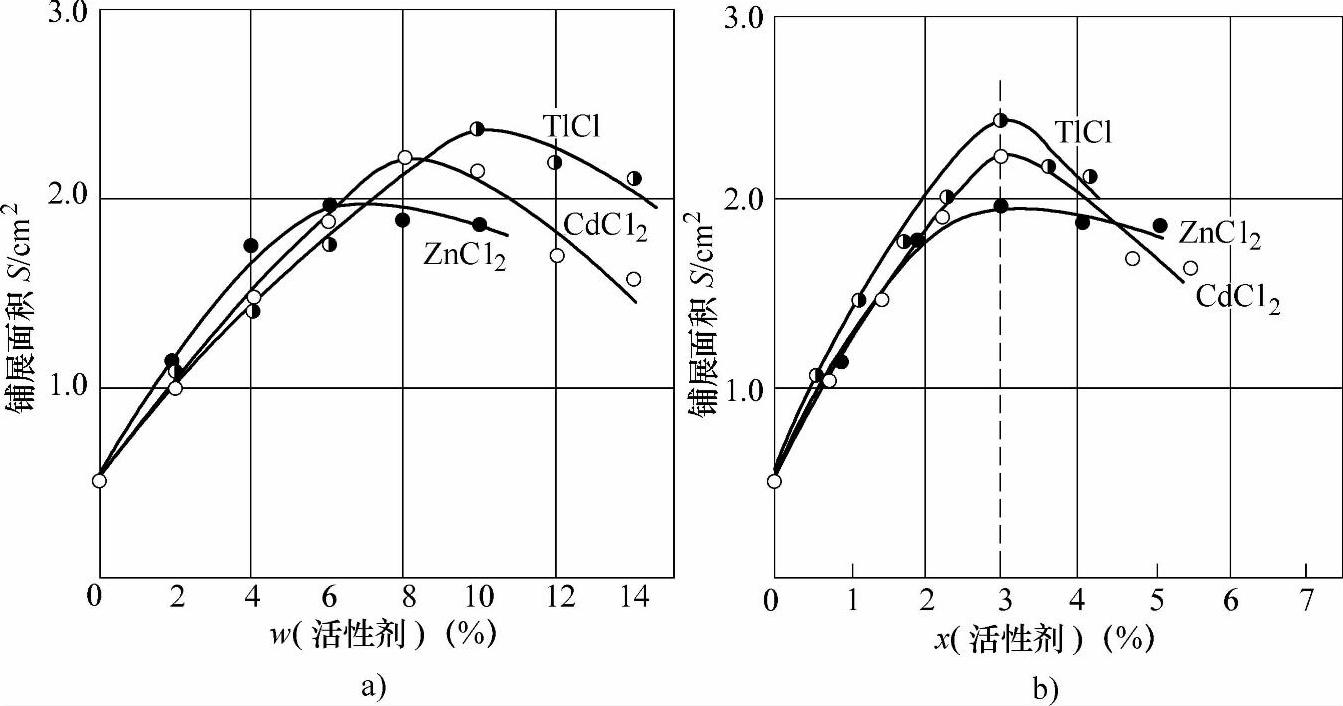
图2-7 界面活性剂的浓度与钎料铺展面积的关系 Fig.2-7 Relationship between spreading area of filler and concentration of surfactant in fluxes
钎剂活性持续的时间随界面活性剂的不同而不同,图2-8[12]所示为几种活性剂的失效曲线。可以看出,在620℃时,ZnCl2是一个速效但不持久的活性剂。速效,显然是由于Zn与Al间有最大的电极电位差,还原速度快;不持久,是因为Zn与Al有很大的互溶度,还原出来的Zn极快渗入母材所致。CdCl2则是缓效的,和Cd2+—Al间还原速度较慢,互溶度又很小有关。TlCl在开始阶段有一活性降低的过程,可能与Tl+首先有一下短暂被氧化为Tl3+的过程有关。由此可见,单独用哪一个活性剂都有缺点,搭配使用则有较好的效果。
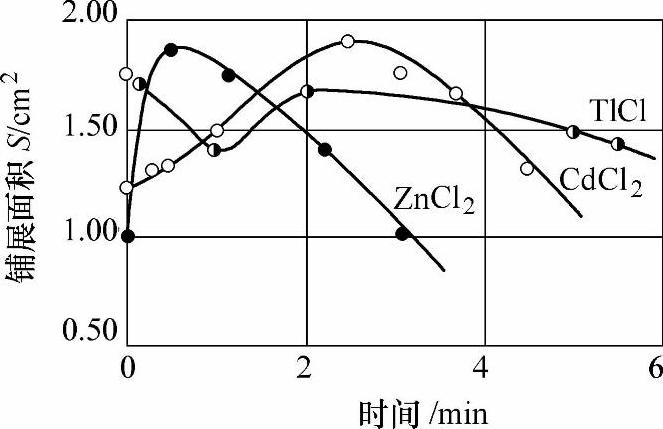
图2-8 几种活性剂的失效曲线 Fig.2-8 Deactivation curves of different surfactants in flux
和加氟化物提高钎剂的熔化温度不同,重金属氯化物的加入常有降低钎剂熔化温度的趋势。
4.氯化物钎剂的配制和检验
氯化物钎剂的检验标准在配方正确时主要有四项:一是熔化温度(液相线)合乎标准(即和钎料液相线的搭配);二是在坩埚中熔化后应完全透明澄清,不能有絮状物或不溶的渣滓;三是钎剂粉末干燥,不能吸水,表现是钎剂粉末不沾玻璃瓶;四是钎剂的水溶液的pH值不能超过6.5。
钎剂的各组元中以LiCl、ZnCl2吸水最厉害,脱水不慎,将会引起水解并产生Li2OHCl和Zn(OH)Cl,因此提高了钎剂的pH值并产生絮状物,这将阻碍钎料的流动。参考文献[12]介绍了四种脱水方法,认为,真空脱水最佳,但在小规模的配制时,用NH4Cl与LiCl或ZnCl2共热脱水是一个比较方便而又能有效抑制水解的方法。在钎剂各组元中,最有害的杂质是Fe3+和Mg2+,它们的存在是引起钎剂中产生絮状物的另一重要根源。
钎剂以熔融法配制然后粉碎的方法最为理想。既能保证绝对均匀,又能保证干燥和没有水解。
钎剂在熔融为液态时,基本上解离为单个的离子,即Li+、Na+、K+、Zn2+、Cd2+等阳离子和Cl-、F-阴离子,和加入原始化合物的种类已经毫无关系。例如,2LiF和ZnCl2在一起熔化后与ZnF2和2LiCl在一起熔化后的结果是完全一样的,因为熔体中都是单个离子并且数量一般多。在一些文献和手册中,常可以看到许多不同形式的配方,可是仔细一看,实质并无分别。
5.钎剂的实际配方
表2-7列出了已发表或已成为商品的铝用硬钎剂的配方和应用。
表2-7 铝用硬钎剂的配方和应用Table 2-7 Composition and application of aluminum brazing fluxes

(续)
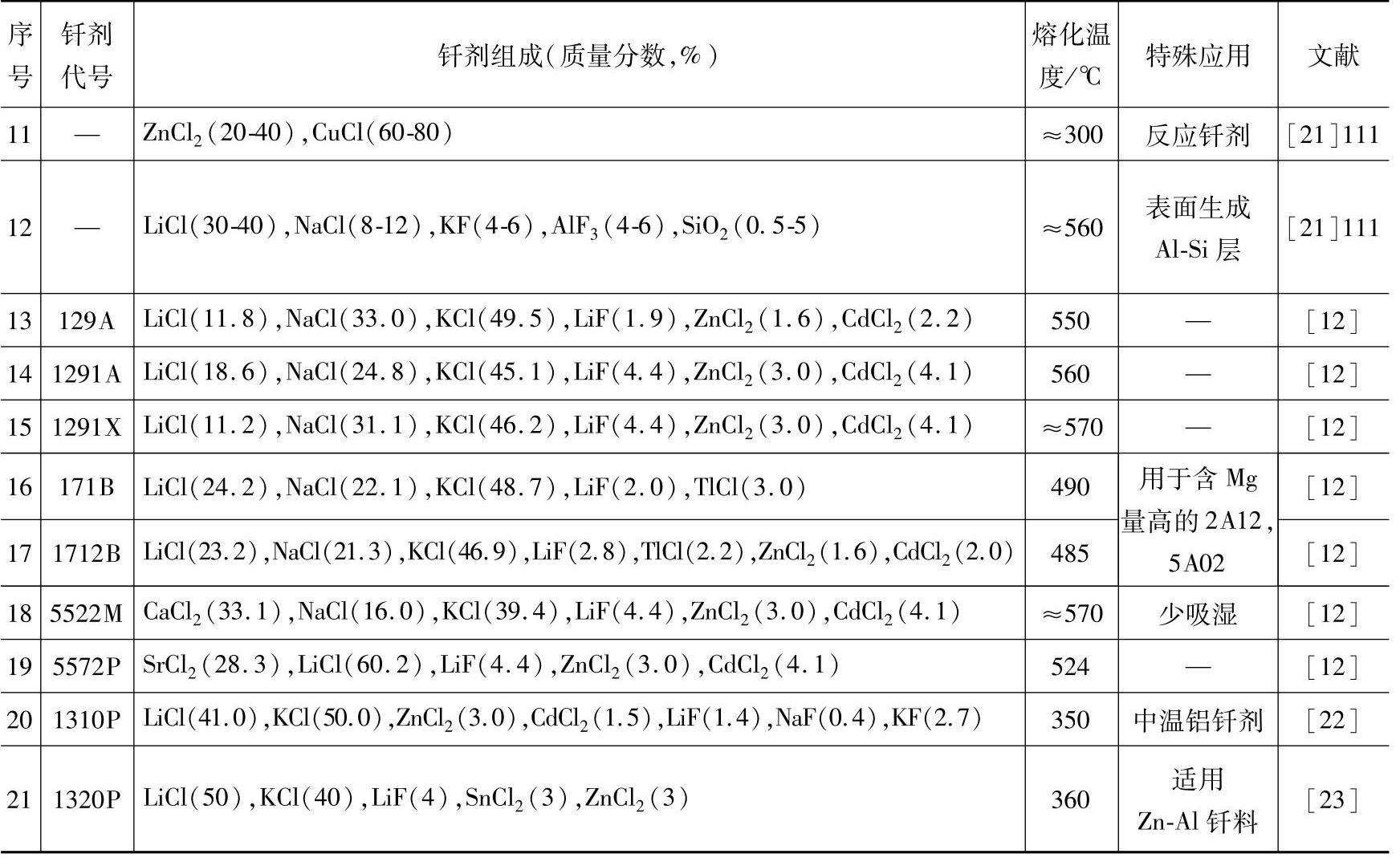
钎剂的实用效果与组元中有害杂质(Fe、Mg等)的含量和配制工艺有很大的关系。如果组元中,特别是LiCl、ZnCl2、SnCl2等脱水不尽或发生水解,将大大降低钎剂的活性。钎剂应当采用熔炼方法配制,然后在密闭下球磨粉碎。直接用有关的盐不经熔融直接在室温球磨混匀是不可取的。
在表2-7中,序号为17、18的171B和1712B钎剂对于含Mg量较高的铝合金有特殊的活性,其中应用了界面活性剂Tl+(铊)。它的特殊活性机制尚未有深入研究,看来它与镁在固相有适当的互溶度,以及它与镁之间有很大的熔盐电位差是促成它易被镁还原并合金化的原因。其他所有界面活性剂离子,除了Zn略强外,都不具备这一条件。可能这是它去除镁氧化膜活性较强的原因。遗憾的是金属Tl,包括所有的铊盐都是被管制的B级剧毒品,这就限制了它的使用,因此在特殊条件下必须使用时,应该特别注意它的安全防护。此外,Cd2+离子也是有毒的,它的特殊优点在于容易脱水,不易吸湿也不易水解,比Zn2+、Sn2+稳定得多。这是它难于被完全取代的主要原因。
在铝母材中,随着Mg含量的增加,氯化物钎剂的钎焊性越来越差。当Mg的含量超过1%(质量分数,下同)时,钎焊过程变得非常困难,甚至被认为不可钎焊。有意思的是,对于镁含量超过95%的镁合金,如AZ31B,普通铝的氯化物钎剂却又具有相当的活性,钎焊过程并不太难进行。Wa-tanabe[136]的报告令人思考良多。他用成分为59.7%CaCl2-18.5%LiCl-21.8%NaCl(摩尔分数)的钎剂和成分为34.5%Mg-64.5%In-0.8%Al-0.2%Zn(质量分数)的钎料,在低于480℃时,成功地钎焊了AZ31B镁合金。报告的表述虽然扭捏兜圈,不愿直言,但还是看得出无论在钎剂还是在钎料中,他都尽量降低或回避使用Zn2+和金属Zn。显然,Zn-Al和Zn-Mg有着截然不同的相关系。前者易互溶,有大面积的固溶体,而后者却生成高熔点的化合物MgZn2。这严重影响含Zn2+的钎剂或含Zn的钎料在高Mg母材上的活性、润湿和铺展。要想因循Zn-Al的相关系,In-Mg或Cd-Mg是仅有的选择,它们之间也是生成大面积的固溶体而没有化合物。这很可能就是Watanabe为什么选用In-Mg合金作为钎料基础的原因。他所用的LiCl-CaCl-NaCl系基质熔盐相图如图2-9所示。
为什么普通氯化物铝钎剂对含Mg1%(质量分数)以上的Al-Mg合金钎焊困难而却在钎焊AZ31B这样高Mg合金上反而会有相当的活性?从Mg-Zn的二元相图上可以看出:当Mg的量超过50%(质量分数),或Zn的量很低时,已经离开了化合物MgZn2的相区。也就是说钎焊时铝的氯化物钎剂在AZ31B上不再会有生成MgZn2化合物的干扰。
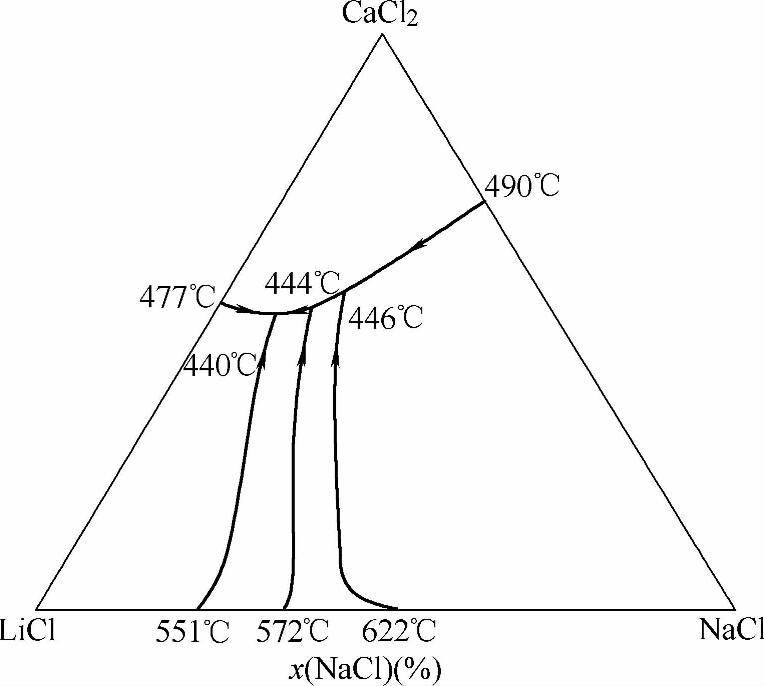
图2-9 LiCl-CaCl2-NaCl系熔盐相图 Fig.2-9 The phase diagram of system LiCl-CaCl2-NaCl
在浸渍钎焊使用的盐浴钎剂中,往往使用AlF3兼作去膜剂和活性剂(见表2-7的序号4),而不使用重金属盐。AlF3溶于LiCl-KCl共晶熔盐中析出F-或形成AlF4-离子,起到去膜作用是可以理解的,但它的活性作用却是间接的。当浸渍钎焊的盐浴槽用耐火材料砌成时,耐火材料中SiO2是主要成分之一,它在含氟的熔盐中有一定的溶解度,进入熔盐后形成SiF26-离子。钎焊时,它在Al面上被还原析出元素Si,同时与Al合金化,这个传质过程起到了活化作用。耐火材料中Si的溶入速度大体和它沉积在铝面上的速度相当,而维持了盐浴中SiF26-浓度的平衡,不需额外时时添加其他活性剂。通常使用的重金属盐活性剂,如在这里使用则有很多弊病,不但没有上述的优点还会因重金属沉积不能完全和铝合金化,悬浮在熔盐中而弄脏整个盐浴和焊件,使得焊件难于清洗干净。图2-10所示为LiCl-KCl-AlF3系相图[13]。图2-10a所示为这个体系的等温线图,图2-10b所示为体系在LiCl-KCl多温侧面上的中心投影。图中的数据点序号下面括弧内的数值为AlF3的摩尔分数,图的横坐标为KCl∶LiCl,这样就可以很容易从图上得出三元系中二元共晶线上不同序号点液相线的组成和熔化的温度。
2.5.1.2 氟铝酸盐钎剂(Nocolok钎剂)
氯化物钎剂的吸湿不但使得它保管和使用不便,特别是焊后的清洗十分费事并有废水的污染。1963年一篇荷兰的专利[25]首先提出了利用AlF3- KF共晶作为钎剂。KF-AlF3系相图如图2-11[26]所示,图2-12所示为它的细部。
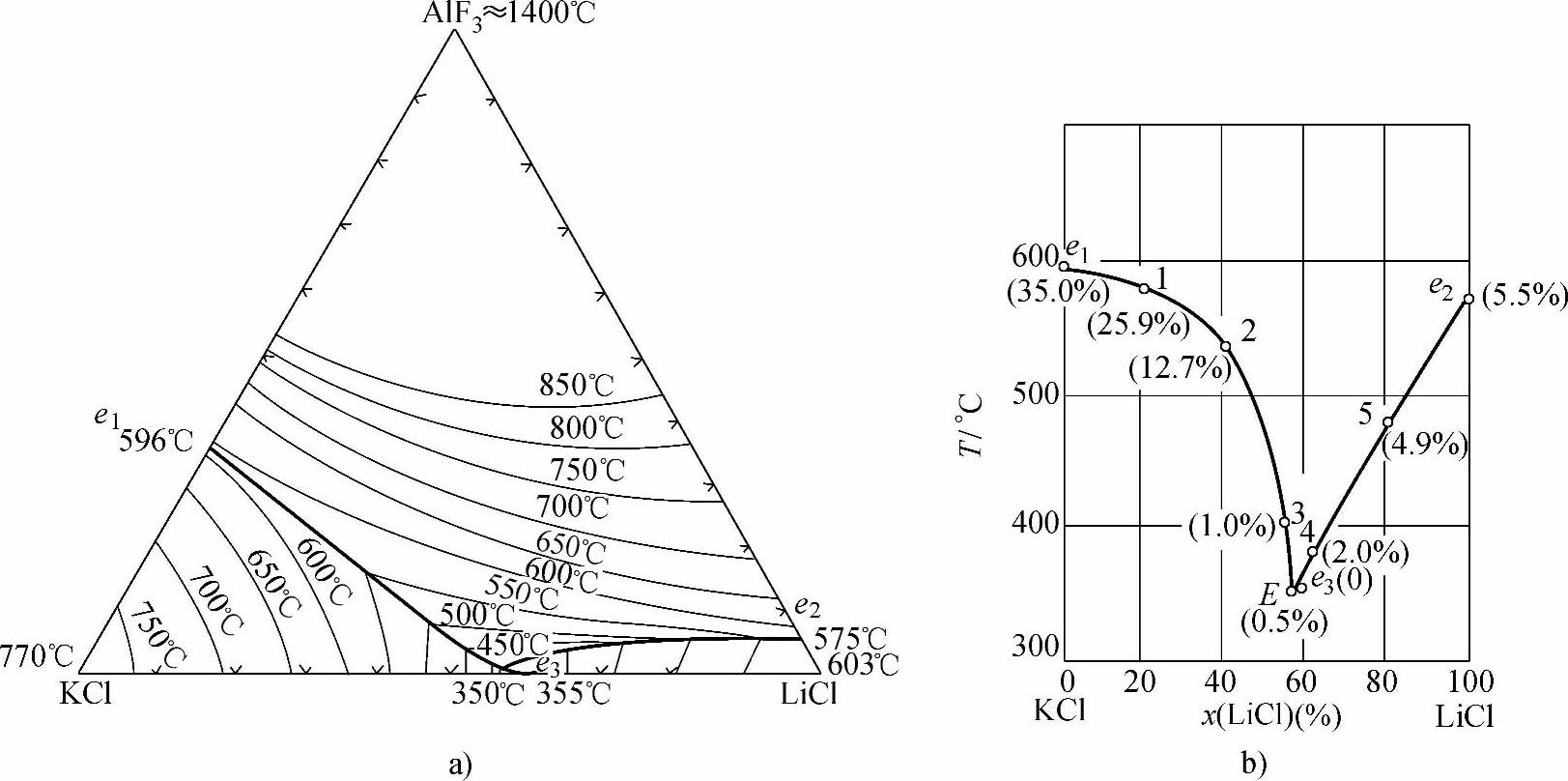
图2-10 LiCl-KCl-AlF3系相图[13] a)等温线图 b)三元系在LiCl-KCl多温侧面上的中心投影 Fig.2-10 Phase diagram of LiCl-KCl-AlF3system[13]
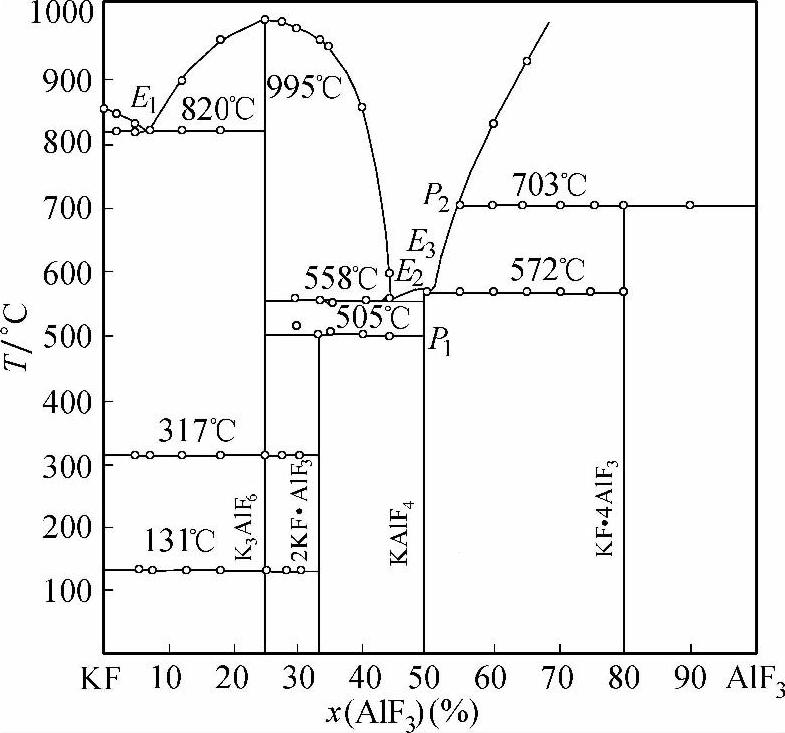
图2-11 KF-AlF3系相图[26] Fig.2-11 Phase diagram of KF-AlF3system[26]
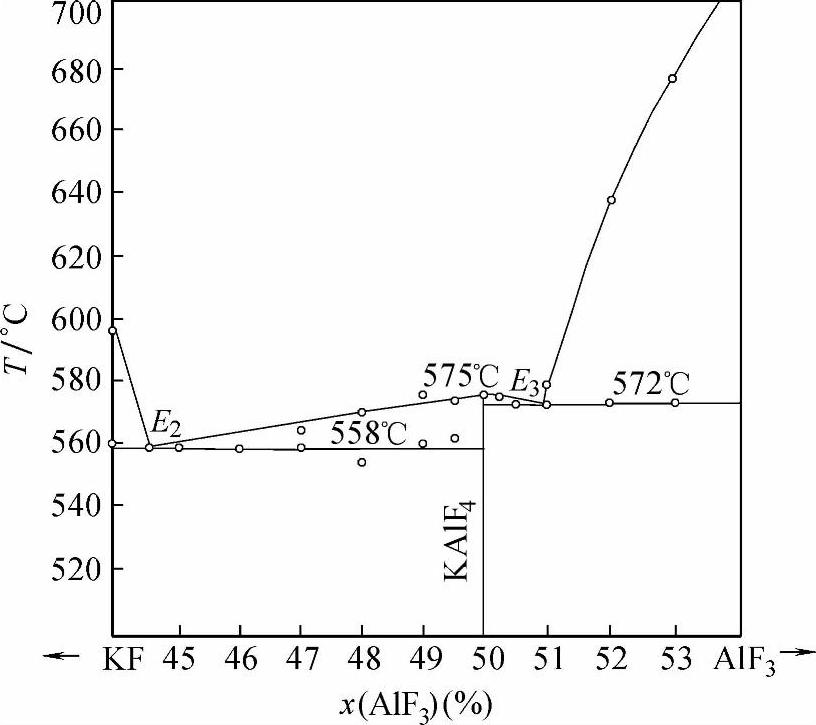
图2-12 KF-AlF3系相图x(AlF3)=44%~54%间细部[26] Fig.2-12 Fine-scale phase diagram of KF-AlF3system between 44 and 54 mol%AlF3[26]
这一钎剂在20世纪70年代得到迅速发展[27],后来加拿大的Alcan公司将它付诸应用并取名No-colok方法,表示无腐蚀之意(non-corrosive-look)。此种钎剂在水中溶解度很小,使用时制成水悬浮液喷布于工件之上。烘干后形成一层极薄的药膜,然后入炉钎焊。当然,它也可以像普通钎剂那样使用。
氟铝酸盐钎剂应用得最广的是钾盐系。因为它的熔化温度为558℃,偏高,只能应用于纯铝及少数铝合金,如3003等。近年也发展了熔化温度较低的铷盐系和铯盐系钎剂。
1.氟铝酸钾钎剂的制备与检验
本钎剂应用的是KF-AlF3系中两个中间化合物K3AlF6与KAlF4间E2点共晶成分的熔盐(见图2-11和图2-12),x(AlF3)=44.5%或w(AlF3)=53.7%,熔化温度为558℃。钎剂的成分必须十分准确才能获得558℃的最低点,这是钎剂配制的关键。如果KF量偏高,熔化温度会迅速升高而不能使用。此体系中有自由度为零的三个组成点,即E2、KAlF4和E3。熔化温度分别为558℃、575℃和572℃,而它们的熔化区间都为零。也就是说,加热时,少量钎剂熔化开始和结束瞬间完成,毫不拖泥带水。如果钎剂合成时组成不准确,不处在这三点上,而是在它们之间,特别是在E2—KAlF4之间,这时因为熔化区间有10℃左右,熔化时就会有些拖沓不爽。配制的成分如果AlF3含量偏高,而超过E3点的组成[x(AlF3)=51%或w(AlF3)=60%],这时熔化温度将会迅速升高而不能使用。
(1)氟铝酸钾钎剂的制备 氟铝酸钾钎剂的制备方法,综合文献报道约有下列各种:
1)用定量的AlF3和KF加水磨成糊,然后在低于200℃烘干1h[28],或将AlF3和KF加入50℃的水中,充分搅拌使反应完全,产物在100~550℃温度下蒸发至干并加热[29]。
2)用定量的AlF3和KF加热熔融,冷却物磨细至150~200筛目[30]。
3)分别合成K3AlF6[31]和KAlF4[32],然后将它们按比例混匀成图2-11中E2点的组成。
4)将无水AlF3和KF脱水后的干粉按比例混匀研细,在300℃下焙烧1h[33]。(https://www.xing528.com)
5)将定量的Al(OH)3溶于HF中,然后用定量已知浓度KOH溶液处理。温度保持30~100℃、pH<4[34,35]。
6)将无定形的Al(OH)3加入到HF和KF(或KOH、K2CO3)的混合液中。温度50~60℃,pH=5~10。由此可得到粒度细、比表面大、易于在水中悬浮的钎剂[36]。
7)将定量的Al(OH)3或纯铝的金属屑溶在定量的KOH溶液中,生成KAlO2和KOH的混合液,再用过量的HF转化为氟铝酸钾钎剂[37]。
8)将定量的Al(OH)3溶于稍过量的HF中,获澄清液,用定量的K2CO3溶液处理,终了的反应液pH<4[38]。
以上各方法中,以5)~8)四种方法更便于量产。由于要精确称量,Al(OH)3要绝对干燥,否则要事先在100~110℃烘干。KOH除了干燥以外,还需要密封没有吸收CO2的产品,否则称量不易准确。在这一点上,用K2CO3代替KOH更有优点,因为K2CO3稳定而不甚吸潮,价格也较便宜。
以上还只能算是制备的粗略叙述。严格来说,应该配合化学分析,精确控制Al3+和K+的量,才能够得到E2、K3AlF4或E3点准确组成的钎剂。
在合成反应过程中,应保持适当的温度并要长时间充分搅拌令其反应完全。这时反应的产物是白色的糊状液。为了防止水解,澄清液中允许有稍过量的HF。最好不要采取过滤获取沉淀的方法,而宁可连汤蒸干。为了防止酸性的溶液对蒸发容器(如不锈钢容器)的腐蚀,不妨向乳状液中滴加少许NH4OH,将乳状液调至pH≈6。
为了防止蒸发过程中发生局部水解,蒸发的最后阶段应该在低于80℃下进行真空蒸发,这一点对于获得高质量、熔化温度准确的产品至为重要。
如果对以上所得产物进行XRD分析,可以看出,产物主要是由K2AlF5(或2KF·AlF3)相和较少量的KAlF4相所构成。这从图2-11的相图上可以很清楚地看出来。如果产物脱水不彻底,还会出现K2AlF5·H2O相。只有升温到505℃以上或在此温度以上进行热处理,才会得到K3AlF6和KAlF4的混晶。
当然,成分为K3AlF6+KAlF4共晶点E2组成的钎剂是最理想选择。如果配成准确的KAlF4(m.p.575℃)或E3(熔化温度572℃)点组成的钎剂,也会有良好的效果,不过熔化温度偏高,工艺操作不易。
工业原料Al(OH)3中难以避免的Si杂质是一个有益的“歪打正着”的活性剂[37],忌讳最大的杂质是铁,w(Fe)不要超过0.1%,对其他常见杂质没有特别严格限量的苛求。
无论用哪种方法制备的钎剂,都应符合以下几个基本要求:
1)成分准确。
2)不含游离的KF。
3)熔化温度约为560℃,最高不得超过565℃,熔化时没有明显的温度区间。
4)在铝面上加热熔化时,钎剂迅速铺展开来,不得有难熔的残余物堆积,钎剂也不得发黑(钎剂熔化的中心有一片发亮的合金层是允许的,那是析出的杂质Si与母材形成的Al-Si液态合金层)。
5)粒度细,比表面大,易于在水中悬浮。
(2)氟铝酸钾钎剂的检验 成分与熔化温度是一致的。检验钎剂,首先就要精密测定它的熔化温度,最好用目测变温法或DTA方法[39]。检验是否含有游离的KF,可以用去离子水或蒸馏水洗涤钎剂1~2次,在100℃烘干后再测熔化温度。如果洗后熔化温度上升,或者熔体不透明,说明原来钎剂中含有游离的KF。
钎剂的粒度要求在2~50μm的范围内。此外,还应做钎剂在水中沉降速度的测定。可在带刻度的试管中,将钎剂与去离子水配成质量分数为5%的混合液充分摇匀后,垂直静置10s,不应在试管底部看到明显的固体沉降物。
2.氟铝酸钾钎剂的物理化学性质
以KAlF4为主体的氟铝酸钾钎剂,在水中溶解度很小(0.2%~0.4%),但热稳定性并不佳,在空气中加热时不同程度上有:
2KAlF4+3H2O=2KF+Al2O3+6HF↑和 4KAlF4+3O2=4KF+2Al2O3+6F2↑的反应发生。第一个反应主要是在潮湿的空气中发生,空气中的水分在钎焊的温度下(600℃)明显地将钎剂水解,留下不熔的残渣Al2O3。第二个反应主要是在绝对干燥的空气或氧气中进行,钎焊过程中它不是主要的,并且只在800℃以上才能较明显地察觉到。
钎剂中存在的另一成分K3AlF6(钾冰晶石)在加热过程中也有类似的反应,但要比KAlF4稳定得多。钎剂的水解主要产生于KAlF4。
KAlF4和K3AlF6都属于弱酸盐,容易被强酸破坏,因此钎焊后的钎剂残渣如果需要清除时,可以用稀硝酸浸泡除去。强酸中以HNO3对铝母材伤害最小。
固态的Nocolok钎剂很稳定,不吸潮,难溶于水,也不溶于有机溶剂。但熔态的Nocolok钎剂强烈地腐蚀玻璃、陶瓷等硅酸盐。
熔态的Nocolok钎剂具有超低的黏度和超低的表面张力。盛在铂坩埚中的熔融体会自动爬出坩埚壁,有类似液氦那样的“超流动性”。实验表明,熔态的KAlF4是一个具有分子态结构比例很高的熔盐[40],许多离子态的氟化物盐类在其中都难溶化。
KAlF4固态晶体属四方晶系,a=35.58nm,c=61.49nm,是一个固液同分化合物。Колосов[24]研究了KF-AlF3体系在838K(565℃)时的蒸气压。表明组成为KAlF4时的蒸气压要比其他组成的蒸气压大得多,大3个数量级以上。蒸气由KAlF4单分子和(KAlF4)2双分子共同组成。这一事实旁证了熔态KAlF4具有分子结构的特征,也说明KAlF4有可能用作气体钎剂。
3.氟铝酸钾钎剂的应用
氟铝酸钾钎剂不太适用于火焰钎焊,这是因为可燃气体燃烧以后的废气主要就是水蒸气(和CO2),火焰的高温容易使KAlF4水解,使得水解产物脱水后的Al2O3残渣增多。这时要多费许多钎剂才能完成钎焊的过程,并且接头很不美观。有经验的焊工常在施加钎剂以前将工件充分预热,达到钎剂熔化的温度后再施钎剂,尽量缩短火焰和钎剂接触的时间,只有这样才能获得比较满意的工艺结果。
炉中钎焊是最可取的办法。在干燥空气中进行本钎剂的钎焊已可获得足够满意的结果。我国华北以北的北部地区,冬季12月至翌年2月间空气的相对湿度常低于25%,直接进行炉中钎焊是完全可行的。其他季节和地区应该应用氮气保护的炉中钎焊,关键是要控制气氛中的水分,其次是含氧量。
4.氟铝酸钾钎剂的改性(modification)
在应用氟铝酸钾钎剂的基础上,近年来发表了大量的文献讨论Nocolok方法的改进。总结有两个方面:一是在氟铝酸钾钎剂中加入第三种或更多种盐以增加钎剂的活性及其他性能,另一是发展氟铝酸钾钎剂的新的应用方法。
硅的存在可以使氟铝酸钾钎剂的活性大为增加[37],这是原料中已有的杂质起到的意外效果。如果想进一步提高钎剂的活性,比较理想的方式是以K2SiF6的形式加入[41]。K2SiF6和AlF3-KF三元系的关系可以参阅Аидрийко发表的AlF3-KF-SiF4相图[42]。在w(Si)超过钎剂总量的2%时,析出的Si和母材反应生成的合金可以自钎,无须另加钎料。加入K2GeF6会有更高的活性,加入ZnF2[43]、PbF2[44]、ZnF2[45]或KBF4[46]都能有效提高钎剂的活性。这道理很明显,因为这些添加物的阳离子在钎焊时都会被母材还原析出,并与母材合金化成为液态的金属层,起了传质的作用。但钎剂中如果含过量重金属离子,钎焊时将会使接头颜色变暗,因为析出的重金属一时过多,来不及和母材合金化而成微细颗粒悬浮在钎剂中。而有硼的存在时,实验表明,接头往往严重发黑,因为还原出来的硼根本不能与母材合金化,这可从Al-B的相图上看出来。
在Nocolok方法的改进上,一些专利文献报道了将氟铝酸钾钎剂与一些合金粉末混合后使用,例如用锌粉[47,48]、Al-Zn合金粉[49,50]与钎剂调成浆料喷涂于工件表面,加热熔化后使工件表面形成相应的Zn层或Al-Zn层,以利进一步的钎焊。
近年来,将KAlF4当作气相钎剂的方法逐渐发展起来。一种是直接在低压非氧气氛中混入KAlF4的蒸气来进行铝合金的钎焊[51],另一种则是在铝合金零件外面用真空沉积一层KAlF4[52],然后根据需要拼装组合后再钎焊。
在Al-Si共晶钎料粉的表层用漂浮法(Floating method)沉积一层KAlF4钎剂而形成钎料-钎剂复合体[53],再用有机溶剂,如正癸醇,调成焊膏使用。
氟铝酸钾钎剂的一个缺点就是熔化温度偏高,不利钎焊工艺的操作。一些学者探讨设法降低K3AlF6-KAlF4共晶点温度的途径。因为一切离子型的氟化物都不能溶入液态的K3AlF6-KAlF4熔盐,但存有部分共价结构的氯化物却可溶。图2-13所示为AlF3-KF-KCl的熔盐相图[137]。这个体系有三个三元共晶点:其中,E2和E3共晶温度分别为534℃和541℃。较之Nocolok钎剂熔化温度降低了24℃和17℃,这是很可喜的。遗憾的是添加了KCl以后熔盐的黏度大为增加,失去了Nocolok钎剂极高的流动性和铺展性。不过这个熔盐能溶于水,方便熔渣的清洗,而在潮湿空气中又完全不吸湿。如果把它作为基质,再添加一定量的界面活性剂,还是有可能得到它实际的应用。
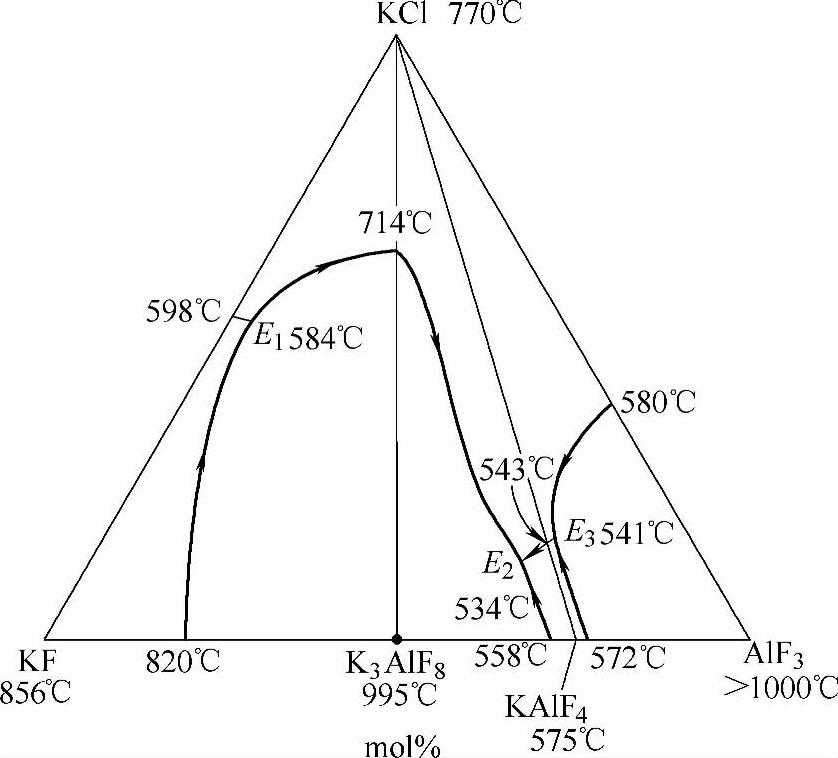
图2-13 KF-AlF3-KCl的熔盐相图[137] Fig.2-13 Phase diagram of KF-AlF3-KCl system[137]
刘赟等[138]做了向AlF3-KF共晶中添加不同量KBr后测定其熔化温度的实验。实验表明,KBr的含量为20%(质量分数)时,可以获得熔化温度为522℃的熔盐。文章认为:钎剂中形成KAlF4-K3AlF6-KAlBr4三元共晶是钎剂熔点降低的主要原因,钎焊效果良好。
5.中温氟铝酸盐钎剂
常规Nocolok方法应用氟铝酸钾钎剂的最大不足在于操作温度(600℃)太高,这也是迫于钎剂和钎料熔化温度(分别为558℃和577℃)的限制。一多半的铝合金由于过烧温度低于600℃而不能用氟铝酸钾钎剂钎焊。所谓过烧温度通常是指超过合金的固相线的温度(见表2-3),合金加热到这一温度时,晶间开始出现熔化相,从而产生结构组织的破坏。图2-14所示为主要铝合金的过烧温度[54]。可以看出,除了硬铝(2×××系)和(7×××系)以外,如果钎焊温度不超过540~550℃,则有相当多的合金是安全的。如果要考虑钎焊硬铝,那么钎焊的温度便不能超过500℃。这样,钎剂的熔化温度就要求低于480~490℃,因此要求研发无腐蚀、难溶于水而熔化温度又低于480~490℃的钎剂,就成为十余年来铝钎剂发展的重要方面。

图2-14 铝合金(AA)的过烧温度 Fig.2-14 Over burn(collapsed)temperatures of most aluminum alloys(AA)
以氟铝酸钾Nocolok钎剂为基础,加入第三氟化物组元来降低氟铝酸钾的熔化温度是理所当然的设想。而事实上,在熔盐电势序(见表2-5)Al之后元素的氟化物,包括稀土、钛、锆等金属的氟化物都不能用作钎剂的主组元。实验表明,含少量这些元素的氟化物时,它们有时还可以起到活性剂的作用,当用它们来作为降低Nocolok熔化温度的主组元时,由于含量太大,这时的钎剂就会被铝还原析出大量的金属微粒,并把母材表面弄得一团糟。事实上,可供选择的只有碱金属和碱土金属的氟化物。
根据最近一项研究表明[40,55],KAlF4熔融时,熔体中的KAlF4要呈分子态。离子型的氟化物,包括MgF2、CaF2、SrF2、BaF2,甚至含有部分共价键的LiF,在其中都难溶,对氟铝酸钾钎剂的熔化温度不产生影响。只有分子型的BeF2及其他呈分子态的铬氟化物才能够明显地降低氟铝酸钾共晶温度。AlF3-KF-BeF2相图的研究有比较详细的报道[56,57],其中有些数据颇具吸引力。例如,KAlF4-KBe2F5赝二元系截面的共晶点的熔化温度只有335℃。但由于铍化合物的剧毒,这项研究结果除了在特殊情况下,很难有实际意义[58]。
Thoma[59]发表了KF-AlF3-LiF系熔盐相图的报道,这个相图指出,组成为w(KF)=43.0%、w(AlF3)=54.7%和w(LiF)=2.3%处为一温度为490℃的三元共晶点。Yamawaki[60]根据Thoma的相图,申报了这个成分钎剂的专利保护。但经我们反复的实验,证明Yamawaki的专利根本不可信,连同Thoma的相图也都存疑。
尽管如此,但根据有经验的工作技术人员透露,LiF虽然未能有降低钎剂的熔化温度的效果,但在Nocolok钎剂中如果添加1%~1.5%(质量分数)的LiF却有可以减少钎剂用量、延长活性时间,更易工艺操作的优点,因而添加LiF常成为这些应用Nocolok钎剂单位的潜流程。为此,也有一些Nocolok钎剂的生产厂家,未做标明,却也在产品中添加了约1%(质量分数)的LiF。
一个有可靠应用前景的中温不溶性钎剂是Su-zuki[61]对CsF-AlF3系的应用。报道指出,此钎剂的熔化温度为440~480℃,专利保护成分为x(AlF3)=26%~67%,x(CsF)=74%~33%。指出,此钎剂有较高的钎焊效率,对火焰的稳定性比氟铝酸钾剂高,据称最大的优点是对含镁量高的合金有特殊的活性。CsF-AlF3系相图如图2-15所示[62]。图中可用作钎剂的共晶点E2的成分为x(AlF3)=42.0%、x(CsF)=56.0%,熔化温度为471℃。
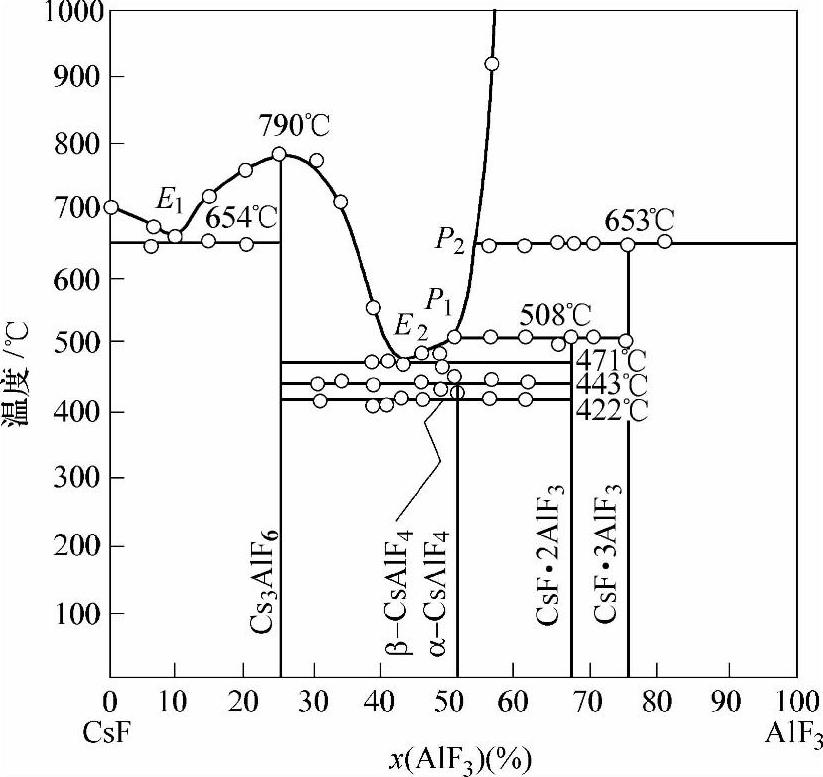
图2-15 CsF-AlF3系相图[62] Fig.2-15 Phase diagram of CsF-AlF3system[62]
对比CsF-AlF3和KF-AlF3两个体系的相图可以看出,KAlF4是个固液同分化合物,热稳定性较好;而CsAlF4是个固液异分化合物,热稳定性则很差,加热到443℃就分解。在CsF-AlF3系中利用配制钎剂的E2点其实是Cs3AlF6和CsAl2F7(即CsF·2AlF3)的共晶。纯相的KAlF4可以独立作为钎剂,而CsAlF4则不行。Cs3AlF6-CsAl2F7共晶熔盐在水中的溶解度也比Nocolok大得多,这主要是CsAl2F7的影响,它的溶解度约在0.8%~1.0%。尽管如此,它在空气中还是不吸湿的,钎焊的残留物并无腐蚀。相反,这个钎剂的残留物比Nocolok的残留物要容易清洗得多,用冷水即可将残渣清洗干净。
为了进一步降低上述E2共晶点钎剂的熔化温度,也为了降低价格昂贵的CsF的含量,1986~1987年连续发表了AlF3-KF-CsF三元系钎剂的专利[63,64],由于没有有关相图的指导,这个专利申请保护的范围很宽。专利指出,可获得最低熔化温度为460℃的钎剂,据称对含Mg量高的铝合金有很高的活性,几乎可适用于所有的铝合金的钎焊。
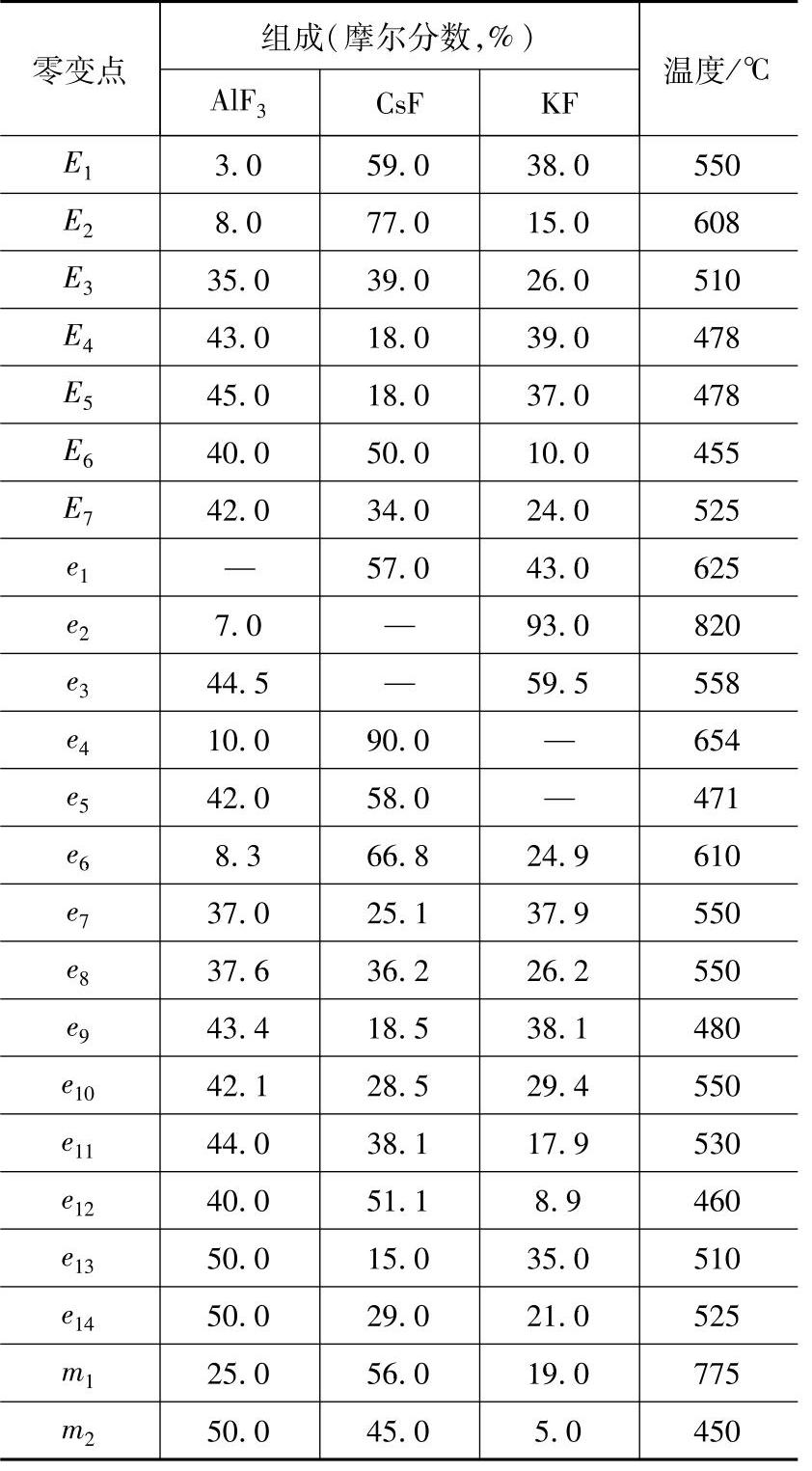
AlF3-KF-CsF三元系详细相图不久前发表[65-67](见图2-16)。这个相图的结构比较复杂,图中各零变点的组成和温度见表2-8。零变点即指自由度为零的相变点,在这里熔盐的熔化区间为零。由图及表可以看出E6(455℃)、e12(460℃)都是非常可取的组成点。温度最低的组成点在E8,本相图没有精细测定,估计熔化温度应在430~440℃左右。E4和E5的熔化温度都是478℃,和CsF-AlF3二元系的e5熔化温度471℃大体相当,但E4和E5所用的CsF要少多了,只及e5的1/3,因此利用这两个组成点配制钎剂更有经济上的意义。
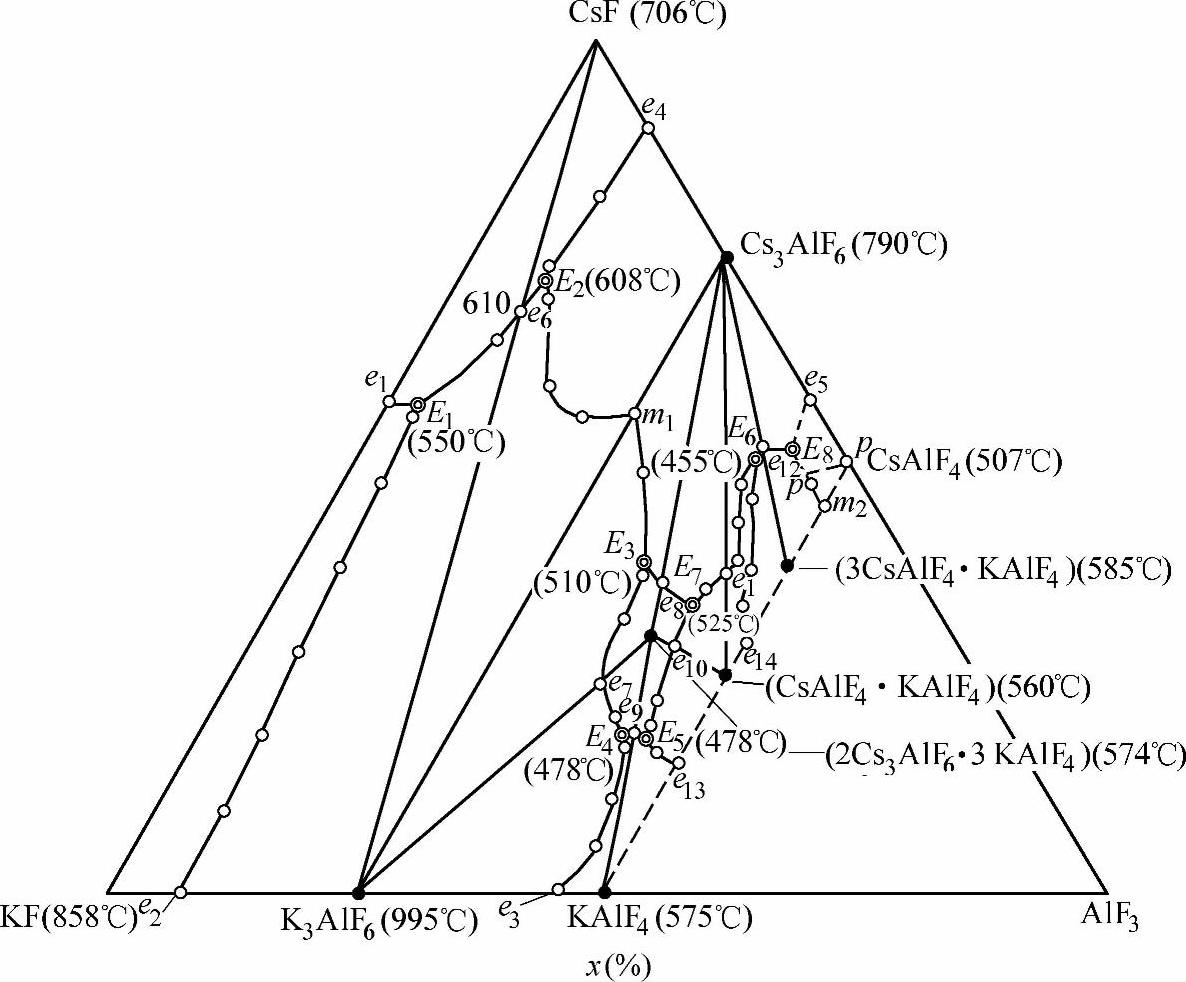
图2-16 AlF3-KF-CsF相图的正交投影图[67] Fig.2-16 Orthogonal projection of the AlF3-KF-CsF system[67]
图2-16中的E4点是K3AlF6-KAlF4-(2Cs3AlF6·3KAlF4)赝三元系中的共晶点,熔化温度为478℃。这三个化合物都是固液同分的(见参考文献[66]),热稳定性都很好。e9是KAlF4-(2Cs3AlF6·3KAlF4)赝二元系的共晶点,熔化温度为480℃,也有类似的特性。其次可选的是E3(510℃),是更稳定的K3AlF6-Cs3AlF6-(2Cs3AlF6·3KAlF4)赝三元系中的共晶点。因此,如果一个生产商企图规划这种铝钎剂的系列产品,那他们钎剂的组成点当然就应该是:e3(558℃);E3(510℃);E4(478℃);E6(455℃);E8(≈430℃)。
表2-8 AlF3-KF-CsF三元系中零变点的数据Table2-8 Nonvariant points in the ternary system AlF3-KF-CsF
CsF的价格很高,是此型钎剂的不足。CsF的相对分子质量很大,约为152,换算成质量分数时,钎剂中CsF占的比例看起来更大。于是人们的注意力转向AlF3-RbF系,这个体系的相图如图2-17[68]所示。体系中E2点的组成为x(RbF)=51.6%、x(AlF3)=48.4%,熔化温度为486℃,是个可选的钎剂组成。RbF的相对分子质量为104.5,换算成质量分数要比CsF系钎剂用量少许多,而两者的价格则不相上下。
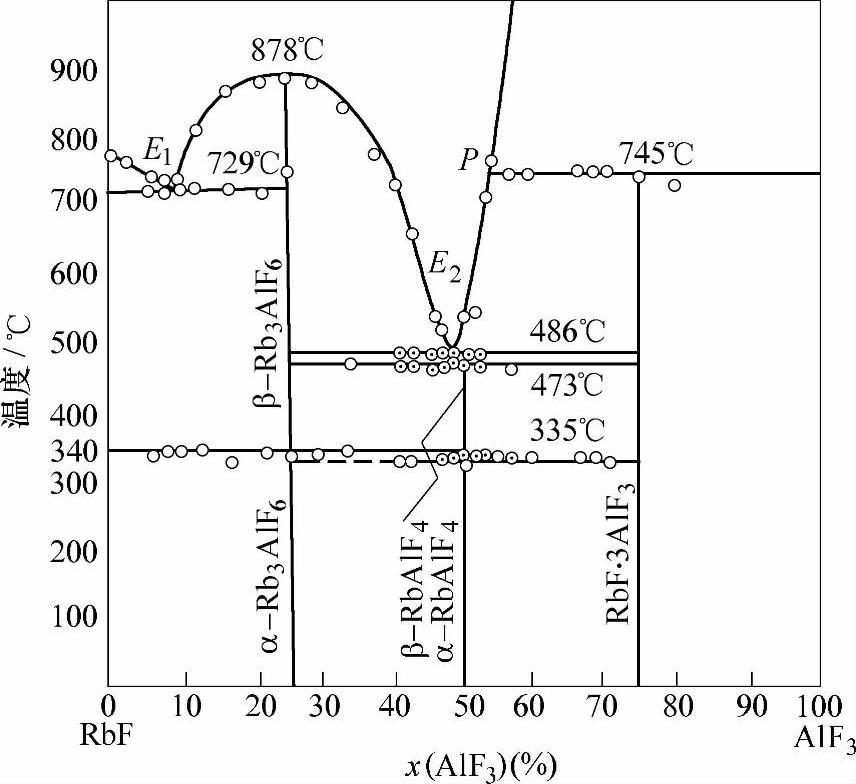
图2-17 RbF-AlF3系相图[68] Fig.2-17 Phase diagram of RbF-AlF3system[68]
合成CsF或RbF系钎剂可以采用它们的碳酸盐为原料,它比氢氧化铯稍稳定,虽然不像氢氧化铯那样会吸收CO2,但也严重吸水,因此称量前要在120~130℃彻底脱水。合成可按照Nocolok用K2CO3的方法进行,没有特别之处。Si杂质在AlF3-KF系钎剂中是一个“天赐的”活性剂,但Si杂质在CsF或RbF系钎剂中却会造成很大的麻烦。Nocolok AlF3-KF系钎剂的熔化温度较高(558℃),钎剂一熔化的瞬间,被铝母材还原出来的元素Si立即和母材合金化,在母材表面生成一层闪亮的熔态合金层,这一过程起了有效的活化作用。CsF或RbF系钎剂的熔化温度比较低,钎剂熔化以后还原出来的Si不能和母材立即合金化,而以微粒形式悬浮在钎剂之中,这就使得钎剂铺展的中心处发黑。国内商品化学纯的Cs2CO3或Rb2CO3在杂质含量的标签上都标识良好,但往往不标注硅的含量,其实硅的含量常大大超过0.1%(质量分数)。将Cs2CO3或Rb2CO3溶解在纯水中,如果浑浊不清,则说明Si含量太高。这是因为以Cs2SiO3形式存在的杂质水解为硅胶而悬浮,这种硅胶无法通过过滤而除掉,所以使用这种原料时,要在聚四氯乙烯容器中反复加过量的HF并加热以除去Si。因此,在选用原料时,要十分注意碳酸盐中的硅,还有铁的杂质含量。
关于CsF系钎剂的应用屡见诸文献,用它来钎焊2A12硬铝[69]以及铝锂合金。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




