目前,血栓、钙化和细菌感染是包括医用TPU 在内的用于血液接触材料所面临的主要并发症。当医用材料进入人体,人体组织及血液和材料的表面会产生反应,因此,与上述的通过调整TPU 材料的组成与结构(本体法)来改善生物相容性的方法相比,表面改性是一种更为直接有效地改善材料表面性能、提高生物相容性的方法。
1. 亲水改性
基于对表面抗血栓材料、人体血栓形成和抗血栓过程的认识,表面亲水性被认为是具有良好血液相容性的表面特征性质之一。亲水性表面明显比憎水性表面更具有抗蛋白质吸附的性能,此外还具有抗细菌黏附、提高表面润滑性和降低损伤等优点。材料抗非特异蛋白质吸附的能力越强,与血液相互作用越小,其血液相容性越好。在提高血液相容性改性中,聚乙二醇/聚氧乙烯(PEO)及其衍生物(结构式如图5-4 所示)是研究最为广泛的可作为热塑性聚氨酯弹性体表面改性的材料。PEG 良好的血液相容性可能来源于其较低的表面自由能、亲水性和高表面活性、空间的排斥力、独特的溶液性质和分子构象等因素。而PEO 与水有独特的相互作用,PEO 改性TPU 表面在溶液中能够很快地发生表面分子结构再定位,导致十八烷基链在空气界面富集,这可以提高表面润湿性,长链PEO 分子更易吸附水分子,因此,其抗蛋白吸附能力增加。Park 等在有机硅改性热塑性聚氨酯弹性体的表面接枝了单官能度的聚乙二醇大分子,由于PEG 分子的高流动性,接枝聚氨酯展现了更低的血小板黏附性。
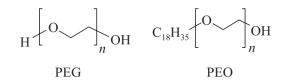
图5-4 聚乙二醇和聚氧乙烯的结构式
2. 等离子体改性
等离子体技术处理聚合物材料的表面可以使其表面富含活性基团,并使其表面的化学性质得以改善,利用等离子体法在热塑性聚氨酯弹性体表面接枝具有良好抗凝血性的物质是提高热塑性聚氨酯弹性体生物相容性的一种有效方法。Mota 等将等离子体聚合的聚乙二醇二甲醚沉积在聚氨酯表面,提高其亲水性。Aksoy 等用等离子处理TPU 的表面,在其表面上成功地化学固定了两种不同肝素,固定方式如图5-5 所示,血液细胞黏附实验证明接枝肝素后的聚氨酯能有效降低红细胞的黏附。Lim 等在聚氨酯薄膜上用氩气微波等离子体处理,图5-6结果显示处理后的聚氨酯膜的亲水性显著提高,表面粗糙度增加,处理后的TPU 膜对内皮细胞有良好的生物相容性。Sidouni 等利用等离子处理TPU 的表面,处理过程如图5-7所示,在TPU 的表面上产生氨基,然后在TPU 的表面上接枝具有生物活性的含RGD精氨酰-甘氨酰-天冬氨酸片段的合成肽,结果表明RGD 片段成功接枝在聚氨酯的表面,增强了内皮细胞的黏附。
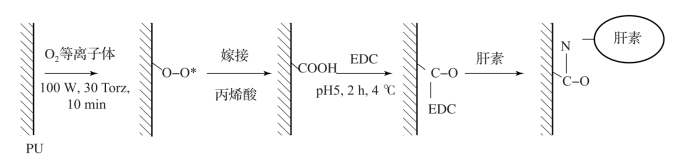
图5-5 两种不同肝素的固定方法

图5-6 TPU 膜的水接触角随处理时间的变化图
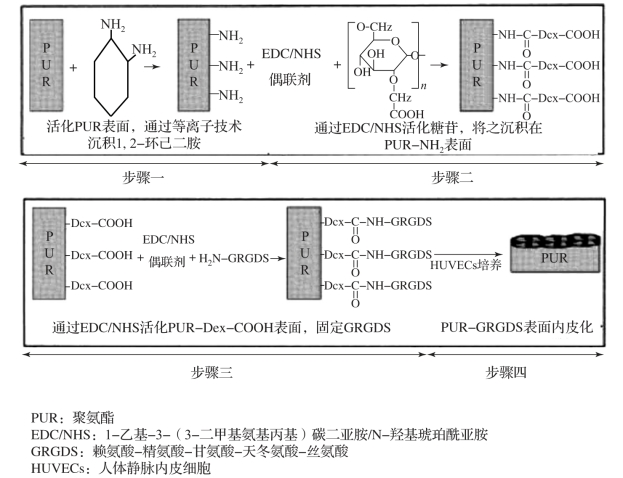
图5-7 热塑性聚氨酯弹性体表面改性流程
3. 生物活性大分子对TPU 的表面改性(https://www.xing528.com)
1)粘连蛋白
为了改善内皮细胞在TPU 材料表面的黏附和生长,人们设想使材料表面更生物化,更接近细胞生长的生理条件,在TPU 表面附加各种细胞黏附因子如胶原、纤维粘连蛋白、白蛋白等。Pierschbacher 等研究发现精氨酰-甘氨酰-天冬氨酸三肽是许多细胞膜和细胞外基质(ECM)中的粘连蛋白所共有的细胞间识别的最小序列,因此在材料表面固定RGD 三肽序列成为一种提高内皮细胞黏附和生长的中间途径。这种方法是先使TPU 表面活化,使其表面带有易与肽链的胺基和羧基反应的基团,然后通过生物分子的肽链与活性基团反应而使生物分子共价接枝到TPU 表面。如Sanchez 等使TPU 表面带上—NCO 活性基团,后将多肽GRGDS 接枝到TPU 表面;Anderheiden 等使TPU 表面带有—OH 活性基团,将多肽GRGDS接枝到TPU 表面,但此方法下,内皮细胞的生长状况并不理想。
2)肝素
肝素在生物体内能够抑制促凝血蛋白的吸附和活化,提高抗凝血蛋白的修复和血液活性,但是肝素在生物材料表面倾向于非均匀地分布,抗血栓活性不稳定,带负电荷特性的肝素链可以增加与蛋白的键合,导致形成血栓的概率增大。抗凝血酶-肝素共价复合物(ATH)能够克服肝素的缺点,具有非常高的抗血栓活性。Li 等将各种甲基丙烯酸酯和磷脂胆碱极性头基接枝到含乙烯基的TPU 上,发现血小板与改性过的聚合物黏附被抑制了90%左右。Klement 等研究了抗凝血酶-肝素共价复合物的TPU 表面改性,未改性的TPU 和通过肝素改性的导管表面均存在血栓症状,而ATH 改性的导管表面未有发现。在活体内106 天后的ATH 改性导管表面在扫描电镜下没有发现纤维蛋白质。因为ATH 涂层有极好的亲水性,其与血浆蛋白的结合减少,可快速酯解遏制血栓形成记忆抗Xa 活性的能力,同时增强抗凝血酶活性。
3)磷脂分子
细胞是生命功能的最小结构和功能单元,而一切细胞都以磷脂双分子层为其膜结构骨架,那么材料表面的磷脂化就可以避开体内免疫识别系统的攻击,从而提供生物相容性。磷酸胆碱是磷脂的一种具有双亲水性结构,对水分子的作用力扰动小,并与之结合成水合层,同时磷脂分子具有柔性尾部,对蛋白的吸附作用基本上为可逆吸附,即蛋白可保持其天然构象。Iwasaki 等通过电晕辐照法将聚ω-甲基丙烯酰氧基烷基磷酰胆碱(MAPC)(单体结构如图5-8)逐步接枝到TPU 表面,非特异性地减少了蛋白质的吸附和细胞黏附,改善了聚合物表面的生物相容性。Heiden 等将带有磷酸胆碱基团的芳香叠氮化合物通过紫外光照射接枝到聚醚型TPU 表面,减少了血小板黏附、活化和血栓的形成,从而提高了TPU 的血液相容性。Lin 等用甘油磷酰胆碱作为扩链剂合成了TPU,有效降低了嗜中性粒细胞的黏附,进而削弱了炎症反应和异物反应。Yung 将磷脂分子引入TPU 分子链,操作方法简单,并且可以克服表面涂覆易脱落的缺点,在一定程度上提高了TPU 植入人体内的长期的生物相容性。
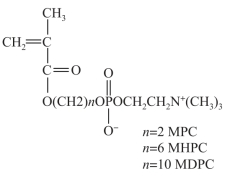
图5-8 MDPC 的单体结构
4. TPU 表面的负离子化
在聚醚型TPU 分子中引入负电性的羧酸基团或磺酸基团,通过负电荷之间的静电排斥作用也可以减少血小板在材料表面的黏附。而血液中的血红蛋白、血小板和部分血浆蛋白在血液环境中呈现负电性,同时,血管内壁也呈现负电性。因而,从模拟人体功能的方向出发,研究人员也考虑将TPU 材料进行表面负电性化的改性,这可以通过给材料表面引入阴离子来解决,同时,考虑到生物活性物质肝素良好的抗凝血性能,肝素结构中又含有羧基和磺酸基团。因而,很多文献都报道了表面羧基化或带有磺酸根离子的TPU。Chen 等采用在扩链剂上引入离子的方法在脂肪族TPU 表面引入了羧酸根离子和磺酸根离子,并且血小板黏附实验表明,羧酸根离子表面显示了更好的血栓形成阻力。Okkema 等研究则认为在相同的离子含量与非常短的血液接触时间时,磺酸根离子的引入很大程度上降低了血小板的沉积,但羧酸根离子对血小板黏附则没有太大的影响。许利娜等在TPU 的表面构建了磺胺两性离子结构,认为磺胺两性离子结构在热力学上不可能进入蛋白质等生物大分子天然构象的内部,与蛋白质表面上离子结构的作用力小,有利于维持其天然构象,能改善血小板黏附性。
5. 表面协同改性
当上述一种改性方法不能达到使用要求时,还可以考虑协同效应的作用。Han 等利用末端接上磺酸根负离子的PEO 在TPU 表面进行接枝改性,并提出了一种所谓“纤毛模型”(图5-9)。如前所述,PEO 分子具有极度的亲水性,与血液具有极低的自由能、独特的溶液特性,能形成水合柔韧的PEO 链,通过分子链的运动限制和阻止血浆蛋白和血小板的停滞和黏附。同时,分子链上的负电荷又能起到静电排斥作用,展示了较好的抗凝血性能,很好地体现了PEO 的运动性和负电荷磺化基团排斥的协同作用。
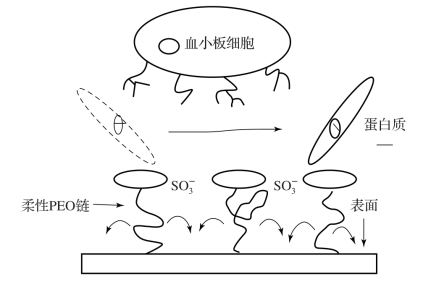
图5-9 纤毛模型
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




