曳光技术应用已近一个世纪。随着炮弹射程的提高、目标的快速移动及远程监测仪的发展,研究曳光剂反应机理对曳光装置或曳光管的设计具有现实意义。哈德特(Hardt A.P.)和帕卡尔斯基(Puchalski W.J.)为此做出了贡献。
7.3.3.1 哈德特(Hardt)模型
哈德特研究工作是以燃烧速度、持续时间和能见度为曳光剂的特征量。他测定了Sr(NO3)2与PVC分解动力学数据,以及不同可燃物与氧化剂配制成的曳光药柱的热导率,并对曳光药柱热传递的过程做了数值分析,获得了静态和旋转条件下的热通量。该模型只是假设金属粉氧化发生于气相阶段,燃烧速度仅是不同配比的热导率的函数,黏结剂的作用忽略不计,因此只适用于由金属可燃剂与氧化剂配制的药剂(如照明剂、信号剂)。
(1)燃烧过程的基本现象。曳光剂热分解速率方程如下:
![]()
式中,v——燃速,cm/s;
B——常数;
E——活化能;
R——气体常数;
Ts——燃烧面温度。
设氧化剂和可燃剂表面反应速度近似相等,则单位时间内物料消耗:
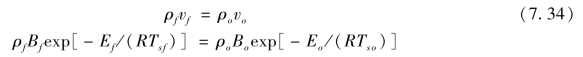
式中,ρ——密度;
下标f和o——分别表示可燃物和氧化剂。
通常,可燃物和氧化剂的B、E不等,而Tsf和Tso也有差异,故vf≠vo。热分解速率不同,某些成分会很快气化反应,而另一些成分则残留在燃烧面处进行反应。在燃烧面处的组分容易被燃烧块组分的热气流带出燃烧面而进一步进行燃烧反应。经高速摄影,的确发现曳光剂中大部分镁粉粒子被“驱逐”出燃烧面。高速摄影还发现,只有部分镁粒子同氧化剂起反应,在这部分镁粒子周围形成了氧化层。该氧化层是孔状结构,它迅速地向镁粒子中心扩散,最终使镁粒子形成一个“空泡”(an empty bubble)状反应产物。镁的反应速度取决于氧化层的扩散速度。
(2)模型分析。
基于Sr(NO3)2/Mg/PVC常规曳光剂反应历程,理论分析认为是一个固相的和气相的过程。
1)固相过程的热传递如图7.9所示。
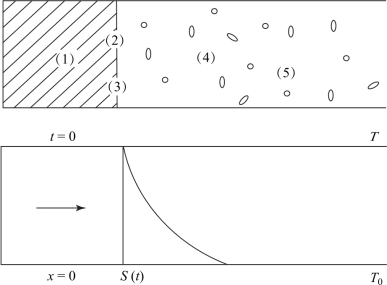
图7.9 固相过程热传递示意图
图中(1)区为PVC分解区;(2)区为Sr(NO3)2分解区;(3)区为Mg熔化区;(4)区为Mg升华区;(5)区为Mg蒸气燃烧区。t时刻的燃烧面位置为S(t);按燃烧理论,燃烧将以ds/dt速度传播。热传递过程是流进燃烧面的热流量H使Sr(NO3)2吸热分解。
热传导方程为:
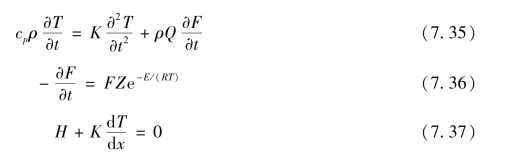
式中,Q——Sr(NO3)2的分解热;
Z——动力学参数;
F——未分解药剂的百分比;
H——热流量;
K——导热系数;
ρ——密度;
cp——定压比容。
当x=S(t)时,边界条件:
![]()
动力学参数Z和E由试验测定。未分解药剂的百分比F在给定的时刻是一个常数。燃烧面的温度分布由热流量H和材料热导率求出。哈德特编制了计算机程序,进行了数值计算。结果表明,可燃物过量的配方具有较高的气化速率。他认为原因是:其一,金属粉含量越高,热传导越快;其二,由于分解吸热量与氧化剂量成正比,可燃物增加氧化剂量则减少,这样氧化剂分解吸热量减少,则气化速率就高。理论分析结果与试验测定的气化速率一致。
2)气相过程曳光剂的反应机制主要表现在气相反应中镁“液滴”的破裂,在常压条件下镁蒸气的热分解速度为:

式中,dm/dt——气化速率,mol/s;
r——时刻![]() 时的可燃剂的球半径;(https://www.xing528.com)
时的可燃剂的球半径;(https://www.xing528.com)
Ts——可燃剂微元表面温度(1 363 K);p
s——微元表面的初始压力(1.01 MPa);
p0——液态下镁的初始压力(0.12 MPa);
D——扩散系数;
R——气体常数,R=358 cm2/s;
m——Mg的气化摩尔数;
M——Mg的摩尔质量。
积分式(7.38)得
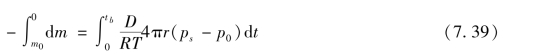
得到镁“液滴”寿命tb为:
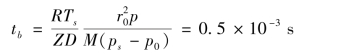
在时刻dt时,固体表面放出的气体厚度为:
![]()
式中,Ta——镁的沸点(1 373 K)与火焰温度(3 000 K)的平均值,约为2 000 K;
mg——每克固体分解的气体摩尔数(1.66×10-2);
yn——NO与氧原子的摩尔分数;
ρg——气体混合物密度;
v——退化速度。
将由式(7.38)得到的m代入式(7.40),积分即得燃烧区厚度:

式中,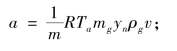
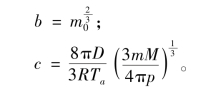
7.3.3.2 帕卡尔斯基(Puchalski)模型
帕卡尔斯基模型是把整个燃烧过程分成凝聚段(固-固或固-液混合段)和燃烧段(气相反应与发光段)两段。在凝聚段,反应是吸热的或放很少量的热。影响反应的两个主要因素有两个:一是外部条件(压药压力、装药直径和转速等);二是配比(各成分的百分比及其热力学特性等)。在燃烧段激烈放热时,反应几乎不受外部条件影响,因而可以认为凝聚段决定着燃速,燃烧段支配着热释放。燃烧模型如图7.10所示。
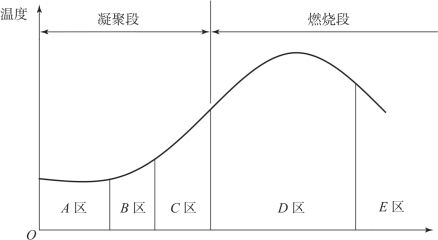
图7.10 燃烧反应温度分布图
其中,A区:没有进行反应,外界条件无影响。
B区:预热区,发生明显的热传递,组分温度升高。
C区:凝聚段反应,在此区氧化剂熔化并放热分解,所放热大部分供给发光段。在C区内,组分以液态存在,而不再是固态。相对A、B两区而言,C区是不稳定的。
D区:温度最高,由于空气中的氧与氮参加反应,使得已放热的反应区的热量进一步增加。
E区:反应产物区。反应基本结束,因而温度降低。
在旋转的条件下,上述A~E区发生的变化有如下情况:
(1)虽然温度梯度有所变化,但A、B区不变化。
(2)D区和E区两燃烧反应区宽度比凝聚段要窄。
(3)凝聚段C区的药粒迅速向外移动,接近管壁处密度增大,径向热传递增加,形成凸形燃烧面。
帕卡尔斯基认为,静止条件下,曳光药的燃烧面是一平面或略带点低凹的凹面;而在旋转的条件下,燃烧面则是凸面。也就是说,静态是平面燃烧,旋转条件下是凸面燃烧。这一结论已被拍摄的燃烧阵面照片证实。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




