烟火药燃烧温度是评定烟火药性能的重要依据。获得烟火药燃烧温度的方法有计算法和试验测量法两种。这里介绍烟火药燃烧温度的理论计算法。
烟火药燃烧反应的最高温度,可按下式进行计算:
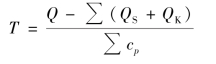
式中,Q——燃烧反应放出的热量,kJ;
T——燃烧温度,℃;
Σ(QS+QK)——燃烧生成物的熔化热和汽化热的总和;
Σcp——燃烧生成物的总比热容。
有些化合物的熔化热和汽化热目前尚未获得精确值,再加上许多化合物在高温下缺少正确的比热容数据,所以计算法受到限制。同时,由于热传导、热对流、热辐射的影响,以及燃烧生成物的热解离,计算结果往往比实际测定结果要大得多。下面简要介绍计算中涉及的相关参量。
(1)生成物热容计算。烟火药多在空气中燃烧,取定压下热容数据较合理。气体分子摩尔定压比热容与摩尔定容比热容关系为:
![]()
对于单原子气体来说,cV,m=3R/2,cp,m=5R/2;双原子气体,cV,m=5R/2,cp,m=7R/2;多原子气体,cV,m=3R,cp,m=4R。
对于由B,C,…形成的理想气体混合物,其摩尔热容可按下式计算:
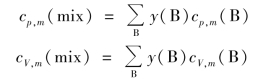
即理想气体混合物的摩尔比热容等于各气体摩尔比热容与其摩尔分数的乘积之和。实际上气体cp理论值与试验值也有差别,计算时可参照表5.3。
表5.3 气体cp的试验值J·(mol·℃)-1

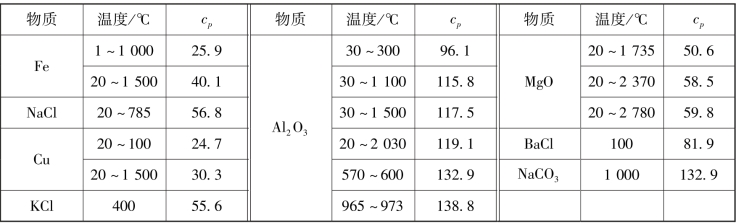
对1 000℃以上的单质固体,按杜明-普蒂定律,可粗略地认为cp=26.8 J/(mol·℃)。对于高温下固体化合物来说,按尼曼-高伯定理,复杂固体化合物的比热容等于组成该化合物各元素原子比热容的总和。至于1 000℃以上液体的比热容,要指出一定的规律性较困难,当没有液体比热容的数据时,可以按该物质在固态时的比热容计算,这样做会不可避免地引入一些误差。应注意,物体的液体比热容大于其固态比热容。固体cp的试验值见表5.4。
表5.4 固体cp的试验值J·(mol·℃)-1
(2)熔化热和汽化热。大多数单质熔化热和熔化温度有下列关系:
![]()
式中,QS——熔化热,kJ/mol;
TS——熔化温度,K。
对于许多无机化合物熔化热,可近似按下列经验公式计算:
![]()
式中,n——化合物分子中的原子数。(https://www.xing528.com)
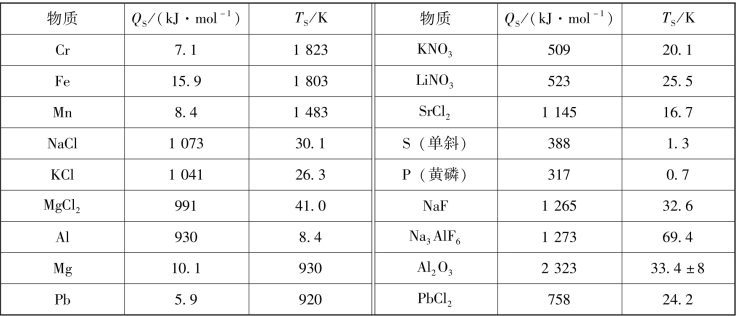
某些物质的QS和TS试验值见表5.5。
表5.5 某些物质的QS和TS试验值
同一物质的汽化热,通常随着汽化温度的升高而降低。在常压下液体沸点TK(K)时的分子汽化热QK可由特鲁顿公式估算:
![]()
某些物质的QK和TK试验值见表5.6。
表5.6 某些物质的QK和TK试验值

许多无机化合物(尤其是沸点高的)的汽化热可以按下列经验式计算:
![]()
(3)计算实例。
例5.2 计算含75% Fe2O3及25% Al的高热剂的燃烧反应温度。
解:①写出燃烧反应方程式:
![]()
②计算Q:
![]()
③查表得,Al2O3的熔点为2 050℃,沸点为2 980℃;Fe的熔点为1 535℃,沸点为2 740℃。
④求Σ(QS+QK),查表得:TS=1 535℃(1 808 K)时,QS(Fe)=15.9 kJ;T=2 050℃(2 323 K)时,QS(Al2O3)=33.44 kJ;TK=2 740℃(3 013 K)时,QK(Fe)=0.08×3 013=241.0 kJ;TK=2 980℃(3 253 K)时,QK(Al2O3)=484.9 kJ。
![]()
显然,QK=484.9+241.0×2=966.91(kJ),汽化总热超过了反应热Q=857 kJ,因此,最高沸点物质Al2O3是不可能汽化的,故计算时应除去QK(Al2O3),故⑤求Σcp:Fe在20~1 500℃时,cp=40.1J/(mol·℃),温度升高,cp将上升,在20℃~t范围内,近似选用cp(Fe)=46 J/(mol·℃),同理,cp(Al2O3)=129.6 J/(mol·℃)。
![]()
则得:

必须看到,在计算时,铁的汽化热已经考虑进去,而所得温度反而低于铁的沸点,有矛盾。如果将QK(Fe)去掉,则有:
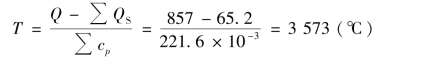
但是,经过这一处理又有矛盾,所得数值比Al2O3、Fe的沸点都高,而计算中又把它们的QK去掉了。不过,由上述两项计算可以得出这样结论:该药剂燃烧温度比Al2O3的熔点(2 050℃)高,比Fe的沸点(2 740℃)低,故该高热剂的燃烧温度是在2 050~2 740℃。该例表明,烟火药的燃烧温度的计算结果不太准确,只能粗略估计一个大致温度范围。至于较为精确的结果,需要通过试验来测定。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




