氧化剂和可燃剂是组成烟火药的最基本成分,烟火药燃烧过程中还可借助空气中的氧气作为可燃剂,但常常燃烧速度过慢,达不到预期的烟火效应。因此,烟火药配方中一般都含有氧化剂。氧化剂可以是含氧氧化剂,也可以是无氧氧化剂。一般电负性大的元素都可作为氧化剂,如烟幕剂中的CCl4就是无氧氧化剂:
![]()
烟火药中氧化剂的选择除满足对烟火药成分的一般要求外,还应符合以下原则:
(1)氧化剂应为固体,其熔点不低于60℃,并在±60℃范围内保持稳定;
(2)应含大量的有效氧(>30%),且燃烧时易释放;
(3)吸湿性小,受水作用不分解;
(4)制成的烟火药机械感度和摩擦感度低,安全可靠。
烟火药中所用氧化剂通常要求其是富氧的离子型固体,在中等温度下即可分解放出氧气。富氧的离子型固体氧化剂的阴离子应含有高能键,如Cl—O或N—O等,通常是下列各种阴离子:硝酸根离子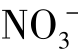 、氯酸根离子
、氯酸根离子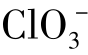 、高氯酸根离子
、高氯酸根离子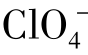 、铬酸根离子
、铬酸根离子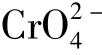 、氧离子O2-、重铬酸根离子
、氧离子O2-、重铬酸根离子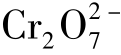 。
。
需要指出的是,与上述阴离子构成离子型固体氧化剂的阳离子,必须对所产生的烟火效应起积极作用而不产生消极影响。例如,Na+阳离子与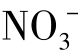 阴离子构成的NaNO3氧化剂,其Na+阳离子是黄光发射体,在黄光剂中起积极作用,但NaNO3氧化剂不宜用于制造红光剂、绿光剂、蓝光剂,因为Na+阳离子在红光剂、绿光剂、蓝光剂中起消极作用,它的存在会干扰红色、绿色和蓝色火焰比色纯度(色饱和度)。Li+、Na+、K+碱金属阳离子和Ca2+、Sr2+、Ba2+碱土金属阳离子都是不良的电子受体,它们也不与Mg、Al等活性金属可燃剂在常温贮存下发生反应,因此由它们与阴离子结合的盐类氧化剂在烟火药中应用相对广泛。由Pb2+、Cu2+这类阳离子与阴离子结合的盐类氧化剂,例如Cu(NO3)2,易氧化Mg等活性金属可燃剂,可以发生如下反应:
阴离子构成的NaNO3氧化剂,其Na+阳离子是黄光发射体,在黄光剂中起积极作用,但NaNO3氧化剂不宜用于制造红光剂、绿光剂、蓝光剂,因为Na+阳离子在红光剂、绿光剂、蓝光剂中起消极作用,它的存在会干扰红色、绿色和蓝色火焰比色纯度(色饱和度)。Li+、Na+、K+碱金属阳离子和Ca2+、Sr2+、Ba2+碱土金属阳离子都是不良的电子受体,它们也不与Mg、Al等活性金属可燃剂在常温贮存下发生反应,因此由它们与阴离子结合的盐类氧化剂在烟火药中应用相对广泛。由Pb2+、Cu2+这类阳离子与阴离子结合的盐类氧化剂,例如Cu(NO3)2,易氧化Mg等活性金属可燃剂,可以发生如下反应:
![]()
因此,由Pb2+、Cu2+这类阳离子与阴离子结合的盐类氧化剂很少用于烟火制造。
除富氧的离子型固体被选作氧化剂外,含有卤素原子如F和Cl的共价键分子也可以用作烟火药的氧化剂,例如六氯乙烷(C2Cl6)和聚四氟乙烯,它们分别与Zn和Mg的烟火反应如下:
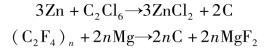
综上所述,烟火药中氧化剂应满足下列技术要求:
(1)纯度应不低于98%~99%;
(2)水分含量应极小,通常不大于0.5%;
(3)容易吸湿的盐和重金属盐的含量应极小;
(4)不含有增强药剂机械敏感度或降低药剂化学安定性和影响烟火效应的杂质;
(5)氧化剂的水溶液应为中性;
(6)氧化剂粉末应具有适当的颗粒度。
但是,在烟火药氧化剂选择中最不希望的是含有氯化物一类的杂质,因为它们可使氧化剂变得易吸湿。例如在氯酸钾氧化剂中加入0.05%和0.1%的氯化钾后,氯酸钾的吸湿性明显增加,见表2.1。氯化物杂质中氯化钾的吸湿点较高,见表2.2。
表2.1 氯化物对盐类氯化剂吸湿性的影响
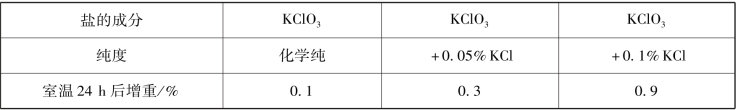
表2.2 几种氯化物杂质的吸湿点

烟火药中常用氧化剂的物理化学性质见表2.3,其理化性质主要包括以下几个方面:
(1)氧化剂的熔点。氧化剂的熔点和它的分解温度密切相关,在大多数情况下,氧化剂只能在其熔点或稍高于其熔点的温度下才进行剧烈的分解。通常知道其熔点的高低,即可大致判定该类烟火药点燃的难易程度及燃烧反应速度的快慢。
在选用氧化剂时,其熔点或其分解温度必须适应烟火药的燃烧温度。例如有些发烟剂一般是在不高的燃烧温度下借助有机染料的升华而产生有色烟云,所以这类烟火药不能选用熔点太高的氧化剂。
表2.3 烟火药常用氧化剂的物理化学性质
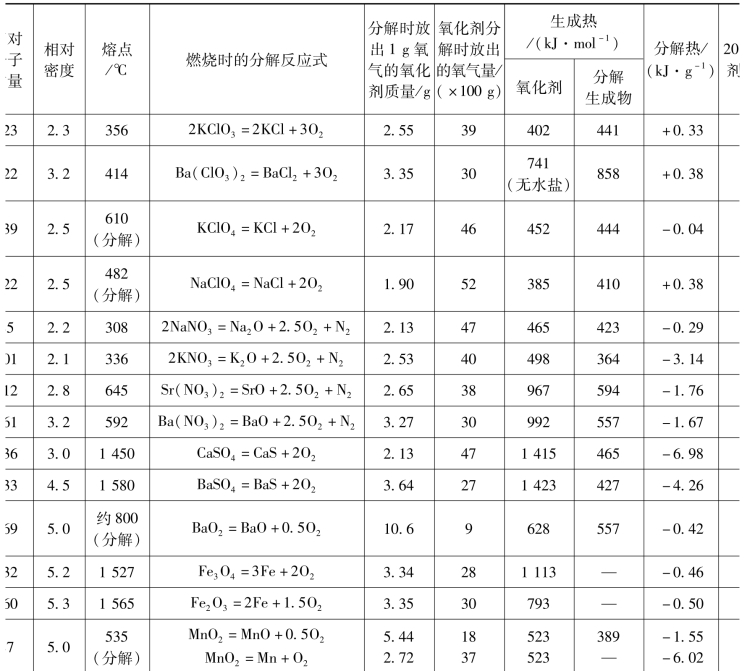
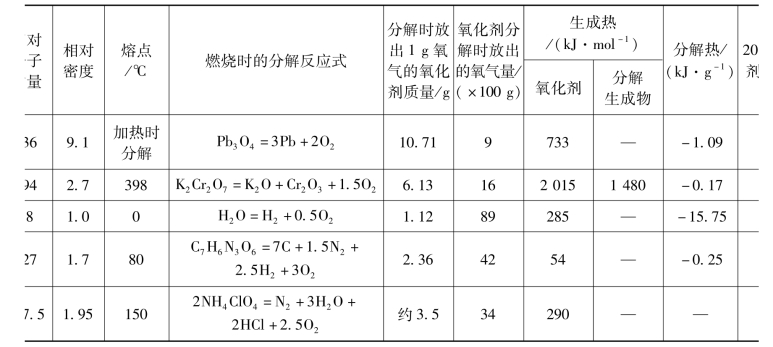
(2)氧化剂的分解反应。氧化剂受热时的分解反应式不同于烟火药燃烧时其中的氧化剂分解反应式。这两种反应式必须严格区分开来。当烟火药燃烧时,氧化剂最可能发生的分解反应见表2.3中第5列燃烧时的分解反应式。(https://www.xing528.com)
氯酸盐和高氯酸盐在烟火药燃烧过程中分解为氯化物和氧气。
硝酸盐随可燃剂性质不同,其分解反应生成物也各异。当可燃物为C、S、P或其他有机物时,硝酸盐可彻底分解成金属氧化物:
![]()
当可燃剂为乳糖,燃烧温度不高的情况下,生成物中将含有大量的亚硝酸盐。当可燃剂为强还原剂,如Mg或Al时,硝酸盐能产生较完全的分解:
![]()
硫酸盐类与Mg、Al燃烧,如不与空气接触,则生成硫化物,且放热量很大。
![]()
氧化物和过氧化物在烟火药燃烧时,发生还原反应,生成游离金属:
![]()
在烟火药燃烧时,氧化剂究竟生成何种化合物,可按化学反应最大放热法则或最小自由能法则来判断,即放热量大的比放热量小的反应更为可能。如:
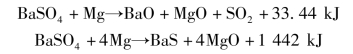
依据最大放热原则,判断BaSO4和Mg的反应生成产物是BaS,而不是BaO。
(3)氧化剂的氧量。在选择氧化剂时,要考虑氧化剂中直接用于氧化可燃剂的氧量,通常称之为有效氧量。如K2Cr2O7的总含氧量为38%,但它的有效氧量只有16%。有效氧量是以氧化剂所分解出的氧量占总质量的质量分数表示,它是评定氧化剂氧化能力的重要因素之一。显然,配制烟火药时应选取含有效氧量多的氧化剂。
(4)氧化剂的分解热。在合理选择氧化剂时,还必须考虑氧化剂的分解热。氧化剂放出氧的难易程度和它在分解时放热或吸热多少有关。氧化剂分解时所需热量越少,则释放氧越容易。氧化剂中除氯酸盐分解是放热过程外,其他氧化剂分解基本都是吸热过程。在烟火药燃烧过程中,一般氯酸盐放出氧较高氯酸盐和硝酸盐容易,而硝酸盐又较硫酸盐和氧化物容易,见表2.3中的数据。选用分解热小的氧化剂,有利于烟火药的快速燃烧并放出最大的热量。但其机械感度也相应提高,例如用KClO3配制的烟火药极易发生爆炸,原因是其分解时将放出大量的热。KClO3的分解反应如下:
![]()
(5)氧化剂分解产物的熔点和沸点。烟火药的燃烧产物、燃烧状态都对其烟火效应有所影响。根据氧化剂分解生成物的熔点和沸点的数据,可以预先估计有无气体生成,有无液、固相生成物,以及在燃烧过程中发烟的程度等。
(6)氧化剂的吸湿性。氧化剂的吸湿性将直接影响烟火药的物理、化学安定性。选用比金属可燃剂电动势高的、吸湿性小的盐类作烟火药的氧化剂较为有利。有许多盐类具有较大的吸湿性,如果影响到烟火药的安定性,则不能选用。
盐类吸湿的程度取决于空气的湿度和温度、盐本身的性质及盐和潮湿空气接触面的大小。盐类的吸湿过程首先由水蒸气的吸附作用开始,即当溶于水的盐类吸附了若干水分后,在晶体表面形成一薄层的饱和溶液。若在某一温度下,大气中的水蒸气压超过饱和溶液上的水蒸气压时,该盐类吸收水分;反之,则由于释放出水分而被干燥。
盐类既不吸湿又不干燥的相对湿度谓之“吸湿点”,用下式表示:
![]()
或用相对湿度来表示:

式中,pa——盐类饱和溶液上的水蒸气压,Pa;
p——在同温度下使空气饱和的水蒸气压,Pa;
h——吸湿点;
A——相对湿度。
根据吸湿点的大小,可将氧化剂分为三类。
A类:Ba(NO3)2、KClO4、KMnO4、KClO3;
B类:Ba(ClO3)2、Pb(NO3)2、KNO3;
C类:Mn(NO3)2、Ca(NO3)2、Mg(NO3)2、Sr(ClO3)2、Ba(ClO3)2、Al(NO3)3、NaNO3。
军品中都将采取一定的措施在将其做成制品并烘干后很快密封,但一些民用的火工品,工艺要求不是很高。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




