【摘要】:甲烷重整的两个吸热反应是CH4+H2OCO+3H2和CH4+CO22CO+2H2TCR的图解如图9-13所示。经过加热它们的温度上升。假定当温度T3=T4=TAR、m=0001时,反应开始。在第一个反应中,TAR=415K,然而在第二个反应中TAR=515K。加热量为QH1=H2-H1=H7-H9,QH2=H4-H2=H8-H10在R点的反应吸收热量为Qin=H6-H7-H8=QR+图9-13 热化学反应图解
甲烷重整的两个吸热反应是
CH4+H2O⇒CO+3H2(9-37)和
CH4+CO2⇒2CO+2H2(9-38)TCR的图解如图9-13所示。图中,1、2、3和4是入口反应流,5是反应产物流,6、7、8、9和10是活塞发动机的废气流,放出它的显热来驱动吸热反应的进行。
大气压下的平衡常数K仅仅决定于温度并且和标准吉布斯自由能ΔG0T的变化相关:

对于第一步反应,式(9-37)为
ΔG0T=188748+22875·Ti-6961·Ti·lnTi+80711·10-3·(T2i)/2-22874·10-6·(T3i)/6(9-40)
对于第二步反应,式(9-38)为
ΔG0T=230323+1937·Ti-7175·Ti·lnTi+10681·10-3·(T3i)/2-3606·10-6·(T3i)/6(9-41)
直到这两个反应平衡时甲烷重整率为
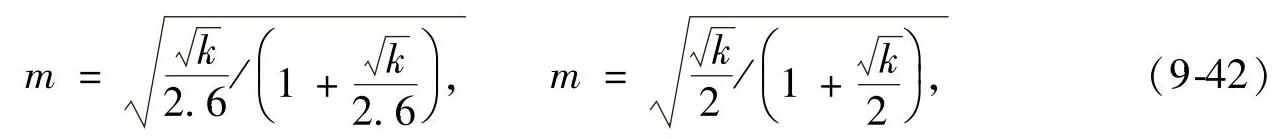
两个反应的反应物的摩尔分数分别是(https://www.xing528.com)
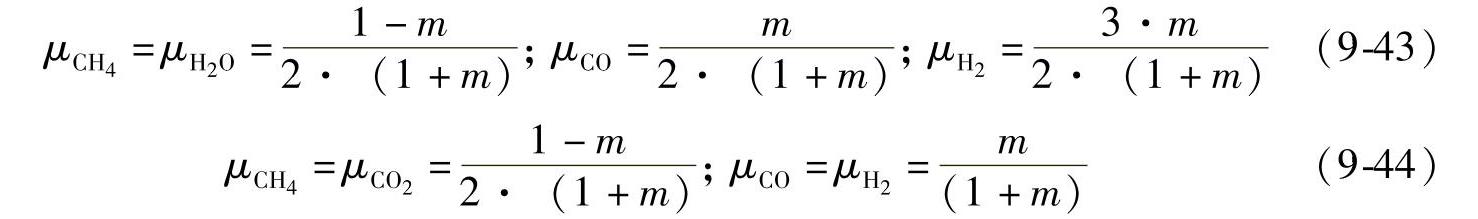
最终反应物量与入口反应物量的比值(化学分子变更系数)是
β=1+m(9-45)
入口反应物的温度是环境温度T1=T2=T0。经过加热它们的温度上升。假定当温度T3=T4=TAR、m=0001时,反应开始。在第一个反应中,TAR=415K,然而在第二个反应中TAR=515K。
加热量为
QH1=H2-H1=H7-H9,QH2=H4-H2=H8-H10
在R点的反应吸收热量为
Qin=H6-H7-H8=QR+(H5-H3-H4)
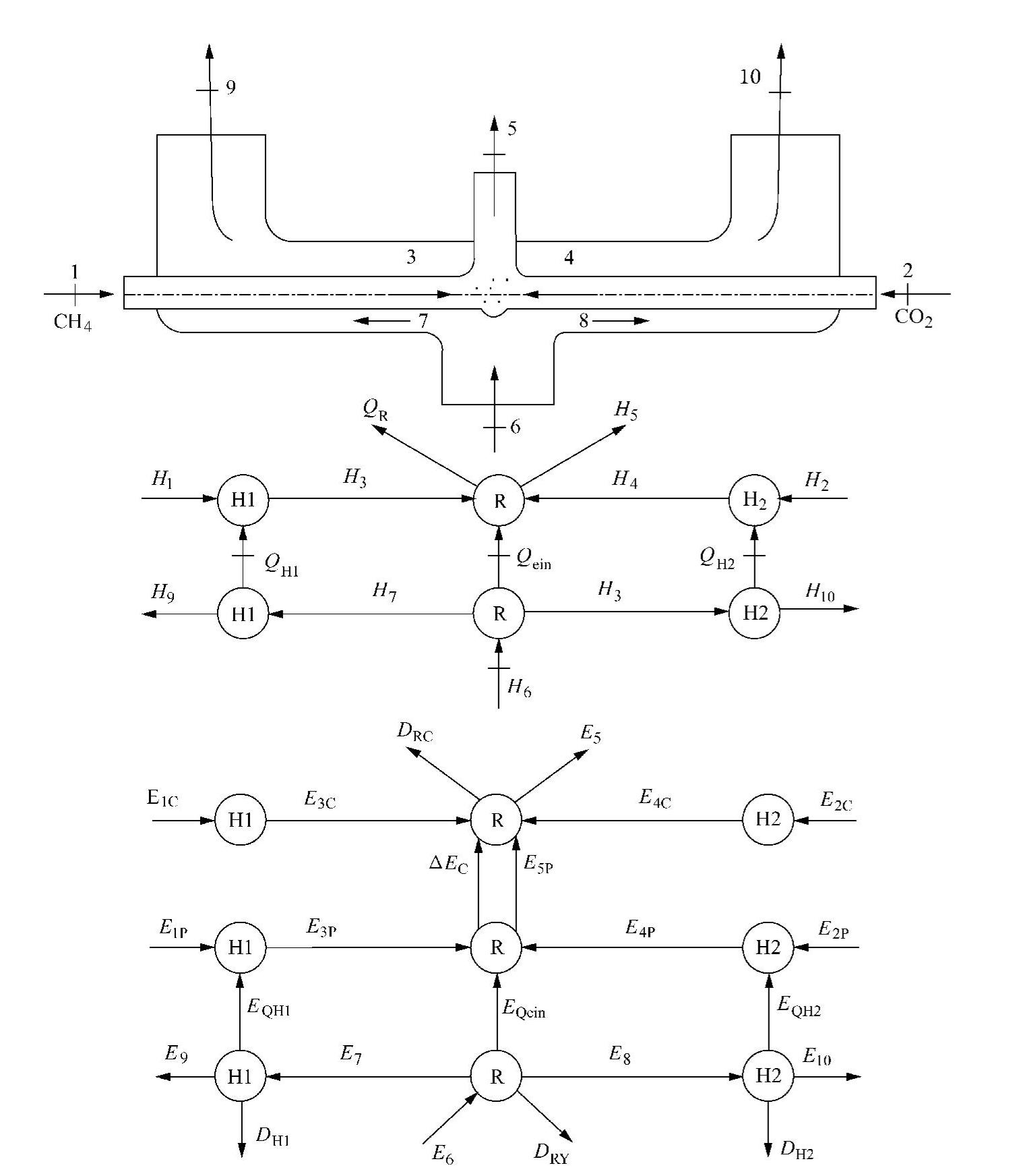
图9-13 热化学反应(TCR)图解
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




