H2SO4溶液不仅是铅酸蓄电池的电解质,它还参与电极反应和电池反应,也是活性物质,这从电池反应方程看得很清楚。
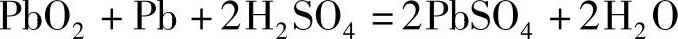
H2O也是活性物质,它定量地参与充电和放电反应。上面的反应方程清楚地表明了这一点。按照法拉第电解定律,在铅酸蓄电池成流反应(current generating reaction)中放出1A·h的电量理论上需要H2SO43.6594g。从充电的电极反应能够更清楚地看到,充入1A·h的电量理论上需要H2O 0.67217g。
正极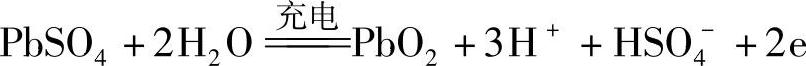
负极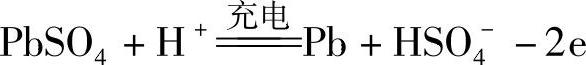 由于配制的电解质溶液中总是有大量的H2O,一般说H2O都是过量的,人们更多地注意H2SO4的量。利用率不同时,完全充电的铅酸蓄电池需要的H2SO4溶液量列在表9-1中。
由于配制的电解质溶液中总是有大量的H2O,一般说H2O都是过量的,人们更多地注意H2SO4的量。利用率不同时,完全充电的铅酸蓄电池需要的H2SO4溶液量列在表9-1中。
表9-1 铅酸蓄电池放电1A·h实际需要的H2SO4溶液量
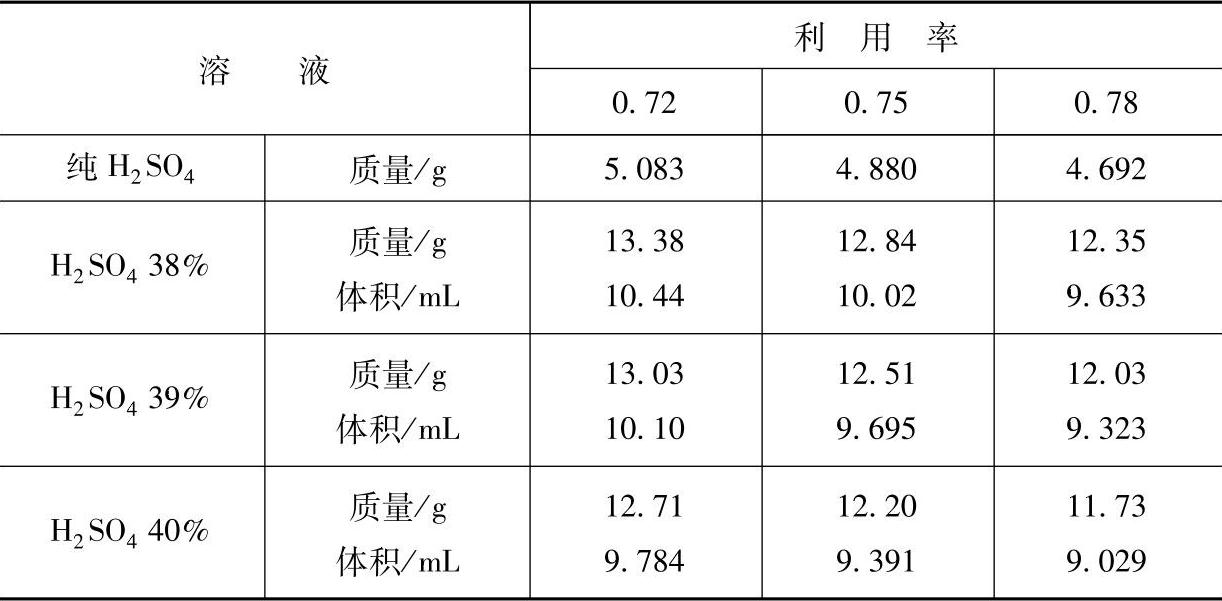
注:表中体积的毫升数指25℃时的值,是蓄电池完全充电时的H2 SO4溶液的体积。
还应当考虑到VRLA在使用过程中不断失水,电解液密度不断增大,注液量还应更多些,应适当选择密度较低的H2SO4溶液。
如果选用已定型的商品蓄电池槽,极群组的设计确定之后,注液量就是一定的。单体蓄电池槽内腔的长、宽、深的乘积用Vo表示。这里的深不是蓄电池槽的总深度,而是略大于极板高度的一个值,Vo减去单体蓄电池中深度以下所有固相物的体积就应当是注液量。固相物包括:
● 所有板栅的体积VG;
● 正极活性物质的体积V+;(https://www.xing528.com)
● 负极活性物质的体积V-;
● 隔板的体积Vs。当然这里的体积指的都是固相物的体积,不是含有孔隙的表观体积。这些值都可以从产品设计的参数计算出来。注液量Ve可以表示为
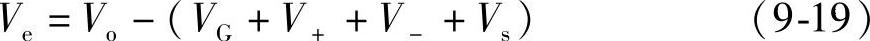
这里指的是完全充电的VRLA的H2SO4溶液的量。
如果采用蓄电池内化成的工艺,还应当考虑生极板中的PbSO4在化成后生成H2SO4引起的浓度增高,注液的H2SO4溶液浓度就应低些。化成生成的H2SO4的量近似等于和膏时加入的H2SO4的量。正铅膏酸量为A+′,铅粉质量为P+(kg),化成后正极板生成的H2SO4的质量近似等于P+A+′;同样,负铅膏酸量为A′-,铅粉质量为P-(kg),化成后负极板生成的H2SO4的质量近似等于P-A′-。蓄电池内化成时注液的密度为ρ,体积为Ve,这一密度的H2SO4溶液的质量百分浓度为ω。那么,注液加入的H2SO4的质量就是ρVeωo,用下式能近似计算出蓄电池完全充电时电解液的质量百分浓度ω
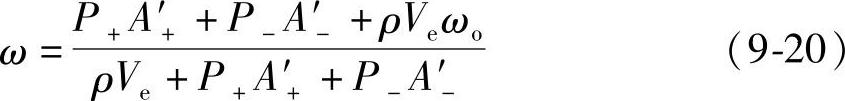
反之,如果要求完全充电的蓄电池的电解液浓度是一定的,也应当能计算出应当注入的电解液的浓度ωo。式(9-20)中的两个变量ωo和ρ不是互相独立的,ρ依赖于ωo,一定温度下ρ只依赖于ωo,即两者实际上是一个变量。但两者的关系还难以用一个严谨的数学解析式来表示,所以由ω求ωo的计算稍为繁琐。
电池内化成的过程一般说时间较长,往往是90~120h甚至更长。过程中由于气体逸出和蒸发,水的损失是不可避免的;温度较高时,损失的水量也更多。化成过程中补充注入纯水的量应根据实验确定。
参考文献【8】给出一个公式,完全充电的蓄电池1A·h电量的最低用酸量用体积V表示
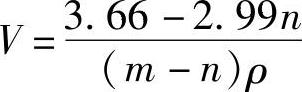
式中,m和n分别是蓄电池开始放电时和放电终止后的电解液的质量百分浓度,ρ是开始放电时的电解液的密度,g·mL-1,V以mL为单位。例如,m=39%,n=7%,ρ=1.29,则V=8.36mL。这是最低用酸量,实际上注液量多大于这一公式的计算值。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




