铅酸蓄电池的电极结构较之基础理论研究中的平面电极、圆盘电极等要复杂的多。这是一种多孔结构的电极。为了描述和确定其电化学特性,应当确定的物理和化学的参数有孔率、表面积、孔径分布、电解液的电导率与黏度对于浓度的依赖关系、硫酸铅的溶解度和扩散系数、电化学反应的速率常数、传质系数(coefficient of mass transfer)、板栅与活性物质的欧姆电阻和固相-固相与固相-液相界面的欧姆电位降等。
当有电流流过时,多孔电极的极化包括电化学极化、浓差极化、欧姆极化和结晶极化【23】。
接通电流之后,经过电极微孔中电解质电阻的双电层电荷导致在电极内部建立相对稳恒状态电流分布的时间的滞后,由于微孔的欧姆电阻,从电极表面到极板内部,相对稳恒状态的电流密度很可能是不相同的。
正极和负极的放电曲线如图7-16所示。
铅酸蓄电池放电时,接通电路后的瞬时A的电位降是由于充满隔板的电解液的电阻、板栅、活性物质以及固相-固相、固相-液相界面的欧姆电阻引起的。双电层电容的放电和活性物质微孔中电解质溶液电阻同时起作用,导致B这部分的倾斜。过饱和现象、核晶和结晶现象开始引起正极放电曲线上C部分的电位降【24】。正极的这一行为,也影响到蓄电池在低温与高倍率情况下充电时正极的充电接受能力相对较小。图中D部分表示活性物质不断放电而生成硫酸铅PbSO4。由于酸量不足和硫酸盐晶体阻塞微孔,出现最后的急剧极化部分E。
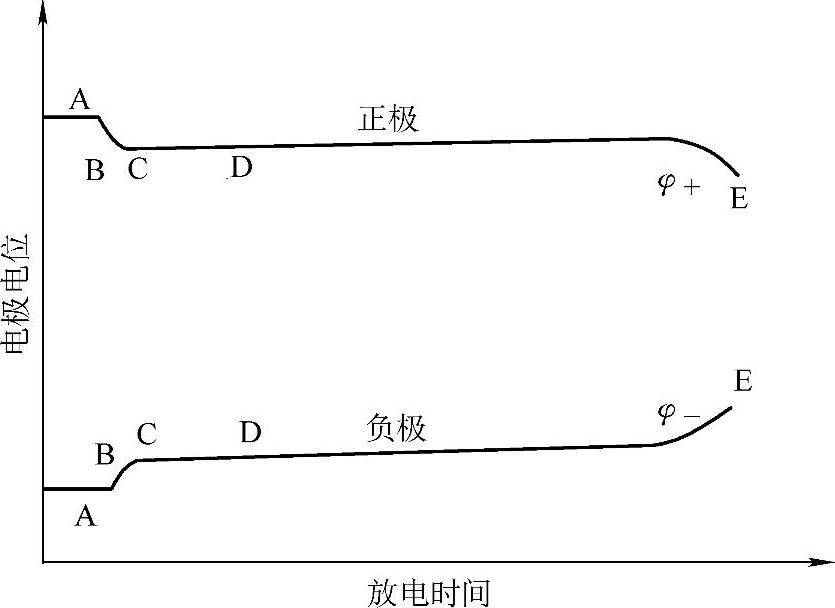
图7-16 铅酸蓄电池正极和负极的放电曲线
正极和负极的基本电极过程的机理是溶解、沉淀。铅电极在硫酸溶液中放电时有下面两个步骤:

和
图7-17表示一个正在放电的微孔。在35%的H2SO4溶液中,铅离子Pb2+的浓度也只有约2mg·L-1,因为多孔电极具有很大的内表面(internal surface),所以,溶解-沉淀机理可以解释铅酸蓄电池能够以高倍率放电这一事实。韦特(Vetter)曾导出一个铅离子Pb2+浓度的简单方程【25】。他假设经过多孔电极各处的电流分布是相同的,所有的电极内表面积都是完全有效的。尽管如此简化假设,计算出来的浓度的数量级还应当是正确的。甚至在表观电流密度(单位表观电极面积的电流强度)很大的情况下,计算出来的浓度增量ΔC也出乎意外的小。例如,在0.1A·cm-2时,电极表面铅离子浓度增量ΔC=4×10-7mol·L。这个值比平衡时PbSO4的溶解度低得多。平衡时PbSO4的溶解度随着酸浓度的增加而减少,随着温度的降低而减少。不论在任何情况下,PbSO4的溶解度对于用溶解-沉淀机理解释蓄电池放电都是足够大的。
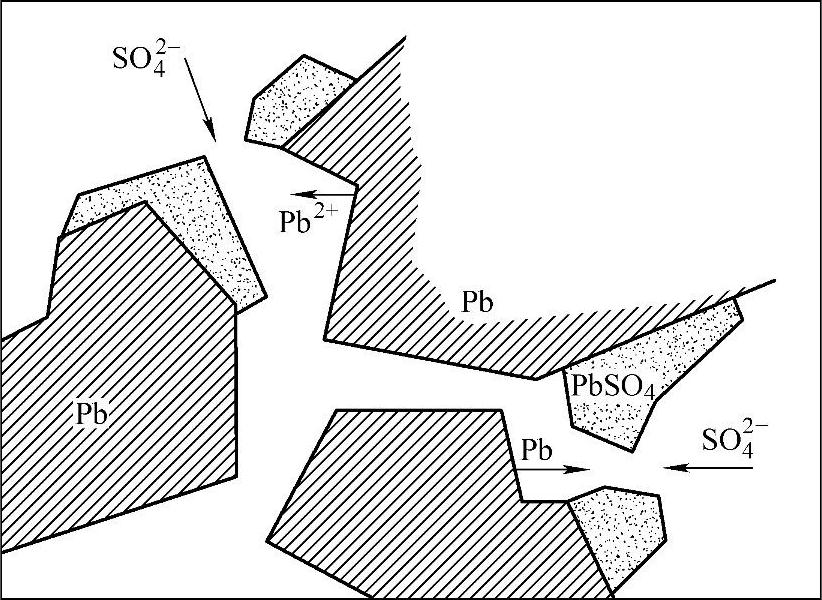
图7-17 负极板微孔中溶解-沉淀机理示意图(https://www.xing528.com)
铅电极的放电和充电可以分别看成是铅离子在稀溶液中的阳极溶解和阴极析出。负极活性物质中的膨胀剂(expander)的作用可以解释为它能够抑制充电时Pb的粗大晶体和放电时PbSO4的粗大晶体的生长【26~31】。
负极放电时的溶解-沉淀机理示意地表示在图7-17中。应用电子扫描显微技术可以看到这一结果。反应产生PbSO4晶体的生长方向是从表面伸向液相内部的,这只能解释为晶体是从溶液析出的【32.33】。
正极二氧化铅电极的放电反应也是通过溶解-沉淀过程进行的。【34】这一过程图示于图7-18。过程的反应方程如下:
PbO2+4H++2e=Pb2++2H2O
Pb2++SO2-4=PbSO4

图7-18 正极板微孔中溶解-沉淀机理示意图
用电子扫描显微技术观察放电的PbO2电极表明,反应生成的PbSO4晶体的形状和放电率有关【35-40】。
用电子扫描显微技术周期性地观察极板的同样的点状微孔的结果,表明溶解-沉淀机理是正确的【41】。在放电时,PbO2表面的晶粒变粗,而在放电开始时PbSO4并无明显变化。随着放电进程的进行,PbSO4很快从溶液中析出。
在5h率放电的后期,相当大一部分表面仍然明显地保留着PbO2。这样看来,似乎是微孔中的酸不足和分离的PbO2晶粒的接触电阻限制了活性物质的利用,而不是由于生成致密的钝性的PbSO4层限制了活性物质的利用。
有人提出了更为复杂的放电机理,认为有2价或4价铅的络合物中间体形成【37,41-45】。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




