(一)水与溶质的相互作用
1. 水与离子和离子基团的相互作用
与离子或离子基团相互作用的水是食品中结合得最紧密的一部分水。因为水-离子相互作用的强度大于H2O-H2O氢键的强度,但是小于共价键的强度。纯水靠氢键键合形成的四面体排列的正常结构可以通过加入电离溶质被破坏。水和简单的无机离子(既不具有氢键受体又没有供体)会产生极性结合即偶极-离子相互作用。图2-1所示为邻近NaCl的水分子之间可能出现的相互作用方式。这种作用通常称为离子水合作用。图中描述了纸平面的第一层水分子。在稀的离子水溶液中,由于第一层水分子和处在更远的以四面体方式定向的体相水所产生的相互矛盾的结构的影响,因此可以认为第二层水是以结构被扰乱的状态存在。在浓的盐溶液中,或许不存在体相水,而离子或许支配着水的结构。
图2-1 邻近NaCl的水分子可能出现的相互作用方式
图中只显示出纸平面上的水分子
在不同的稀盐溶液中,离子对水结构的影响是不同的。一类是电场强度较强、离子半径小/多价离子,大多数阳离子,它们有助于水形成网状结构,因此这类离子的水溶液比纯水的流动性小,例如Li+、Na+、Ca2+、Ba2+、Mg2+、Al3+、F-和OH-。另外,一类电场强度较弱、离子半径大/单价离子,大多数阴离子和大多数阳离子,能阻碍水形成网状结构,这类盐的溶液比纯水的流动性大,例如K+、Rb+、Cs+、NH4+、Cl-、Br-、I-、 和
和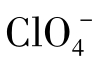 等,实际上,从水的正常结构来看,所有的离子对水的结构都起破坏作用,因为它们能阻止水在0℃下结冰。
等,实际上,从水的正常结构来看,所有的离子对水的结构都起破坏作用,因为它们能阻止水在0℃下结冰。
2. 水与具有氢键键合能力的中性基团(亲水性溶质)的相互作用
食品中蛋白质、淀粉、果胶物质、纤维素等成分通过氢键与水结合。水与亲水性溶质的相互作用弱于水-离子相互作用,强于水-溶质之间的相互作用,后者主要取决于水-溶质氢键的强度。人们或许认为能形成氢键的溶质会促进或至少不会打破纯水的正常结构,然而,在某些情况下,溶质氢键部位的分布和定向与正常水的结构是不相容的,这些类型的溶质对水的正常结构往往都具有一种破坏作用。例如,尿素是具有形成氢键能力的小分子溶质,由于几何构型原因,它对水的正常结构具有明显的破坏作用。但当体系中添加具有氢键键合能力的溶质时,每摩尔溶液中的氢键总数并不会明显地改变。这可能是由于已断裂的H2O-H2O氢键被水-溶质氢键所代替的缘故,因此,这类溶质对水的网状结构几乎没有影响。
氢键结合水和其邻近的水虽然数量有限,但其作用和性质常常非常重要。例如,水能与各种潜在的合适基团(如羟基、氨基、羰基、酰胺或亚氨基)形成氢键。它们有时可形成 “水桥”(指一个水分子与一个或多个溶质分子的两个合适的氢键部位相互作用),维持大分子的特定构象。图2-2和图2-3所示分别为水与木瓜蛋白质分子中的两种功能团之间形成的氢键(虚线)和木瓜蛋白酶肽链之间存在一个3分子水构成的 “水桥”,木瓜蛋白酶和核糖核酸酶肽键之间由水分子构成 “水桥”,将肽键之间维持在一定的构象,很显然这3分子水成了该酶的整体构成部分。
图2-2 水与蛋白质中两类功能团形成的氢键(虚线)
图2-3 木瓜蛋白酶中的一个3 分子 “水桥”23,24,25 是水分子
3. 水与非极性物质的相互作用
向水中加入疏水性物质,例如烃、稀有气体及引入脂肪酸、氨基酸、蛋白质的非极性基团,由于它们与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强。由于在这些不相容的非极性实体邻近的水形成了特殊的结构,处于这种特殊的结构下的水与纯水的结构相似,使得熵下降,此过程被称为疏水水(Hydrophobic Hydration),见图2-4。
图2-4 疏水水合(1)和疏水缔合(2)的图示
空心圆球—疏水基团;影线区域—水
由于疏水水合在热力学上是不利的,因此水倾向于尽可能地减少与共存的非极性物质的缔合。当存在两个分离的非极性基团,不相容的水环境将促进它们之间的缔合,从而减少水-非极性界面面积,这是一个热力学上有利的过程。此过程是疏水水合的部分逆转,被称为 “疏水相互作用”(Hydrophobic Interaction)。
非极性物质具有能和水形成笼形水合物,以及能和蛋白质分子产生疏水相互作用两种特殊的性质。笼形水合物是一种像冰一样的包合物,“主人”物质就是水靠氢键键合形成像笼子一样的结构,将一种 “客人”物质就是小的非极性物质通过物理作用方式截留。笼形水合物的 “主人”一般由20~74个水分子组成,“客人”是一些低分子质量的化合物,只有它们的形状和大小适合于笼子的 “主人”才能被截留。笼形水合物的微结晶与冰的晶体很相似,它们易于生长且可见大小,当形成大的晶体时,原来的四面体结构逐渐变成多面体结构,其在外表上与冰的结构就存在很大差异。一些笼形水合物晶体在0℃以上和适当压力下仍能保持稳定的晶体结构。
典型的 “客人”包括低分子质量烃、卤代烃、稀有气体、短链第一级、二级和三级胺、烷基铵盐、二氧化碳、二氧化硫、环氧乙烷、乙醇等。“主人”水分子与 “客人”分子的相互作用是轻微的,一般是弱的范德华力。此外,分子质量大的 “客人”,如一些蛋白质、糖类、脂类和生物细胞内的其他物质也能与水形成笼形水合物,使水合物的凝固点降低。
水分子和蛋白质疏水基团的缔合对蛋白质的功能性质是非常重要的,因为典型的蛋白质分子中大约40%的氨基酸含有非极性基团(丙氨酸-甲基、苯丙氨酸-苯基、缬氨酸-异丙基、半胱氨酸-巯基甲基、亮氨酸-仲丁基)。由于蛋白质1/3的非极性基团暴露在水中,这在热力学上是不利的,暴露的疏水基团与邻近的水除了产生微弱的范德华力外,它们之间并无吸引力。从图2-5可看出,疏水基团周围的水分子对正离子产生排斥,而吸引负离子,这与许多蛋白质在等电点以上pH时能结合某些负离子的实验结果一致。
图2-5 水在疏水表面的倾向
(二)水的存在状态
按照食品中的水与其他成分之间相互作用强弱可将食品中的水分成结合水(或称为束缚水、固定水)和自由水(或称游离水、体相水)。(https://www.xing528.com)
1. 结合水(束缚水、固定水)
通常是指存在于溶质或其他非水组分附近的、与溶质分子之间通过化学键结合的那部分水。结合水根据被结合牢固程度的不同,被分为几种不同的形式:
(1)化合水 是结合得最牢固的、构成非水物质组成的那些水。例如,化学水合物中的水。
(2)邻近水 处在非水组分亲水性最强的基团周围的第一层位置,与离子或离子基团缔合的水是结合最紧密的邻近水。主要的结合力包括:水-离子和水-偶极缔合作用,其次是一些具有呈电离或离子状态的基团的中性分子与水形成的水-溶质氢键力。
(3)多层水 是指位于以上所说的第一层的剩余位置的水和在邻近水的外层形成的几个层。多层水主要是靠H2O-H2O和H2O-溶质间氢键而形成。尽管多层水不像邻近水那样牢固地结合,但仍然与非水组分结合得紧密,且性质与纯水的性质也不相同。因此,这里所指的结合水包括化合水和邻近水以及几乎全部多层水。
2. 自由水(游离水、体相水)
通常是指没有被非水物质化学结合的水。它又可分为三类:不移动水或滞化水、毛细管水和自由流动水。
(1)滞化水 是指被组织中的显微和亚显微结构与膜所截留住的水,由于这些水不能自动流动,所以称为不移动水或滞化水。
(2)毛细管水 是指在生物组织的细胞间隙和制成食品的结构组织中存在着的一种由毛细管力所截留的水,在生物组织中又称细胞间水,其物理和化学性质与滞化水相同。
(3)自由流动水 是指动物的血浆、淋巴和尿液、植物的导管和细胞内液泡中的水,因为都可以自由流动,所以称为自由流动水。
食品中水分的划分是相对的。食品中所说水分的含量,一般指在常压下,105℃左右直接干燥情况下,所失去物质的总量。
3. 结合水和自由水的区别
结合水和自由水之间的界限是很难定量地做截然的区分。只能根据物理、化学性质做定性的区分。
(1)食品中结合水对食品的风味起着重大作用,当结合水被强行与食品分离时,食品风味、质量就会改变。这主要是由于结合水的量与食品中有机大分子的极性基团的数量有比较固定的比例关系。
(2)食品中的结合水比自由水难除去。
(3)结合水冰点大为降低,甚至在-40℃都不易结冰,而游离水能结冰,冰点略微降低。
(4)结合水不能作为溶质的溶剂,而自由水可以作为溶剂。
(5)结合水不能被微生物利用,而游离水可以被微生物利用,所以当食品中含有较多的游离水时,易腐败变质。
小资料
水是营养素吗?
水是一切生命活动必需的物质。成年男子60%的体重都是水,成年女子则为50%~55%,可见,水是人体中含量最多的成分。水是营养素的一种,我们必须每天喝水。每人每日的需水量因气温、身体状况、工作条件和环境状况而有很大的变动,补充水分要少量多次。成年人每天应摄入不少于2000 mL的水分,中小学生的饮水量每天在1200~1500mL较为适宜。合格的自来水应成为主要的饮用水来源。此外,还有纯净水和矿泉水。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




