(1)方法提要 试样经酸溶解,在硫酸-磷酸介质中,于室温用高锰酸钾将钒氧化至五价。过量的高锰酸钾在尿素存在下,用亚硝酸钠还原。以N-苯代邻氨基苯甲酸为指示剂,用硫酸亚铁铵标准滴定溶液滴定钒。
本方法适用于高温合金中钒含量的测定,不适用于钴的质量分数大于20%及铈的质量分数大于0.01%的试样中钒量的测定,测定范围为0.20%~5.00%(质量分数)。
(2)主要试剂
1)盐酸(1.19g/mL)、硝酸(1.42g/mL)、磷酸(1.69g/mL)、硫酸(1.84g/mL)、硫酸(1+1)、硫酸(5+95)。
2)高锰酸钾溶液(5g/L):储于棕色瓶中。
3)尿素溶液(200g/L):现用现配。
4)亚硝酸钠溶液(30g/L和5g/L)。
5)亚砷酸钠溶液(5g/L):称取0.5g三氧化二砷,置于适量水中,加入1g无水碳酸钠,加热溶解,冷却后稀释至100mL,摇匀。
6)重铬酸钾标准溶液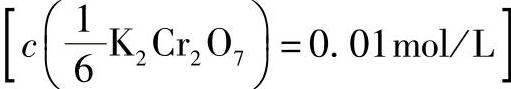 。
。
7)硫酸亚铁铵标准滴定溶液:(NH4)2Fe(SO4)2浓度约为0.01mol/L。称取4g硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]溶解于适量的硫酸溶液(5+95)中,并用此酸稀释至1000mL,摇匀。用重铬酸钾标准溶液进行准确浓度c1的标定和指示剂校正V2。
8)N-苯代邻氨基苯甲酸(2.0g/L):称取0.2gN-苯代邻氨基苯甲酸,置于适量水中,加入0.2g无水碳酸钾,加热溶解,冷却后用水稀释至100mL,摇匀。
(3)分析步骤
1)试样:称取0.25~0.50g试样,精确至0.0001g。所称试样中钒量宜大于1mg,含铬20%(质量分数)或锰20%(质量分数)或钨18%(质量分数)以上的试样,可适当减少称样量。(https://www.xing528.com)
2)测定
①试液的制备:将试样置于300mL锥形瓶中,加入25~30mL盐酸(1.19g/mL)、3~5mL硝酸(1.42g/mL)、10mL磷酸(含高钨试样,可加入15mL),微热至试样溶解,稍冷,加入30mL硫酸溶液(1+1),加热蒸发至冒硫酸烟2~3min(溶样后若有碳化物,则可在冒硫酸烟时滴加硝酸,使之分解),稍冷,加入50mL水,加热溶解盐类。
若试样中铬的质量分数高于20%,宜增加用盐酸散铬的步骤,以便于在氧化钒时容易观察试液颜色的变化。
将试液冷却至室温,在不断摇动下滴加高锰酸钾溶液至试液呈稳定的紫红色并过量2滴或3滴,放置3~5min,加入10mL尿素溶液,静置片刻,在振摇下逐滴加入亚硝酸钠溶液(5g/L)还原过量的高锰酸钾至溶液红色消退,并过量1滴或2滴,加入10mL亚砷酸钠溶液、2滴亚硝酸钠溶液(30g/L),放置2~3min。
②滴定:于上述试液中滴加3滴N-苯代邻氨基苯甲酸溶液,用硫酸亚铁铵标准溶液缓慢滴定,接近终点时,逐滴滴定至溶液由樱桃红突变为亮绿色为滴定终点。
(4)结果计算 试样中钒的质量分数的计算公式为
式中 c1——硫酸亚铁铵标准溶液的浓度(mol/L);
V2——滴定时所消耗硫酸亚铁铵标准溶液的体积(mL);
V1——N-苯代邻氨基苯甲酸溶液(指示剂)的校正值(mL);
m——称样量(g);
0.05094——钒的毫摩尔质量(g/mmol)。
若试样中铈含量不高,则可用校正系数来消除其影响,0.01%(质量分数)的铈相当于0.0036%(质量分数)的钒。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




