1.沉淀分离-EDTA滴定法
(1)方法提要 试样用硫酸溶解,使铅(Ⅲ)以硫酸铅的状态沉淀析出,从而与大量锡、锑、铜、镍、镉、铁等元素分离。将所析出的沉淀物硫酸铅滤出并溶解于乙酸铵溶液中,然后用EDTA滴定。可能被硫酸铅沉淀吸附的少量杂质离子,可用1,10-二氮菲掩蔽。
(2)主要试剂
1)“铅酸”溶液:在500mL水中,加50mL硫酸,另取0.5g硝酸铅,溶于200mL水中,将两份溶液合并,并稀释至1000mL,放置24h,过滤后保存其澄清溶液。
2)1,10-二氮菲溶液(0.25%)乙醇溶液。
3)EDTA标准溶液[c(EDTA)=0.02000mol/L]:称取7.4448g基准EDTA溶于水中,移入1000mL容量瓶中,加水稀释至刻度。
(3)分析步骤 称取0.5000g试样,置于300mL烧杯中,加20mL硫酸,先在低温下加热至试样分解,升温加热至试样溶解完全,稍冷,加100mL“铅酸”溶液,加热使盐类溶解,冷却至60~70℃(不低于60℃),用慢速滤纸过滤,用“铅酸”溶液洗涤沉淀,将沉淀及滤纸移入原烧杯中,加30mL乙酸铵溶液(20%),加热煮沸,使硫酸铅溶解,冷却至室温,加水至约100mL,加5mL1,10-二氮菲,加数滴二甲酚橙指示剂(0.2%),用EDTA标准溶液滴定至溶液由紫红色转变为纯黄色为终点。
(4)结果计算 铅的质量分数的计算公式为
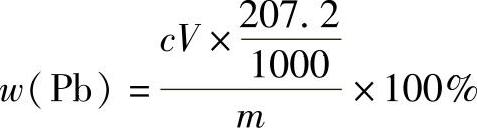 (https://www.xing528.com)
(https://www.xing528.com)
式中 c——EDTA标准溶液的浓度(mol/L);
V——滴定时消耗EDTA标准溶液的体积(mL);
207.2——铅的摩尔质量(g/mol);
m——称样量(g)。
(5)附注
1)根据试样中的铅含量,可改变称样量。
2)过滤时溶液温度不能太低,以防锡水解析出。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




