1.EDTA滴定法
(1)方法提要 试样用盐酸、硝酸溶解,锡呈四价转入溶液中,化学反应式为
3Sn+4HNO3+12HCl=3SnCl4+4NO↑+8H2O
在酸性溶液中,加入过量的EDTA溶液,于沸腾的条件下与四价锡及铅、铁、铜等元素形成络合物,用六次甲基四胺控制溶液pH=5~5.5,然后以二甲酚橙为指示剂,用铅标准溶液滴定过量的EDTA。
加入氟化物络合锡,并释放出与锡等物质的量的EDTA,然后用铅标准溶液滴定释放出的EDTA,间接测得锡含量。
除铝、钛干扰测定外,其他元素不干扰测定。但锡、铅合金中铝、钛含量极少,一般可不考虑。
(2)主要试剂
1)EDTA溶液[c(EDTA)=0.05mol/L]:称取18.6gEDTA二钠盐,溶于水中,并稀释至1000mL。
2)铅标准溶液[c(Pb2+)=0.02000mol/L]:称取4.1442g纯铅(质量分数为99.95%),溶于15mL硝酸中(1+3),煮沸驱除氮的氧化物,冷却,移入1000mL容量瓶中,以水稀释至刻度。
(3)分析步骤 称取0.1000g试样,置于250mL锥形瓶中,加10mL盐酸(1+1)及2mL硝酸(1+1),于低温处溶解,煮沸片刻,驱除氮的氧化物,取下,加40mL水、25mLEDTA溶液(0.05mol/L),加热煮沸20s,冷却至室温,加2滴对硝基酚指示剂(0.2%),用氨水(1+4)调至溶液呈黄色,再用盐酸(1+1)调至黄色褪去,加10mL六次甲基四胺溶液(20%),此时溶液pH值在5.5左右,加3滴或4滴二甲酚橙指示剂(0.2%),用铅标准溶液滴定至溶液恰呈红色(不计数),然后加2g氟化铵,加热至40℃左右(或放置5min)取下,继续用铅标准溶液滴定至溶液呈红色为终点。
(4)结果计算 锡的质量分数的计算公式为
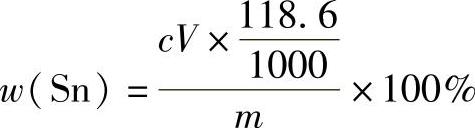
式中 c——铅标准溶液的浓度(mol/L);
V——滴定至终点时所消耗铅标准溶液的体积(mL);
118.6——锡的摩尔质量(g/mol);
m——称样量(g)。
(4)附注
1)可用PAN代替二甲酚橙,而滴定剂用铜标准溶液。为了增加PAN的溶解度,使终点敏锐,可加20mL乙醇(或提高滴定温度至60℃左右),滴定时要缓慢进行。
2)释放剂以氟化铵为好,因为氟化铵不释放Fe-EDTA络合物,而氟化钠、氟化钾有形成氟铁酸盐沉淀的可能,使部分Fe-EDTA络合物中的EDTA释放出来,致使测定结果偏高。
2.碘滴定法
(1)方法提要 试样用硫酸溶解,在盐酸介质中,于隔绝空气的条件下,用纯铝将锡(Ⅳ)还原成锡(Ⅱ),然后以淀粉溶液为指示剂,迅速用碘标准溶液滴定锡(Ⅱ),化学反应式为
SnCl2+I2+2HCl=SnCl4+2HI(https://www.xing528.com)
或用碘酸钾标准溶液作为滴定剂,滴定时碘酸钾在盐酸溶液中与碘离子反应,定量地释放出碘,化学反应式为
KIO3+5KI+6HCl=3I2+6KCl+3H2O
所释放出来的碘再与锡(Ⅱ)反应,滴定终点仍用淀粉溶液指示。
本方法适用于锡基、铅基合金中锡的测定。
(2)主要试剂
1)三氯化锑溶液(2%):称取2g三氯化锑,溶于50mL盐酸中,用水稀释至100mL。
2)淀粉溶液(1%):称取1g淀粉,加5mL水调成浆状后,倒入100mL沸水中,冷却。
3)碘酸钾标准溶液:称取3.567g碘酸钾,溶于含有1g氢氧化钠及10g碘化钾的200mL水中,用水稀释至3000mL。此溶液1mL相当于2mg锡。可称取纯锡,按分析步骤操作,求得滴定度。
(3)分析步骤 称取0.3~1.5g试样(将其中的锡含量控制在0.1~0.2g,而铜、锑的量分别不超过0.01g和0.1g),置于500mL锥形瓶中,加5g硫酸氢钾及20mL硫酸,加热使试样溶解,稍冷,加100mL水、80mL盐酸。若试样不含锑,则需加2滴三氯化锑溶液(2%),再加2g纯铝,迅速装上盛有饱和碳酸氢钠溶液的隔绝空气装置。此时作用十分剧烈,宜用冷水冷却,以防止溶液冲出瓶外。当作用缓慢时,置于低温加热,至铝完全溶解及黑色悬浮物下沉,取下,放在冰水中迅速冷却至10℃以下,并注意补充隔绝空气装置中的碳酸氢钠溶液,以免空气进入瓶内。
冷却完毕后,取去隔绝空气装置,迅速加入5mL碘化钾溶液(10%)及5mL淀粉溶液(1%),立即以碘酸钾标准溶液滴定至恰呈蓝色为终点。
(4)结果计算 锡的质量分数的计算公式为
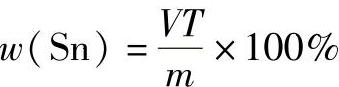
式中 V——滴定时消耗碘酸钾标准溶液的体积(mL);
T——碘酸钾标准溶液对锡的滴定度(g/mL);
m——称样量(g)。
(5)附注
1)溶解试样时,开始时加热温度不宜太高,以免有部分试样熔化而使试样溶解不完全。待试样溶解完全后,应在活火头上强热逐出或洗下瓶壁上的硫。
2)加入少量三氯化锑溶液,可抑制空气对二价锡的氧化。
3)在还原过程中,开始有较多的黑色粉状悬浮物出现,其中大部分是元素状态锡,经加热煮沸后,锡以二价状态溶于盐酸溶液中,最后残留于溶液底部的黑色粉状物为元素状态的铜、锑等元素。
4)经验表明,10mg以下的铜、100mg以下的锑、50mg以下的砷,对测定干扰不大。
5)配制碘酸钾溶液及滴定试样时,都加入了较多的碘化钾,目的是使溶液中有足够的碘离子来保证它与碘酸钾之间的反应能定量地完成。同时,过量的碘离子可使反应中生成的且在水中几乎不溶的碘能以KI3-络合物的状态很好地溶于水中,避免碘的挥发损失。但是碘化钾的浓度太高,会使碘与淀粉所产生的蓝色转变不灵敏。适宜的碘化钾用量应是需要量的4~5倍。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




