在一个完整的IgG分子的基础上,通过去除某些非功能的或者非关键性的抗体片段,只保留对抗原、抗体结合反应有重要意义的功能部分,得到的具有一定生物活性和功能的抗体片段称为小分子抗体。小分子抗体一般具有相对分子质量小、免疫原性低和易于清除等特点。完整抗体分子的糖基化修饰一般由哺乳动物细胞表达产生,技术含量和生产成本都较高。此外,IgG型抗体的相对分子质量约为150000,抗体及其偶联物在实体瘤中存在穿透性较差的问题。与之相比,小型化抗体药物不需要糖基化修饰,可以在原核细胞中表达,操作方便,生产成本较低。同时,小分子抗体也易于进一步进行基因工程改造,如构建抗体融合蛋白等。因此,抗体小型化也日益成为抗体药物研发的一种趋势。
目前常见的小分子抗体有Fab片段、F(ab')2片段、Fv段、单链抗体(single chain Fv,scFv)、单域抗体(single domain antibody,sdAb)和最小识别单位等(图3-4)。

图3-4 小分子抗体组成
(一)Fab抗体
Fab抗体片段由重链V区及CH1区(即Fd段)和完整的轻链以链间二硫键连接而成(图3-5),较好地保持了天然抗体分子的Fv段的结构,主要发挥抗体的抗原结合功能。相比于单链抗体,Fab抗体在构成上多了轻链的恒定区和重链恒定区的CH1区,相对分子质量要大些,一般为50000,因此其药物渗透能力较弱,在人体内被清除的效率更低。Fab抗体生产工艺简单,抗原、抗体结合能力较强,在这两方面优于单链抗体。但是Fab抗体同时也存在稳定性更差、轻重链之间更易解离的问题,再加上引入了部分恒定区,Fab抗体的免疫原性也有所增加,这些缺点都使其在成药应用方面受到一定制约。研究发现,Fab分子具有聚合的先天优势,而且其聚合体的稳定性和抗原、抗体结合能力都优于单体,因此,通过单体产生有价值的其他抗体片段或聚合体分子,也将是Fab抗体应用发展的主要方向之一。目前上市的Fab抗体有阿昔单抗(Abciximab),一种抗血小板凝聚单克隆抗体嵌合Fab,靶标为糖蛋白Ⅱb/Ⅲa受体;赛妥珠单抗(Certolizumab),聚乙二醇人源化抗TNF-α单克隆抗体Fab片段;雷珠单抗(Ranibizumab),一种人源化抗VEGF-A Fab片段等。
早期Fab片段的制备是通过木瓜蛋白酶对完整抗体分子酶解后分离纯化获得的,现已能从大肠杆菌获得。抗体分子与抗原的结合依赖于抗体分子的立体构象,即需要可变区正确的立体折叠、链内二硫键的形成以及轻链、重链可变区两个分子间相互作用形成正确的立体构象,这一过程在B细胞内是在粗面内质网腔内完成。大肠杆菌细胞壁的周质腔(periplasm)可提供类似于内质网的环境。将重链Fd基因与轻链基因5'端接上细菌蛋白的前导序列,所表达的蛋白在细菌前导肽的引导下可分泌到周质腔,前导肽被前导肽酶(signal peptidase)所裂解,生成的Fd段和轻链在周质腔内完成立体折叠和链内、链间二硫键的生成,成为有功能的Fab片段。但其在原核细胞的分泌型表达受到蛋白质分子穿过内膜和折叠效率的影响,因而表达量较低。
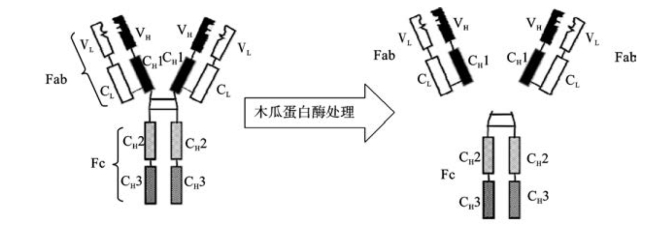
图3-5 Fab抗体结构简图
(二)Fv抗体(https://www.xing528.com)
Fv抗体片段由重链可变区(VH)和轻链可变区(VL)组成,两者通过非共价键结合,是抗体分子中保留抗原结合活性的最小功能片段,约为完整分子的1/6。其分子小,免疫原性弱,对实体瘤的穿透力强,能发酵生产,可作为载体与药物、放射性核素、毒素等相结合,用于肿瘤的诊断和治疗或用于细胞内免疫,也可看作基因治疗的一种方案。用前述基因工程表达方法,通过将VH和VL转送到大肠杆菌周质腔,可获得有功能的Fv段。由于Fv段中VH和VL由非共价键结合在一起,因而在浓度较低时有解离的倾向,极不稳定。不同Fv段的解离常数不同,一般浓度在10-5~10-4mol/L之间,欲获得稳定的Fv段,需设法将两个可变区比较稳定地结合在一起。二硫键稳定的Fv(disulfide-stabilized Fv,dsFv),则是在VH和VL的适当位置各引入一个半胱氨酸而形成的。将VH442-VL100或VH 1052-VL43作为构建dsFv的通用位点,二硫键位置远离CDRs,dsFv稳定且抗原结合活性不受影响。
(三)scFv
将抗体的VH和VL通过一条短的连接肽(linker)连接,就得到了一个单链抗体。单链抗体是保留了完整抗原、抗体结合位点的最小功能片段,较好地保留了亲本抗体对抗原的结合能力。在功能方面,单链抗体具有穿透力强、免疫原性低、易于连接、便于直接获得免疫毒素或酶标记抗体等的特点。在结构方面,单链抗体在不影响正常的抗体、抗原结合的前提下有两种构建方式,分别是VH-连接肽-VL或VL-连接肽-VH。在抗体构建方面,单链抗体构建成功与否的关键在于连接VH和VL的连接肽的设计,要求连接肽要能够保证抗原、抗体结合的正确空间构象。一般以15~20个氨基酸长度为宜,氨基酸的组成设计应使连接肽具备亲水性、易于折叠,不宜有过多的侧链,以减少抗原性。应用最广的连接肽是(GGGGS)3。就抗体片段的生产而言,单链抗体几乎可以在任何抗体表达系统中成功表达,如应用较为成熟的原核表达系统,因而生产难度大大降低。利用大肠杆菌表达scFv可有两种方式:一种方式是表达为包涵体或非包涵体性不溶蛋白,这种表达方式的产量较高,但需进行变性、复性等后续工作;另一种方式是分泌型表达,与Fab抗体片段表达的原理相同,利用前导序列使scFv分子分泌到周质腔内,在周质腔内完成二硫键的形成和肽链折叠,成为有活性的单链抗体分子,但产量比较低。单链抗体分子也有自身的不足,如稳定性差且亲和力低,易形成多聚体等。Brolucizumab是目前Ⅲ期临床试验的人源化单链抗体片段,相对分子质量约为26000,用于治疗新生血管性年龄相关性黄斑变性,靶标是血管内皮生长因子A(VEGFA)。
在scFv基础上进一步改造可得到一系列基于单链抗体的衍生物。如前述通过二硫键稳定连接的dsFv抗体;若缩短连接肽而不允许同一链上的VH和VL结构域之间配对的连接体,从而迫使其与另一条链的VH和VL互补配对并形成两个抗原结合位点则可得到双价抗体(如双链抗体di-scFv,甚至多价小分子抗体);由C端融合恒定区CH 3得到微型抗体等。单链抗体基因片段还可以与适当的毒素蛋白基因重组,直接在大肠杆菌中融合表达重组免疫毒素(immunotoxin)。常用毒素包括假单胞菌外毒素、蓖麻毒素及白喉毒素。与完整抗体免疫毒素相比,scFv免疫毒素具有操作更简单、价廉、免疫原性低和易于进入肿瘤组织内部等优势。进入Ⅲ期临床试验的Oportuzumab monatox是一种靶向上皮细胞黏附分子(EpCAM)的人源化scFv免疫毒素,其由一种人源化抗EpCAM抗体scFv与假单胞菌外毒素A偶联而成。
总而言之,单链抗体虽然由于自身稳定性差等不利于成药,但可将其作为基础或中间体用于其他小分子抗体药物或抗体-药物偶联物的研究。
(四)单域抗体
根据抗体分子的结构特点,Fv段是保留抗原结合活性的最小结构。但有些情况下,单独的抗体的重链可变区或轻链可变区也可以结合抗原。于是,学者们开始研制一种只有可变区的小分子抗体片段,称之为单域抗体(single domain antibody),也称单区抗体、小抗体、纳米抗体。单域抗体的优势在于相对分子质量更小、免疫原性更低,却几乎拥有相当的抗原、抗体结合能力。
驼科动物体内会产生一种独特的抗体:缺失轻链的重链抗体(HcAb)。克隆这种抗体重链可变区可以得到只由重链可变区组成的单域抗体,也称为VH H。驼科动物的VHH亚型单一,而且天然存在,稳定性和可溶性都相当好,省去了其他单域抗体获得后还需要进行的修饰过程。基于驼科动物VHH是单域抗体研究的热点。对VHH立体构象分析发现,其抗原结合部位的构象较为特殊,可形成CDR3凸出的抗原结合部位,可造成特殊的抗体、抗原结合形式,即抗体CDR襻状结构插入抗原表面的凹陷中。这在制备酶的抑制剂中有重要意义,因为酶的催化部位常常位于酶蛋白表面的凹陷中,这些部位通常不易制备相应抗体。驼科动物VH H的这一特殊结构使其可用于制备酶的抑制性抗体,也展示了驼科化人单域抗体的应用前景。罕见血栓性微血管病治疗新药卡普赛珠单抗(Caplacizumab)是一种抗血管性血友病因子(vWF)的人源化纳米抗体,于2018年获欧盟委员会、2019年获美国FDA批准上市。
抗体与抗原的结合机制通常为抗原和抗体可变区上的6个CDR发生相互作用,而CDR中以CDR3尤其重链CDR3最为关键。但有研究发现,某些情况下仅单个CDR就可以实现与抗原的结合,这样的CDR称为最小识别单位(minimal recognition unit,MRU)。最小识别单位在动力学及渗透性方面具有优势,但因为分子本身缺少框架支撑,所以稳定性较差。因为其穿透能力强,半衰期短,本底低,故在临床影像学诊断中具有应用前景。也有研究者提出在最小识别单位的基础上适当引入一些氨基酸序列稳定其理化性质,同时尽可能保证其小分子的特点;或者通过结构分析,用非肽类化学结构进行模拟,开发治疗性药物。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




