生物技术制药应用广泛,可以生产出多种生物技术药物以治疗肿瘤、心血管疾病、糖尿病、免疫性疾病、神经退行性疾病等许多传统药物难以治疗的疑难病症,为人类健康事业的发展开辟了新道路。现就近几年生物技术制药的几个热点应用及其研究进展进行阐述。
(一)基因治疗药物
基因治疗(gene therapy)是指将外源正常基因导入靶细胞,以纠正或补偿缺陷和异常基因引起的疾病,以达到治疗目的。基因治疗按照治疗方式,主要分为两大类。
1.体内基因治疗 直接向血液或者目标器官中注射携带所需基因的载体。
2.体外基因治疗 把患者的细胞从体内移出,在体外对细胞进行基因改造,然后重新输入患者体内。例如:体外对造血干细胞的基因改造,如用于治疗镰状细胞贫血的基因治疗产品;对免疫T细胞的基因改造,包括CAR-T、TCR-T免疫疗法等。
近年来,基因治疗逐渐成为许多国家的科研人员的研究热点,越来越多的基因治疗药物获批上市(表1-5)。
表1-5 近年来上市的一些基因治疗药物
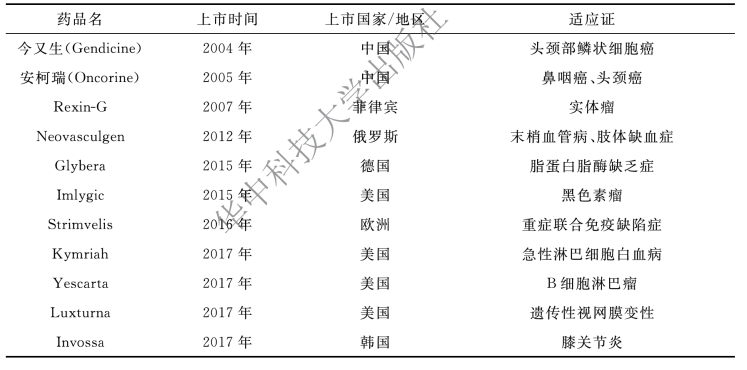
在1989年至2017年4月期间,已完成、正在进行或已获得全球批准的基因治疗临床试验有2463项,其中有64.4%是针对癌症治疗。
2017年7月,美国FDA顾问小组建议批准Tisagenlecleucel(Kymriah)用于治疗儿童和年轻成人(2~25岁)的急性淋巴细胞白血病。Tisagenlecleucel是一种嵌合抗原受体T细胞(chimeric antigen receptor T-cell,CAR-T)免疫疗法,被美国FDA于2017年8月30日批准上市,是全球首个获批的CAR-T免疫疗法,也是美国市场的第一个基因治疗产品,具有里程碑式的意义。
虽然大多数基因治疗临床试验都涉及癌症,但也有大量基因治疗试验针对的是罕见的遗传性单基因疾病(占所有基因治疗试验的10.5%)。单基因疾病是由已知的单基因缺陷引起的疾病,有望通过在宿主细胞中插入并表达突变基因(或缺失基因)的单个正确拷贝而治愈。遗传性出血性疾病——血友病B,就是一种单基因疾病,2017年12月,《新英格兰医学杂志》(The New England Journal of Medicine)报道称,基因疗法首次在血友病B患者身上取得成功。
截至2017年,超过77%的基因治疗临床试验处于Ⅰ期或Ⅰ/Ⅱ期,有93项基因治疗临床试验处于Ⅲ期。预计到2020年,将有5~10种基因疗法可被应用,第一批基因疗法可能用于治疗先天性黑蒙症、镰状细胞贫血、β-地中海贫血以及一系列癌症和罕见的遗传性疾病。基因治疗必将开启一个靶向的、个性化的治疗时代。
除基因治疗药物外,基因编辑技术的突破也在一定程度上推动了基因治疗的发展。其中,人工核酸内切酶介导的基因编辑技术主要包括三种:ZFNs技术、TALENs技术和CRISPR/Cas9技术。与传统基因工程中的病毒载体相比,基因编辑技术提供了一个精准的“手术刀”进行基因的增减及修改。CRISPR(clustered regularly interspaced short palindromic repeats,成簇规律间隔短回文重复序列)作为一种新的、革命性的基因编辑工具,已成功用于体外基因编辑,以纠正有缺陷的基因型,此外,一些研究还表明CRISPR技术可以在体内成功实施。针对癌症靶向治疗,目前已有多项涉及CRISPR/Cas9技术的临床试验在中国和美国获得批准。
2016年,我国肿瘤学家卢铀领导的一个科研团队开始进行全球首例人类CRISPR临床试验。研究人员从晚期肺癌患者体内提取免疫细胞,然后利用CRISPR/Cas9技术删除免疫细胞中的PD-1基因,之后研究人员在实验室中扩增这些基因编辑的细胞,再将它们重新注入患者血液中。正常情况下,PD-1蛋白能检查T细胞启动免疫反应的能力,但当肿瘤细胞上的PD-L1蛋白与其结合后,便提供了抑制性信号,诱导T细胞的凋亡,抑制T细胞的活化和增殖,使肿瘤细胞逃脱免疫细胞的攻击。
近年来,CRISPR疗法已经取得巨大进展,该工具有望大力推动基因治疗的发展。

知识链接1-3
(二)单克隆抗体药物
伴随着抗体技术的不断发展以及新型抗体的不断出现,单克隆抗体药物已成为制药行业发展最快的领域之一,目前正在研究的生物技术药物中有四分之一都是单克隆抗体药物。作为最大类的生物技术药物,其在癌症、炎症性疾病、心血管疾病、器官移植、感染、呼吸系统疾病和眼科疾病中皆有应用。单克隆抗体药物包括单克隆抗体(mAbs)和各种单克隆抗体衍生物,例如双特异性抗体(BsAbs)、抗体-药物偶联物(ADC)、放射免疫偶联物、抗原结合片段Fab和Fc融合蛋白等。
于1986年注册的莫罗莫那-CD3(商品名Orthoclone OKT3),是第一种单克隆抗体药,可用于逆转急性器官(包括心脏、肾脏和肝脏)移植排斥反应。然而,抗体市场的动态发展始于20世纪90年代末期,当时第一个嵌合单克隆抗体被注册。2002年,美国FDA批准了第一个完全人源化单克隆抗体——阿达木单抗。截至2017年3月,在欧盟和美国,共注册了71种单克隆抗体药物。
双特异性抗体是含有两种特异性抗原结合位点的人工抗体,能在靶细胞和功能分子(细胞)之间架起桥梁,从而激发具有导向性的免疫反应。截至2017年11月,美国FDA共批准了三种双特异性抗体,分别是卡妥索单抗(Catumaxomab)、博纳吐单抗(Blinatumomab)、重组艾米希组单抗(Emicizumab)。2017年6月,脑肿瘤治疗药物Burtomab获得美国FDA突破性疗法认定。目前,仍有大量双特异性抗体药物处于研究阶段,许多临床试验正在进行。
抗体-药物偶联物和放射免疫偶联物都可以对癌细胞进行特异性破坏。抗体-药物偶联物包含单抗、连接子和药物三部分,而放射免疫偶联物包含单抗、连接子和放射性核素三部分。抗体-药物偶联物的代表有Brentuximab vedotin和Ado-trastuzumab emtansine,前者用于治疗霍奇金淋巴瘤和系统性间变性大细胞淋巴瘤,后者用于治疗HER2阳性乳腺癌。2017年8月,美国FDA批准将Inotuzumab ozogamicin用于治疗成人复发性或难治性前体B细胞急性淋巴细胞白血病。至于放射免疫偶联物,已有两种该类药物被注册用于治疗非霍奇金淋巴瘤,分别是131-托西莫单抗(131I-tositumomab)和替伊莫单抗(ibritumomab tiuxetan)
此外,由于全球销售排名靠前的多种单抗药物将在近期专利到期,单抗的生物类似药已逐渐成为医药界的研究热点。与原研生物技术药物相比,生物类似药的开发所需的时间和成本大大降低。
(三)疫苗(https://www.xing528.com)
疫苗开发是生物技术药物研究的另一个重要领域。任何在开发过程中使用了分子生物学方法的疫苗都可以被归类为生物技术药物。例如减毒活疫苗使用了DNA重组技术来改变病原体的基因组,基因工程亚单位疫苗是特异性高、高度纯化的重组蛋白抗原。
许多新型疫苗正处在研究阶段或临床试验阶段,如HIV疫苗、疟疾疫苗、万能流感疫苗和治疗性癌症疫苗等。
HVTN 702和Ad26是目前仅有的两种在人体试验中显示出有效性的HIV疫苗。HVTN 702疫苗由两种疫苗组成,一种是基于金丝雀痘载体的疫苗(ALVAC-HIV),另一种是含有MF59佐剂的双组分120 HIV糖蛋白亚单位疫苗,其临床试验预计在2020年末可以产生结果。Ad26疫苗旨在针对引起艾滋病的各种HIV亚型来诱导免疫应答。该疫苗使用一种腺病毒血清型26菌株作为载体,为HIV变异基因和含有磷酸铝的Clade C 140 HIV糖蛋白提供三种或四种嵌合抗原。

知识链接1-4
在过去的十多年中,疟疾疫苗的开发取得了实质性的进展。2015年,基于重组蛋白的疟疾疫苗RTS,S获得了欧洲药品管理局(EMA)的批准,成为世界上首个获得许可的疟疾疫苗。2018年,疟疾疫苗RTS,S在非洲三国(加纳、肯尼亚和马拉维)首次投入应用,为在全球更大范围内推广疟疾疫苗铺设道路。
生物技术制药的发展也促进了万能流感疫苗的开发。与目前使用的疫苗相比,万能流感疫苗能够提供持久而广泛的抗流感作用。从流感病毒H1血细胞凝集素纯免疫原的结构开发中获得了一些有希望的结果:在小鼠和雪貂中接种该免疫原后,诱导出了广泛的交叉反应抗体,可完全保护小鼠并部分保护雪貂免受致死性异源亚型H5N1流感病毒的攻击。更多结果表明,该疫苗诱导的血凝素特异性抗体可以预防多种1型流感毒株。
近年来,随着人类寿命的延长,癌症逐渐成为主要的疾病死亡原因。而治疗性癌症疫苗可在癌症早期阶段就介入疾病管理过程。Sipuleucel-T是一种自体细胞来源的免疫治疗药,用于治疗去势抵抗性前列腺癌。2010年,Sipuleucel-T由美国FDA批准上市,成为首个获批用于治疗癌症的疫苗,为更广泛地使用癌症疫苗免疫疗法带来可能。
新技术的出现是生物技术药物开发的一个重要课题。反向疫苗学、结构疫苗学和合成疫苗等新技术有望为疫苗领域带来巨大的改变。
反向疫苗学使用生物信息学工具来筛选病原体的整个基因组,以鉴定可以编码具有良好疫苗靶标属性的蛋白质的基因。目前的反向疫苗学方法包括多个基因组序列的比较计算机分析,实现了异质病原体群体中保守抗原的鉴定,并可以鉴定存在于病原性菌株而非共生菌株中的抗原。此外,转录组学和蛋白质组数据集被整合到选择过程中,加速了受试动物模型中疫苗靶标的鉴定。反向疫苗学已成功应用于抗血清群B脑膜炎球菌。该技术还用于具有抗生素抗性的病原体的高级临床前和临床疫苗研究。
结构疫苗学可鉴定免疫蛋白结构域并以重组形式进行表达。该结构域含有可诱导保护性免疫应答的表位,而不含有无关的免疫蛋白区域,可以作为有效的免疫原。一项研究表明,利用呼吸道合胞病毒的表位,结构疫苗学能够产生小的、具有热稳定性和构象稳定性的蛋白质支架,它能够准确地模拟病毒表位结构并诱导中和抗体的产生。
合成疫苗技术可以从序列数据中快速生成疫苗病毒,其研究主要是为了应对未来的世界大流行疾病,如流行性感冒。2013年,Dormitzer等人利用由化学合成的寡核苷酸组装的酶和经过改进的体外错误校正,从而快速、准确地合成两种主要的流感病毒表面糖蛋白(血细胞凝集素和神经氨酸酶)。这种合成方法能够在几天内开发疫苗种子,而传统技术常常需要2~3个月。
(四)来源于微生物和微藻的药物
微生物(如细菌、真菌)和微藻是生物药物的巨大来源,生物药物可以通过发酵过程或从植物生物质中直接提取来生产。来源于微生物和微藻的药物在生物技术制药领域扮演着举足轻重的角色。
1.胞外聚合物 胞外聚合物(extracellular polymeric substance,EPS)是在一定环境条件下,由微生物(主要是细菌)合成并分泌至胞外的生物聚合物,如多糖、蛋白质和核酸等。对微生物而言,EPS的主要功能是保护其免受周围环境的影响,还可以将环境中的营养成分富集,通过胞外酶降解成小分子后吸收到细胞内。而在医药方面,已有研究发现,EPS具有抗肿瘤、抗动脉粥样硬化、免疫调节等重要作用。例如,结冷胶可以作为口服、眼部和鼻腔给药的药物配方,也能作为组织工程材料的成分;黄原胶因其具有缓释药物的能力而在药物递送中得到了广泛应用,其形式有脂质体、水凝胶、类脂囊泡、纳米颗粒、微球等;磷酸化的凝胶多糖微凝胶被应用于体外药物释放,显示出优异的生物相容性;细菌纤维素因其良好的保水能力、适宜的孔隙率、有效的阻隔性能且为纳米纤维材料,被认为是伤口敷料材料的最佳替代品,同时还可以作为赋形剂和药物缓释材料(图1-2)。

图1-2 木醋杆菌(Gluconacetobacter xylinus)产生的细菌纤维素
2.微藻类药物 自20世纪60年代以来,科学家提出了“向海洋要药”的口号,掀起了海洋药物研究的高潮。微藻在海洋中含量丰富,是海洋药物的重要来源,它们能产生许多具有医学应用价值的化合物,如色素、蛋白质、糖类和含有重要脂肪酸的脂质等(表1-6)。
(1)色素:微藻色素毒性低、生物活性好,且具有抗氧化和抗炎活性,可用于预防急性和慢性冠状动脉综合征、动脉粥样硬化、类风湿性关节炎、肌营养不良、白内障和神经障碍等疾病。研究发现,大多数微藻色素对试验大鼠的小脑神经元具有保护作用,并且对体外生长的肝细胞具有保护作用。
(2)蛋白质:微藻蛋白质含量很高,且为优质蛋白质,含有人体所需的全部必需氨基酸,已有研究发现在从螺旋藻中分离得到的别藻蓝蛋白和藻蓝蛋白具有抗病毒和抗真菌活性。
(3)糖类:从微藻中提取的硫酸化多糖被发现具有抗氧化、抗凝血、抗炎、抗病毒、抗菌、抗肿瘤、免疫调节和防辐射等作用。
表1-6 一些来源于微藻的生物活性化合物及其应用
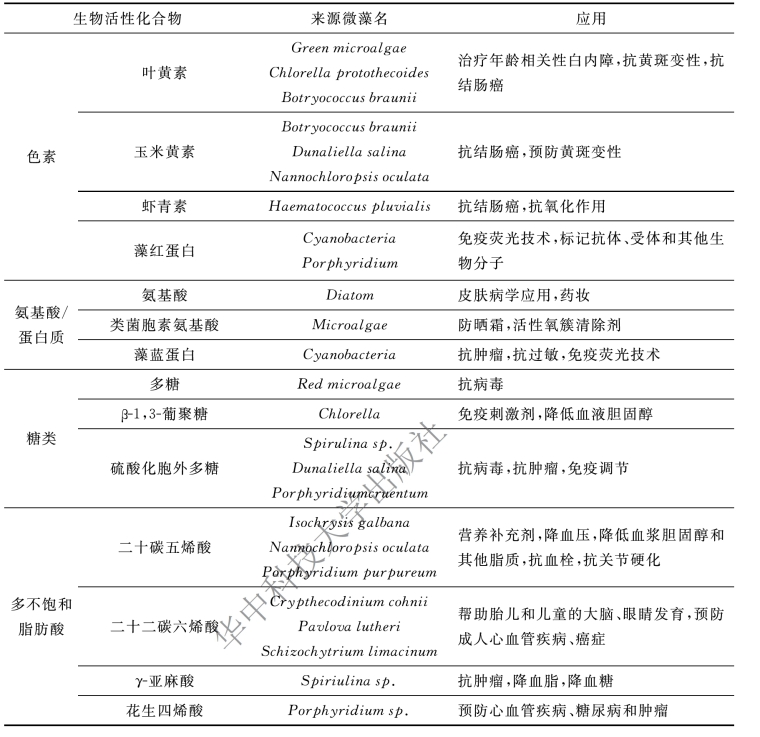
(4)脂质:微藻中的总脂质占比达干重的30%~70%,其重要成分有ω-3族脂肪酸和ω-6族脂肪酸,这两族脂肪酸都属于多不饱和脂肪酸(PUFA),含有人体的必需脂肪酸,必须从食物中获取。ω-3族脂肪酸主要有亚麻酸、二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),摄入EPA和DHA补充剂已被证明可预防心血管、神经系统和炎症性疾病,对于胎儿大脑的健康发育也至关重要。ω-6族脂肪酸主要有亚油酸(LA)和花生四烯酸(ARA),具有抑制和刺激人体细胞免疫反应的作用,可以改善脂质代谢,降低血糖,预防动脉硬化,减少人体脂肪,增强免疫功能。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




