四环素类抗生素包括四环素、金霉素、土霉素、强力霉素(多西环素)等,被广泛应用于畜禽生产中。四环素类药物具有广谱高效的杀菌抗生功效,可以与大多数药物或饲料添加剂混用。此类药物存在使用剂量过大、用药时间过长、滥用等现象,造成其在食品中残留严重。四环素类抗生素已经成为严重危害人类健康的食品安全隐患之一。为此,世界各国对四环素类兽药残留的检测十分关注。我国及欧盟等的相关食品安全法规规定,四环素类兽药在牛奶和肌肉组织中的残留总量不得超过100μg/kg,在蜂蜜中的残留总量应不超过0.05mg/kg;美国药品监督管理局规定,四环素、土霉素、金霉素在动物肌肉组织中的残留总量不超过2μg/g,在牛奶中的限量为300ng/g。
食品中四环素类药物残留量的检测方法有高效液相色谱法、毛细管电泳法、发射受体分析法、酶联免疫法及液相色谱-质谱联用法等。在此介绍《动物源性食品中四环素类兽药残留量检测方法 液相色谱-质谱/质谱法与高效液相色谱法》(GB/T 21317—2007)中的高效液相色谱法。
1.原理
试样中四环素族抗生素残留量用0.1mol/L的Na2 EDTA-Mcllvaine缓冲液(pH=4.0±0.05)提取,经过滤和离心后,上清液用HLB固相萃取柱净化,用高效液相色谱仪测定,用外标法峰面积定量。
2.试剂与仪器
(1)试剂 除另有规定外,所有试剂均为分析纯,试验用水为GB/T 6682—2008规定的一级水。
1)常用试剂:乙腈(高效液相色谱纯)、甲醇(高效液相色谱纯)、乙酸乙酯、乙二胺四乙酸二钠(Na2EDTA·2H2O)、三氟乙酸、柠檬酸(C6H8O7·H2O)、磷酸氢二钠(Na2HPO4·12H2O)。
2)柠檬酸溶液(0.1mol/L):称取21.01g柠檬酸(C6H8O7·H2O),用水溶解,定容至1000mL。
3)磷酸氢二钠溶液(0.2mol/L):称取28.41g磷酸氢二钠(Na2HPO4·12H2O),用水溶解,定容至1000mL。
4)Mcllvaine缓冲溶液:将1000mL 0.1mol/L柠檬酸溶液与625mL0.2mol/L磷酸氢二钠溶液混合,必要时用氢氧化钠或盐酸调节pH=4.0±0.05。
5)0.1mol/L Na2EDTA-Mcllvaine缓冲溶液:称取60.5g乙二胺四乙酸二钠放入1625mL Mcllvaine缓冲溶液中,使其溶解,混匀。
6)(1+19)甲醇-水溶液:量取5mL甲醇与95mL水混合。
7)(1+9)甲醇-乙酸乙酯溶液:量取10mL甲醇与90mL乙酸乙酯混合。
8)Osis HLB固相萃取柱:60mg,3mL,或相当者。使用前分别用5mL甲醇和5mL水预处理,保持柱体湿润。
9)三氟乙酸水溶液(10mmol/L):准确吸取0.765mL三氟乙酸置于1000mL容量瓶中,用水溶解并定容。
10)(1+19)甲醇-三氟乙酸水溶液:量取50mL甲醇与950mL三氟乙酸水溶液混合。
11)标准物质:二甲胺四环素(米诺环素)(CAS:10118-90-8)、土霉素(CAS:6153-64-6)、四环素(CAS:60-54-8)、去甲基金霉素(CAS:127-33-3)、金霉素(CAS:57-62-5)、甲烯土霉素(美他环素)(CAS:914-00-1)、强力霉素(多西环素)(CAS:564-25-0)、差向四环素(CAS:64-75-5)、差向土霉素(CAS:35259-39-3)、差向金霉素(CAS:14297-93-9),纯度均大于或等于95%。
12)标准储备溶液:准确称取按其纯度折算为100%(质量分数)的二甲胺四环素、土霉素、四环素、去甲基金霉素、金霉素、甲烯土霉素、强力霉素、差向四环素、差向土霉素、差向金霉素各10.0mg,分别用甲醇溶解并定容至100mL,质量浓度相当于100mg/L,储备液在-18℃以下储存于棕色瓶中,可稳定12个月以上。
13)混合标准工作溶液:根据需要,用(1+19)甲醇-三氟乙酸水溶液将标准储备溶液配制为适当质量浓度的混合标准工作溶液。混合标准工作溶液应在使用前配制。
(2)仪器 高效液相色谱仪(配二极管阵列检测器或紫外检测器)、分析天平(感量为0.1mg和0.01g)、旋涡混合器、低温离心机(最高转速为5000r/min,控温范围为-40℃至室温)、吹氮浓缩仪、固相萃取真空装置、pH计(精度为±0.02)、组织捣碎机、超声提取仪。
3.样品的制备与储存
在制样操作过程中,应防止样品受污染或残留物含量发生变化。
(1)动物肌肉、肝脏、肾脏和水产品 从所取全部样品中取出约500g,用组织捣碎机充分捣碎,混匀,装入洁净容器中,密封,并标明标记,于-18℃以下冷冻存放。
(2)牛奶样品 从所取全部样品中取出约500g,充分混匀,装入洁净容器中,密封,并标明标记,于-18℃以下冷冻存放。
4.测定步骤
(1)提取(https://www.xing528.com)
1)动物肌肉、肝脏、肾脏和水产品:称取均匀试样5g(精确至0.01g),置于50mL聚丙烯离心管中,分别用约20mL、20mL、10mL浓度为0.1mol/L的Na2EDTA-Mcllvaine缓冲液冰水浴超声提取三次,每次旋涡混合1min,超声提取10min,然后以3000r/min的转速离心5min(温度低于15℃),合并上清液(注意控制总提取液的体积不超过50mL),并定容至50mL,混匀,再以5000r/min的转速离心10min(温度低于15℃),用快速滤纸过滤,待净化。
2)牛奶:称取均匀试样5g(精确至0.01g),置于50mL比色管中,用浓度为0.1mol/L的Na2EDTA-Mcllvaine缓冲液溶解并定容至50mL,旋涡混合1min,冰水浴超声10min,转移至50mL聚丙烯离心管中,冷却至0~4℃,以5000r/min的转速离心10min(温度低于15℃),用快速滤纸过滤,待净化。
(2)净化 准确吸取10mL提取液(相当于1g样品),以1滴/s的速度过HLB固相萃取柱,待样液完全流出后,依次用5mL水和5mL(1+19)甲醇-水溶液淋洗,弃去全部流出液,在2.0kPa以下减压抽干5min,最后用10mL(1+9)甲醇-乙酸乙酯溶液洗脱。将洗脱液吹氮浓缩至干(温度低于40℃),用0.5mL(1+19)甲醇-三氟乙酸溶液溶解残渣,过0.45μm滤膜,待测定。
(3)测定
1)高效液相色谱检测样品的参考条件
①色谱柱:Incrtsil C8柱,长度为250mm,内径为4.6mm,粒度为3.5μm,或相当者。
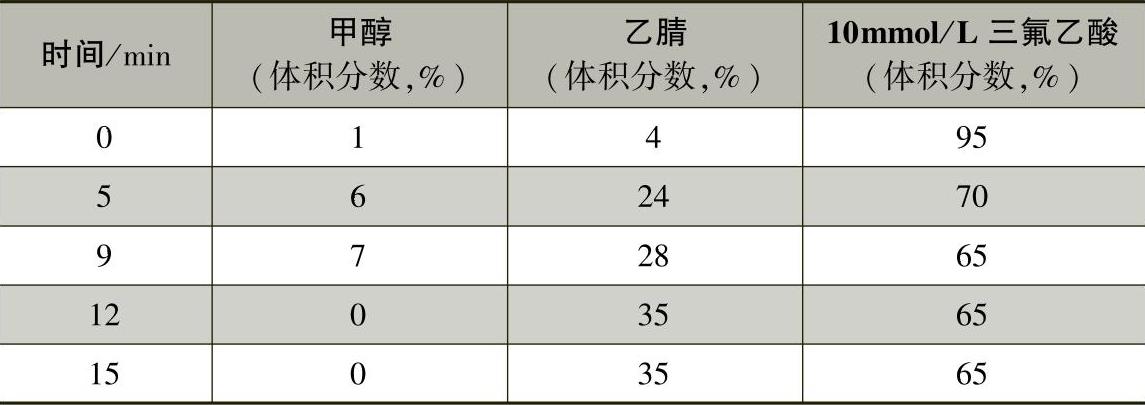
②流动相:甲醇+乙腈+10mmol/L三氟乙酸水溶液,梯度洗脱参数见表7-7-4(柱平衡时间为5min)。
③流速:1.5mL/min。
④柱温:30℃。
⑤检测波长:350nm。
⑥进样量:100μL。
表7-7-4 分离7种四环素类药物的液相色谱流动相梯度洗脱参数
2)测定:根据样液中被测四环素类兽药残留的含量情况,选定峰高相近的标准工作溶液。标准工作溶液和样液中四环素类兽药残留的响应值均应在仪器的检测线性范围内。对标准工作溶液和样液等体积参插进样测定。
5.空白试验
除不加试样外,均按上述测定步骤进行。
6.结果计算
采用外标法定量,按式(7-7-9)计算四环素类兽药残留量。

式中 X——样品中待测组分残留量(μg/kg);
cs——待测组分标准工作液的质量浓度(μg/L);
Ax——测定液中待测组分的峰面积;
As——标准工作液中待测组分的峰面积;
V——样液最终定容体积(mL);
m——最终样液所代表的试样量(g)。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




