1.分离条件选择的指标
(1)分离度 根据塔板理论,有效理论塔板数是衡量柱效能的指标,但柱效能仅能说明柱子的分离效率问题,并不能说明分离效果;而固定相的选择性又只能说明分离效果,并不能说明分离效率问题。为了评价色谱柱分离效果,提出了“分离度”的概念。分离度就是色谱柱总的分离效能的指标。所谓分离度是指同一样品中相邻两组分保留值之差与其峰底宽度(Y)的算术平均值之比。
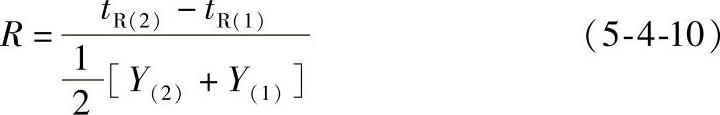
式中 tR(2)和tR(1)——分别为两组分的保留时间;
Y(1)和Y(2)——与保留值具有相同单位的相应组分峰的峰底宽度。
显然,相邻两组分保留值差别越大、平均峰底宽度越小,则R值越大,意味着相邻两组分分离得越好。
理论证明,若峰形对称且满足于正态分布,则当R=1时,分离程度可达98%,即两峰稍有交盖;当R=1.5时,分离程度可达99.7%。因此,可用R=1.5来作为相邻两峰完全分开的标志。
当两组分的色谱峰有交盖、峰形不对称时,峰底宽度难于测量,此时可用半峰宽代替峰底宽度,由式(5-4-11)计算分离度。
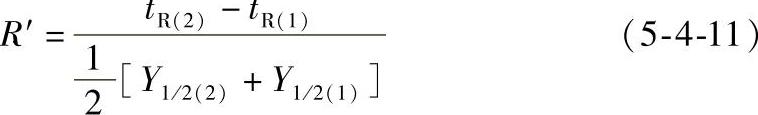
应当指出,R′与R的物理意义是一致的,但数值不同(R=0.59R′),应用时要注意根据具体情况采用相应的分离度计算方法。
总之,分离度概括了实现组分分离的热力学因素(峰间距)及动力学因素(峰宽),定量描述了样品中相邻两组分实际分离的程度,因此可作为色谱柱总的分离效能指标。
(2)色谱分离基本方程式 由于多组分混合物样品中各个组分之间性质上的差异是不同的,而其中性质差异最小的是难分离物质对,因此利用色谱分析解决多组分混合物的分离分析问题,在选择合适的固定相及色谱操作条件时,主要针对其中的难分离物质来进行。对于难分离物质对,由于它们的保留值差别小,因此可合理地认为Y(1)=Y(2)=Y,k1≈k2=k。依据塔板数n、分离度R与保留值及区域宽度之间的关系,可以得到色谱分离的基本关系式。
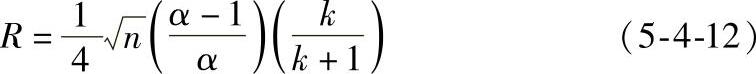
式(5-4-12)将分离度R与体系的热力学性质α和k、塔板数n之间联系在了一起,用有效理论塔板数表示为
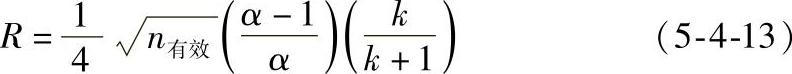
式中 R——分离度;
n或n有效——理论塔板数或有效理论塔板数;
k——容量因子;
α——选择因子。
式(5-4-13)表明:
1)分离度R与n的平方根成正比。当固定相确定时,分离度的大小将由n决定。由于柱长L与n成正比,显然增加柱长可改进分离度,但增加柱长也增加了各组分的保留时间,延长了分析周期并致峰扩张。因此,在保证一定的分离度条件下,应尽量使用短一些的色谱柱。
2)分离度R正比于容量因子k。显然,k大对分离有利,但也并非k越大越好。k的最佳取值范围是1<k<10。在这个范围内,既可获得组分的理想分离,又可保证分析周期不致过长,峰的扩展也不会太严重而影响检测。另外,改变柱温和改变相比均可以改变k。因此,采用细颗粒固定相,填充得紧密而均匀,可降低色谱柱死体积而使分离度提高。
3)α(选择因子)是色谱柱选择性的量度,其值越大,色谱柱的选择性越好,分离效果也越好。在实际工作中,可由一定的α值和所要求的分离度,计算色谱柱所需的有效理论塔板数。因此,增大α值是提高分离度的有效办法。增加α最为简便而有效的方法是改变固定相,使各组分的分配系数有较大差别。
由于分离度总括了实现组分分离的热力学和动力学两方面因素,因此分离度、柱效能和选择性参数三者之间的关系可用数学式表达为

2.色谱分离条件的选择
(1)载气及其流速的选择 一定的色谱柱和试样,有一个最佳的载气流速,此时柱效能最高。根据式(5-4-9),于不同的载气流速下测得的塔板高度H对载气流速u作图,结果如图5-4-7所示。在曲线的最低点,塔板高度H最小(记为H最小),柱效能最高,对应的载气流速即为最佳载气流速(记为u最佳)。因此有
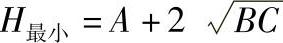
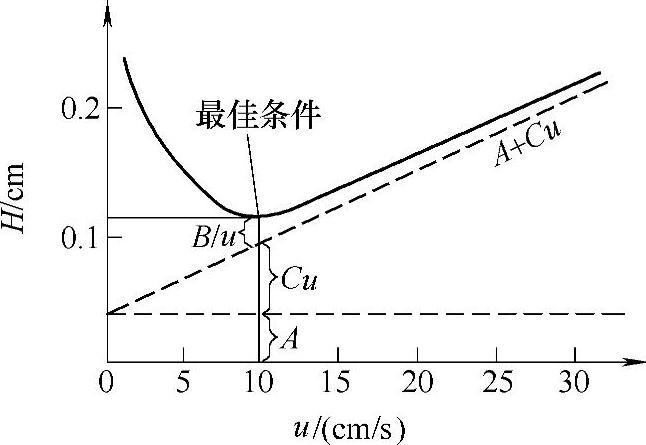
图5-4-7 H-u关系曲线
在实际工作中,为了缩短分析时间,往往使载气流速稍高于最佳流速。
从以上讨论可知,当载气流速较大时,传质阻力项Cu为色谱峰扩张的主要因素,在这种情况下,宜采用相对分子质量较小的载气(H2、He),此时组分在载气中有较大的扩散系数,可减小气相传质阻力,提高柱效能;而当载气流速较小时,分子扩散项B/μ成为控制因素,此时应采用相对分子质量较大的载气(N2,Ar),使组分在载气中有较小的扩散系数。选择载气时还应考虑与检测器的匹配。
(2)柱温的选择 柱温直接影响分离效能和分析速度。柱温对组分分离的影响较大。较高的柱温可减小传质阻力,提高柱效能,但易致各组分挥发靠拢,不利于分离,同时柱温高还会使固定液挥发流失。柱温低有利于分配和组分分离,但柱温过低,被测组分可能在色谱柱中冷凝,或者传质阻力增加,使色谱峰扩张,甚至拖尾。一般通过试验选择最佳柱温。所以选择柱温的原则是:以使难分离物质对达到理想的分离效果、峰形正常、分析周期长短适中为前提,尽可能采用较低的柱温,但以保留时间适宜、峰形不拖尾为度。在实际工作中一般根据样品沸点来选择柱温。
另外还需要考虑样品的沸点范围。分离各类组分的柱温具体应根据实际情况而定,一般应接近被分离组分的平均沸点。对于沸点较低(100~200℃)的混合物,柱温可选在其平均沸点2/3左右;对于高沸点(300~400℃)的混合物,希望在较低的柱温(低于其沸点100~200℃)下分析;对于沸点居中的混合物(200~300℃),可在中等柱温下操作,柱温比其平均沸点低100℃。
对于沸点范围较宽的试样,用恒定柱温往往造成低沸点组分分离不好,高沸点组分峰形扁平,因此宜采用程序升温,即柱温按预定的加热速度,随时间做线性或非线性的变化,可改善复杂组分的分离效果,使低沸点及高沸点组分都能在各自适宜的温度下得到良好的分离。其优点是能缩短分析周期,改善峰形,提高检测灵敏度,但有时会引起基线漂移。
(3)进样时间和进样量的选择 色谱法要求进样速度必须很快,以防人为造成色谱峰原始宽度变大,峰扩张更加严重,甚至峰变形,因而要求采用注射器或进样阀进样时,进样都在1s以内完成。
色谱分析法的进样量一般都是比较少的,如液体试样一般进样0.1~5μL,气体试样进样0.1~10mL。这是因为进样量过多,会造成分离不理想,如使组分出峰的时间差变小而形成叠峰。但进样量太少,又会使含量少的组分因检测器检测灵敏度低而检测不出来,即不出峰。通常最大允许的进样量,应控制在峰面积或峰高与进样量呈正比的范围内。
(4)汽化温度的选择 液体样品进样后首先经汽化室瞬间汽化,再继续随流动相进入色谱柱实现分离。故汽化室温度应足够高,应以试样能被迅速汽化而又不分解为宜。一般选择汽化温度要比柱温高20~70℃。适当地提高汽化温度对分离及定量有利,尤其当进样量比较大时更是如此。
(5)固定相及其选择 在气相色谱分析中,某一多组分混合物中各组分能否完全分离,主要取决于色谱柱的效能和选择性。后者在很大程度上取决于固定相选择得是否适当,因此选择适当的固定相就成为色谱分析中的关键问题。气相色谱固定相分为气-液色谱固定相和气-固色谱固定相。
1)气-液色谱固定相。这类固定相是由起支撑作用的担体和起分离作用的固定液两个部分构成。
①担体:也叫载体,其性能直接影响固定液涂渍的均匀性,进而影响色谱柱的分离效能。担体应是一种化学惰性、多孔性的固体颗粒,能提供一个大的惰性表面,用以承担固定液,使固定液以薄膜状态分布在其表面上。担体应具备的条件是:
a.表面应是化学惰性的,即表面没有吸附性或吸附性很弱,更不能与被测物质起化学反应。
b.多孔性,即比表面积较大(以利与试样的充分接触),孔径分布均匀(以利于形成薄而均匀的固定液液膜)。
c.对热稳定性好,有一定的机械强度。
d.颗粒大小均匀,从而保证色谱柱填充均匀,减小涡流扩散项的数值。一般希望颗粒均匀、细小,以利于提高柱效能。但颗粒过细,会使柱压降增大,对操作不利。一般内径为4~6mm的色谱柱选用40~60目、60~80目或80~100目的颗粒均可。
气-液色谱中所用担体可分为硅藻土型和非硅藻土型两类,常用的是硅藻土型担体。因处理方法不同,硅藻土担体可分为红色担体和白色担体两种。这两种硅藻土担体的化学组成和内部结构基本相似,但它们的表面结构却不相同。红色担体一般适用于分析非极性或弱极性物质,白色担体一般用于分析极性物质。另外,担体需进行钝化处理,以改进担体孔隙结构,屏蔽活性中心,提高柱效能。钝化处理方法有酸洗、碱洗、硅烷化等。
②固定液:在气-液色谱中真正起分离作用的并非担体而是固定液,因此固定液的选择就显得十分重要。用于气相色谱的固定液已有上千种,为选择和使用方便,一般按极性大小把固定液分为四类,即非极性、中等极性、强极性和氢键型固定液。
a.对固定液的要求
• 挥发性要小,热稳定性要高,否则易被载气带走或发生热分解而流失。
• 化学稳定性好,不与被测组分或载气发生化学反应。
• 具有高度的选择性,即对沸点、极性或结构最相近的物质具有不同的溶解能力,以利于分离。
• 具有足够的溶解能力,否则分配系数太小,各组分还来不及分离就流出色谱柱。
• 黏度适中,便于涂渍均匀。
b.固定液的选择。固定液的选择一般根据“相似相溶”原理,即固定液的性质和被测组分有某些相似性时,其溶解度相对就大。常用“极性”来说明固定液和被测组分的性质。固定液的选择方法为:
• 分离非极性物质时,一般选用非极性固定液,这时试样中各组分按沸点次序先后流出色谱柱,沸点低的先出峰,沸点高的后出峰。
• 分离极性物质时,选用极性固定液,这时试样中各组分主要按极性顺序分离,极性小的先流出色谱柱,极性大的后流出色谱柱。
• 中等极性组分可首选中等极性固定液,基本上仍按沸点顺序出柱。但对沸点相同的极性与非极性组分来说,诱导力起主导作用,极性组分后出柱。
• 分离非极性和极性混合物时,一般选用极性固定液,这时非极性组分先流出,极性组分(或易被极化的组分)后流出。
• 对于能形成氢键的组分(如醇、酚、胺和水等的分离),一般选择极性的或氢键型的固定液,这时试样中各组分按与固定液分子间形成氢键的能力大小先后流出,不易形成氢键的先流出,最易形成氢键的后流出。
2)气-固色谱固定相。在分离常温下的气体及气态烃类时,气体在一般固定液中的溶解度小,常采用吸附剂作固定相,利用其对气体的吸附性能常有差异的特点,可获得满意的分离效果。
在气-固色谱法中作固定相的吸附剂,常用的有非极性的活性炭、弱极性的氧化铝和氢键型硅胶。它们对各种气体吸附能力的强弱不同,因而可根据分析对象选用。由于吸附剂种类不多,不是同批制备的吸附剂的性能往往不易重复,并且进样量稍多时色谱峰就会不对称,有拖尾现象等。后来用表面结构均匀的吸附剂分子筛(如碳分子筛等)、高分子的多孔微球等作固定相,不但使极性化合物的色谱峰不拖尾,而且可以成功地分离一些顺、反式空间异构体。
3.定性分析(https://www.xing528.com)
色谱定性分析常采用将样品和标准品对照的方式,根据同一种物质在同一根色谱柱上和相同的色谱条件下保留值相同的原理进行定性,将保留值作为定性分析的指标,如图5-4-8所示。
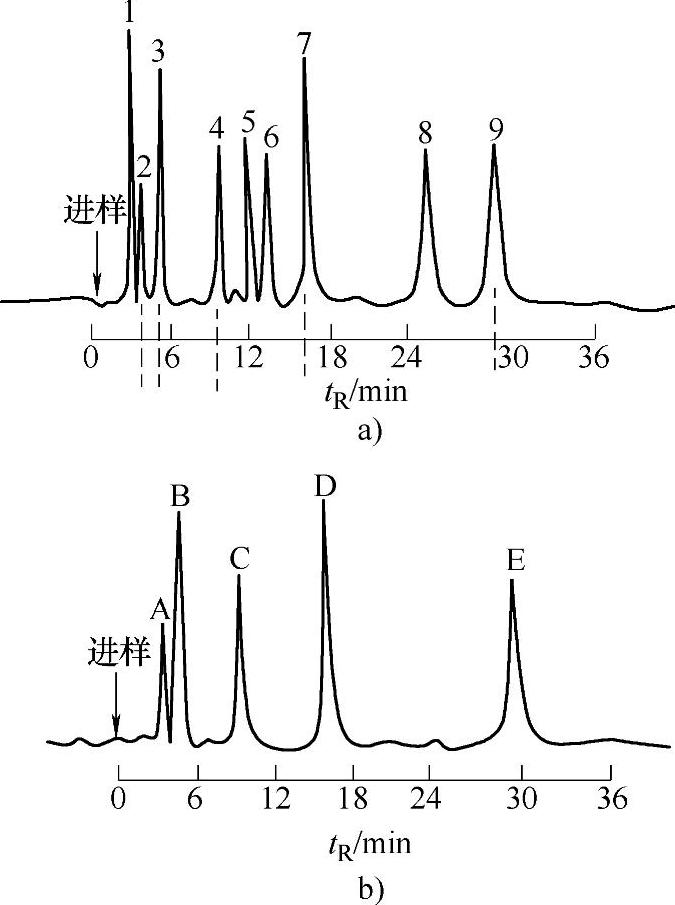
图5-4-8 以标准物直接对照进行定性分析示意图
a)未知物 b)标准物
注:峰上的数字代表出峰顺序;标准物A为甲醇,B为乙醇,C为正丙醇,D为正丁醇,E为正戊醇。
(1)利用相对保留值定性 利用绝对保留值定性时,必须严格控制色谱条件的一致性,其可靠性与色谱柱的分离效率有密切关系。由于分配系数K只取决于组分的性质、柱温与固定液的性质,而与固定液的用量、柱长、载气流速及柱填充情况等无关。因此,当载气流速和温度发生微小变化时,被测组分与参比组分的保留时间同时发生变化,而它们的比值——相对保留值则不变,可作为定性较可靠的参数。
(2)利用加入标准品增加峰高的方法定性 当试样中所含组分种类复杂,由于保留值相近而使色谱峰难以确认时,将适量的标准品加入样品中,混匀,进样,对比加入前后的色谱图,若加入后某色谱峰相对增高,则该色谱组分与已知标准物质可能为同一物质。
(3)利用文献值对照进行定性 在无法获得标准品时,可利用文献值对照定性,即利用标准品的文献保留值(相对保留值或保留指数)与未知物的测定保留值进行比较对照来进行定性分析。
保留指数又称为科瓦茨指数,是一种重现性较其他保留参数都好的且较为可靠的定性参数。保留指数是将待测组分的保留行为用两种与之相邻的基准物(通常是选用正构烷烃)进行标定而得到的,即某待测组分的保留指数是在一定条件下,用两种与之相邻的正构烷烃作参比,进行调整保留值的测定而得到的。这种方法可根据所用固定相和在一定柱温条件下测得的待测组分的保留指数直接与文献值对照定性,而不需要标准试样。
(4)联机定性 气相色谱的分离效率很高,但仅用色谱数据定性却很困难。通常称为“四大谱”的质谱法、红外光谱法、紫外光谱法和核磁共振波谱法对单一组分(纯物质)的有机化合物具有很强的定性能力。因此,将色谱分析与这些色谱法所用仪器联用,能很好地解决组成复杂的混合物的定性分析问题。
联用方法一般有两种:一种方法是将色谱分离后需要进行定性分析的某些组分分别收集起来,然后再用上述“四大谱”的方法或其他的定性分析方法进行分析;另一种方法是将色谱与上述几种色谱方法所用仪器直接连接起来,组成联用仪,可以同时得到样品的定性和定量结果。
4.定量分析
(1)定量分析依据 前已述及,在一定的色谱操作条件下,组分i的质量(mi)或其在载气中的浓度与检测器的响应信号(色谱图上表现为峰面积Ai或峰高hi)成正比,可写为
mi=fiAi (5-4-15)
式中 fi——定量校正因子;
mi——组分i的质量;
Ai——组分i峰面积。
这就是色谱定量分析的依据。可见,在色谱定量分析中,为使结果准确可靠,就需要准确测量检测器的响应信号峰面积A(或峰高h),准确测定定量校正因子以及选用适宜的定量计算方法等。
(2)定量校正因子 色谱定量分析基于被测物质的量与其峰面积(或峰高)成正比例关系。但是由于同一检测器对不同的物质具有不同的响应值,以致相同量的两种物质的色谱峰峰面积往往不相等,这样就不能用峰面积来直接计算物质的含量。为了使检测器产生的响应信号能真实地反映出物质的含量,就要对响应值进行校正,因此引入“定量校正因子”。
式(5-4-15)中的fi为绝对定(质)量校正因子,也就是单位峰面积所代表的物质的质量。它主要由仪器的灵敏度所决定,既不易准确测定,也无法直接应用。所以在色谱定量分析工作中,都是采用相对定量校正因子f′is,即某物质的绝对定量校正因子fi与某一标准物质s的绝对定量校正因子fs之比。平常所指的或由文献查得的定量校正因子均为物质的相对定量校正因子。用来测量相对定量校正因子的标准物质因检测器的不同而有所区别,如热导池检测器常采用苯,氢火焰离子化检测器常采用正庚烷。按被测组分使用的计量单位的不同,定量校正因子又有相对质量校正因子f′m、相对摩尔校正因子f′M和相对体积校正因子f′V(通常把“相对”二字略去)之分。
应当注意,相对定量校正因子是无因次的量,但其数值却与所用单位有关。依进入检测器的组分的量的单位不同(可以是g、mol或L),相对定量校正因子又有相对质量定量校正因子、相对摩尔定量校正因子和相对体积定量校正因子之分。其中,相对质量定量校正因子最常用。再者,除可采用色谱峰的峰面积定量外,还可采用峰高定量,所以相对定量校正因子又有峰面积相对定量校正因子fAis和峰高相对定量校正因子fhis之分。其中,峰面积相对定量校正因子较常用,且不加注明时均表示峰面积相对定量校正因子,使用时应注意其与所用参量的一致性。相对定量校正因子的数值可由文献中查到,但引用文献值时应保证试验条件与文献的一致性,以免得出错误的计算结果。
(3)相对应答值Sis 相对应答值也叫相对响应值。它是待测组分i的绝对响应值(绝对灵敏度)与作为基准标准物质s的绝对响应值(绝对灵敏度)之比。单位相同时,Sis与相对定量校正因子f′is互为倒数关系,即:
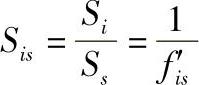
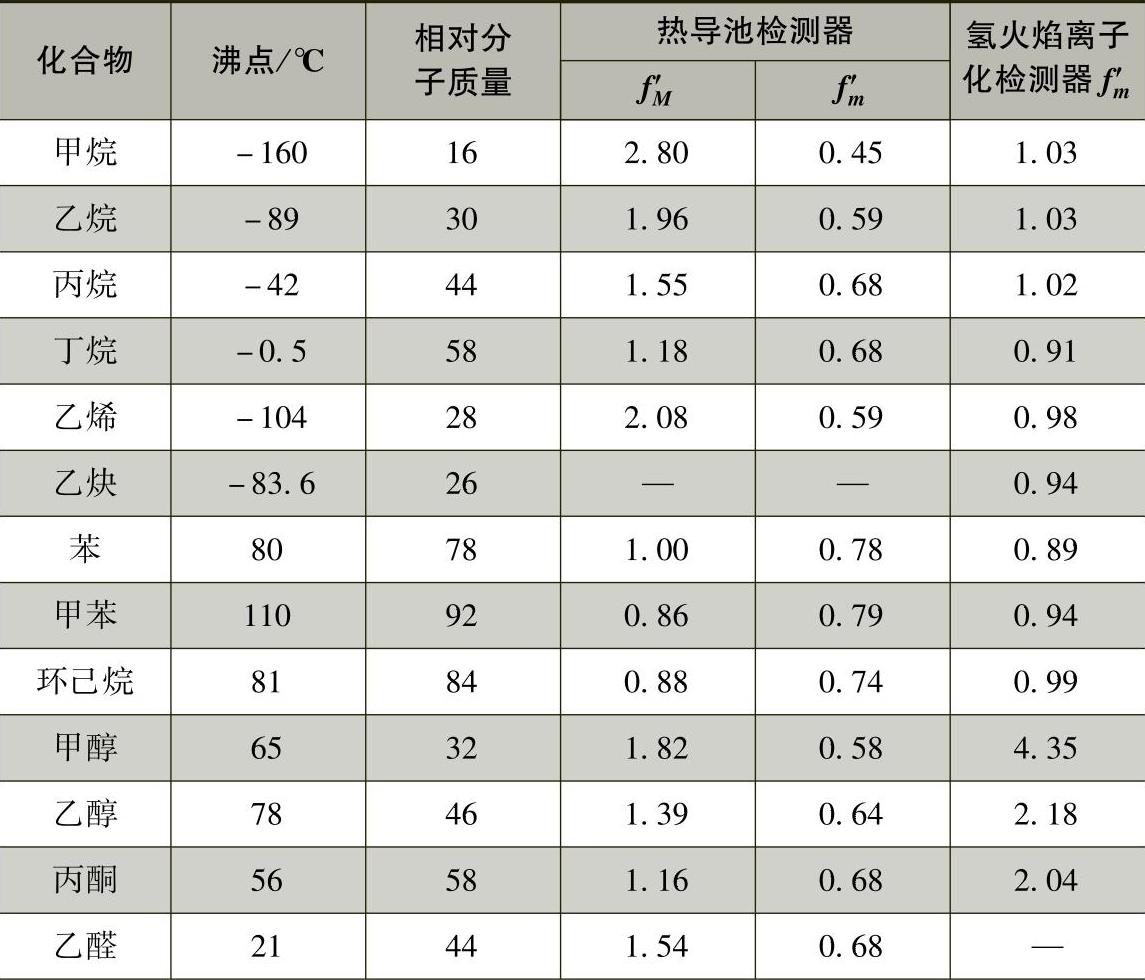
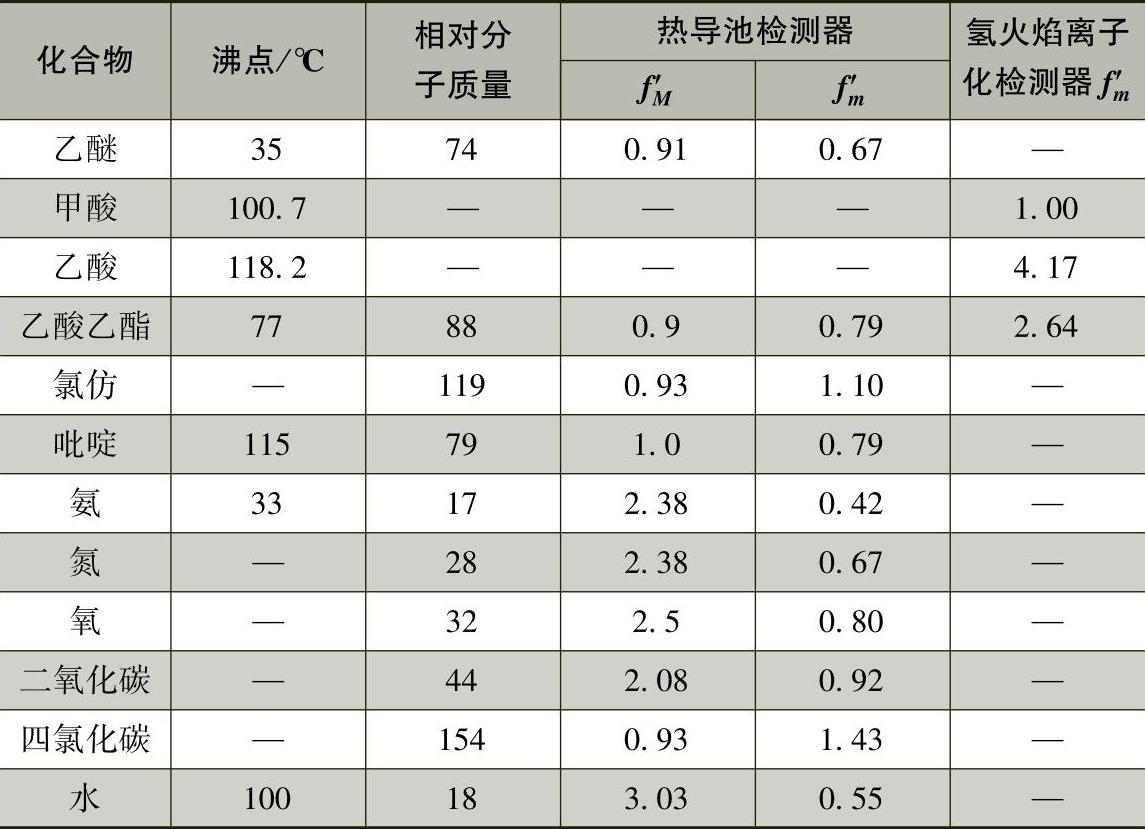
Sis和f′is只与试样、标准物质以及检测器类型有关,而与操作条件和柱温、载气流速、固定液性质等无关,因而是一个能通用的常数。表5-4-3给出了一些物质的相对定量校正因子(未加注明时均表示面积相对定量校正因子)。
表5-4-3 一些物质的相对定量校正因子
(续)
校正因子的测定方法是:准确称量被测组分和标准物质,混合后,在试验条件下进样分析(注意进样量应在线性范围之内),由所得色谱图分别测量它们各自的峰面积,然后根据公式计算相对定量校正因子。如果数次测量的结果接近,则可取其平均值。
(4)几种常用的定量计算方法
1)归一化法。若将所有出峰组分的含量之和按100%计,则这种定量计算的方法就叫做归一化法。只有当试样中所有组分均能出峰时,才可用此方法进行定量计算。
假设试样中有n个组分,每个组分的质量分别为m1,m2,…,mn,这n个组分的含量之和m为100%,其中组分i的质量分数wi可按式(5-4-16)计算。
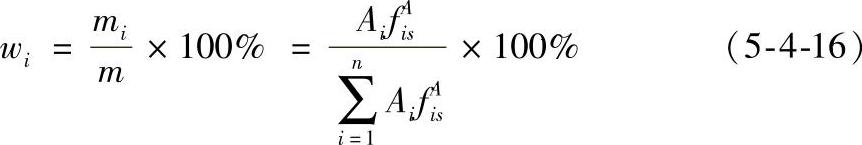
式中 fAis——组分i的相对质量校正因子;
Ai——组分i的峰面积;
mi——组分i的质量(g);
m——各组分质量总和(g)。
对于狭窄的色谱峰,也可用峰高代替峰面积来进行定量测定。当各种操作条件保持严格不变时,在一定的进样量范围内,峰的半宽度是不变的,因此峰高就直接代表某一组分的量,即:
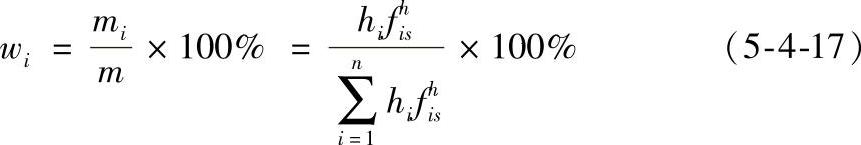
这种方法快速简便,最适合于工厂和一些具有固定分析任务的化验室使用。此时,式(5-4-17)中的fhis为峰高相对定量校正因子,此值需自行测定,测定方法同峰面积校正因子,不同的只是用峰高来代替峰面积。
若各组分的f值相近或相同(如同系物中沸点相近的各个组分),则式(5-4-17)可进一步简化为
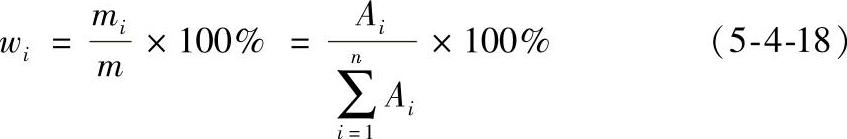
归一化法的优点是简便、准确,当操作条件(如进样量、流速等)变化时,对分析结果的影响比较小。
2)内标法。当试样中所有组分不能全部出峰而需测定的组分出峰时,可采用这种方法。所谓内标法是将一定量的纯物质作内标物,加入到准确称取的试样中去,根据被测物和内标物的质量及其在色谱图上相应的峰面积的比,求出待测组分的含量。例如,要测定试样中组分i(质量为mi)的质量分数wi,可事先向质量为m的试样中加入质量为ms的内标物,则

式中 mi——组分i的质量(g);
ms——内标物的质量(g);
fi——组分i的相对质量校正因子;
fs——内标物的相对质量校正因子;
Ai——组分i的峰面积;
As——内标物的峰面积。
在分析工作中,常以内标物为基准,则fs=1,此时计算公式为
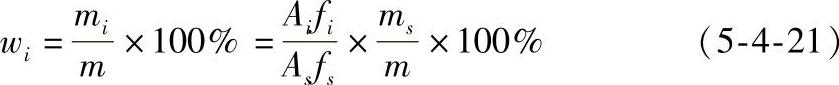
可简化为
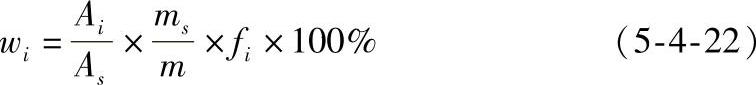
可见,内标法是通过测量内标物及待测组分的峰面积的相对值来进行计算的,因而由操作条件变化所引起的误差,都将同时反映在内标物及待测组分上而被相互抵消,所以可得到较为准确的分析结果。这一内标法的主要优点,已在很多仪器分析方法上得到应用。
显然,在内标法中内标物的选择是至关重要的。它应该是试样中不存在的纯物质,加入的量应接近于被测组分的含量,同时要求内标物的色谱峰位于被测组分色谱峰附近,或几个被测组分色谱峰的中间,并且与这些组分的组分峰完全分离,还应注意内标物与待测组分的物理及物理化学性质(如挥发度、化学结构、极性以及溶解度等)应相近,以便操作条件发生变化时,内标物与待测组分作匀称的变化。
内标法的优点在于定量较准确,而且不像归一化法那样有使用上的限制,但每次分析都要准确称取试样和内标物的质量,因而不适于生产中进行快速控制分析。
3)外标法(又称为定量进样-标准曲线法)。所谓外标法就是单独应用待测组分的纯物质来制作标准曲线的方法。这与分光光度分析中的标准曲线法是相同的。此时用待测组分的纯物质加稀释剂(液体试样用溶剂稀释,气体试样用载气或空气稀释),配成不同质量分数的标准系列溶液,依次取固定量的标准系列溶液进样分析,从所得色谱图上测出响应信号(峰面积或峰高等),绘制响应信号(纵坐标)对质量分数(横坐标)的标准曲线,然后取和制作标准曲线时同量的试样(固定量进样),进样后由所得色谱图测得该试样中待测组分的响应信号,带入标准曲线中查出其对应的质量分数。
此方法的优点是操作简单,计算方便,但结果的准确度主要取决于进样量的重现性和操作条件的稳定性。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




