指示剂是化学试剂中的一种,用于滴定分析中确定或指示滴定终点和环境检测中检验有害物。其基本应用原理是:在一定介质条件下,其颜色能发生变化,能产生混浊或沉淀以及有荧光现象等,利用这些现象起到指示作用。指示剂一般分为酸碱指示剂、氧化还原指示剂、金属指示剂、吸附指示剂等。
在各类滴定过程中,随着滴定剂的加入,被滴定物质和滴定剂的浓度都在不断变化,在计量点附近,离子浓度会发生较大变化。能够对这种离子浓度变化作出显示(如改变溶液颜色,生成沉淀等)的试剂就叫指示剂。
1.酸碱指示剂
酸碱指示剂一般是有机弱酸或弱碱,其酸式体及碱式体有不同的颜色。当溶液的pH值改变时,指示剂由于结构的改变而发生颜色的改变,依此指示终点变化。例如,酚酞是一种有机弱酸,当pH值渐渐升高时,酚酞先失去质子H,由酸式结构转化为碱式结构,颜色由无色变为红色;反之,由红色变为无色
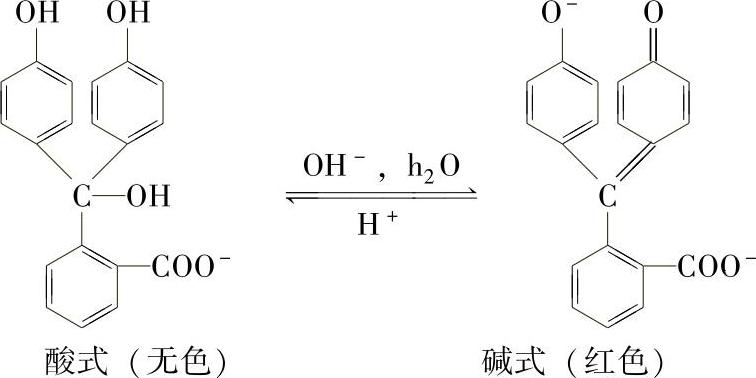
甲基橙是一种有机弱碱,变色反应如下:
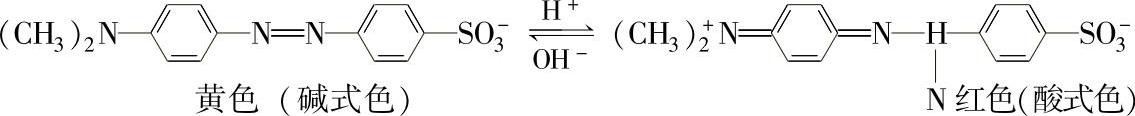
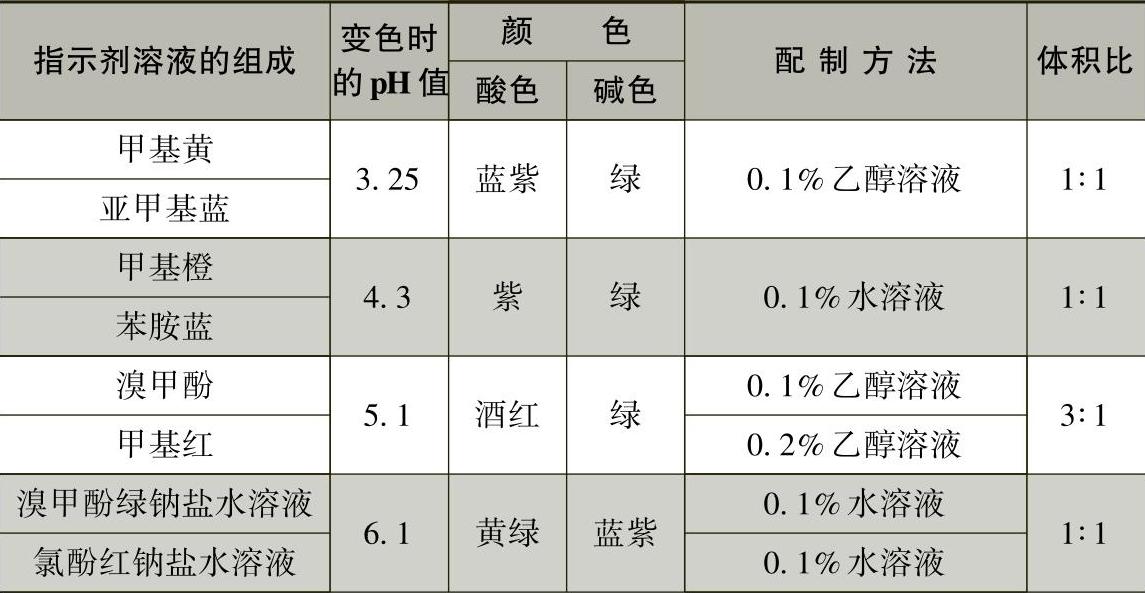
增大溶液的酸度,甲基橙主要以醌式结构存在,溶液呈红色;降低溶液的酸度,甲基橙主要以偶氮式结构存在,溶液呈黄色。常见指示剂及变色范围见表1-5-5。
表1-5-5 常见指示剂及变色范围

注:表中百分含量均为体积分数。
2.混合指示剂
某些酸碱滴定中pH值变化范围很窄,使用一般指示剂难以判断终点,此时可采用混合指示剂。混合指示剂是利用颜色的互补原理,使终点颜色变化敏锐,有两种配制方法:
(1)将两种或两种以上的指示剂混合 例如,甲基红与溴甲酚绿按一定的比例混合,颜色变化如下:

(2)在某种指示剂中加入一种不随溶液中H+浓度变化而改变颜色的惰性染料

由于颜色互补使变色间隔变窄,变色敏锐。几种常用的混合指示剂见表1-5-6。
表1-5-6 几种常用的混合指示剂
(续)

注:表中的百分含量均为体积分数。
3.氧化还原指示剂(https://www.xing528.com)
氧化还原指示剂是本身具有氧化还原性质的有机化合物,在氧化还原滴定过程中能发生氧化反应。它的氧化型和还原型具有不同的颜色,因此可指示氧化还原滴定终点。
现以Ox和Red分别表示指示剂的氧化型和还原型,其氧化还原半反应如下:

根据能斯特公式得:
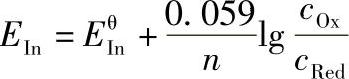
EθIn为指示剂的条件电极电势。随着滴定体系电势的改变,指示剂氧化型和还原型的浓度比也发生变化,从而使溶液的颜色发生变化。与酸碱指示剂的变化情况相似,氧化还原指示剂变色的电势范围为
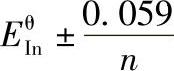
当用K2Cr2O7溶液滴定Fe2+时,以二苯胺磺酸钠为指示剂,滴定到化学计量点时,稍微过量的K2Cr2O7溶液就使二苯胺磺酸钠由无色的还原型氧化为紫红色的氧化型,以指示终点的到达。一些重要的氧化还原指示剂的条件电极电势及颜色变化见表1-5-7。
表1-5-7 一些重要的氧化还原指示剂的条件电极电势及颜色变化
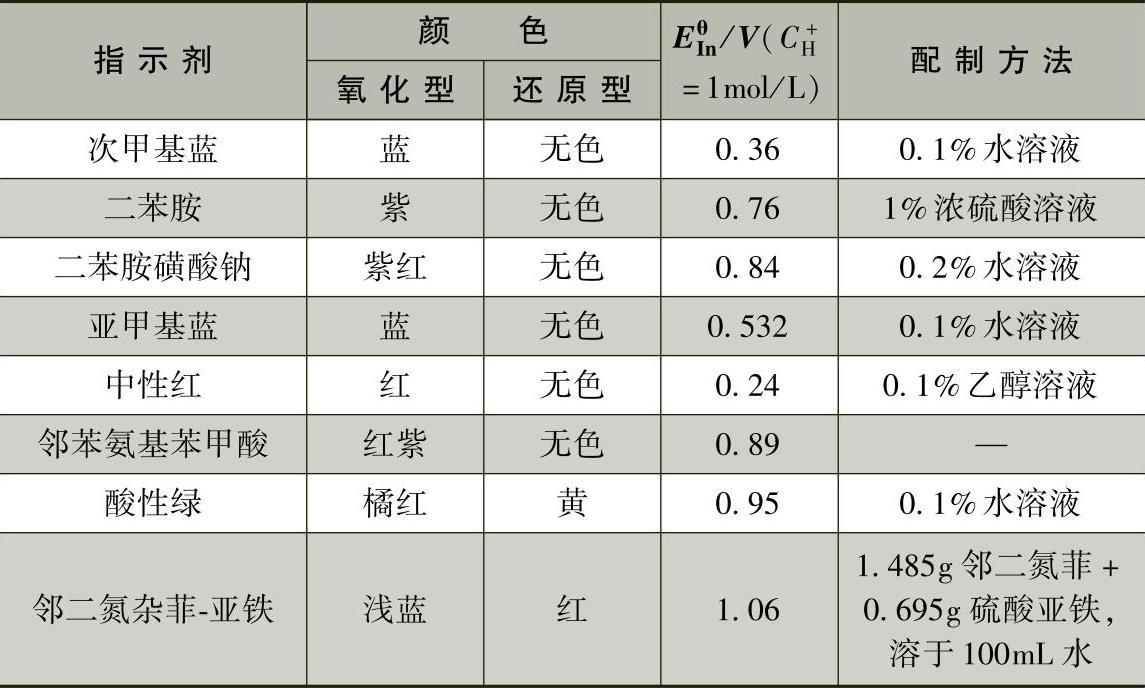
4.金属指示剂
金属指示剂是一种有机染料,也是一种配位剂,能与某些金属离子反应,生成与其本身颜色显著不同的配位化合物以指示终点。常用的金属指示剂见表1-5-8。
表1-5-8 常用的金属指示剂

(续)
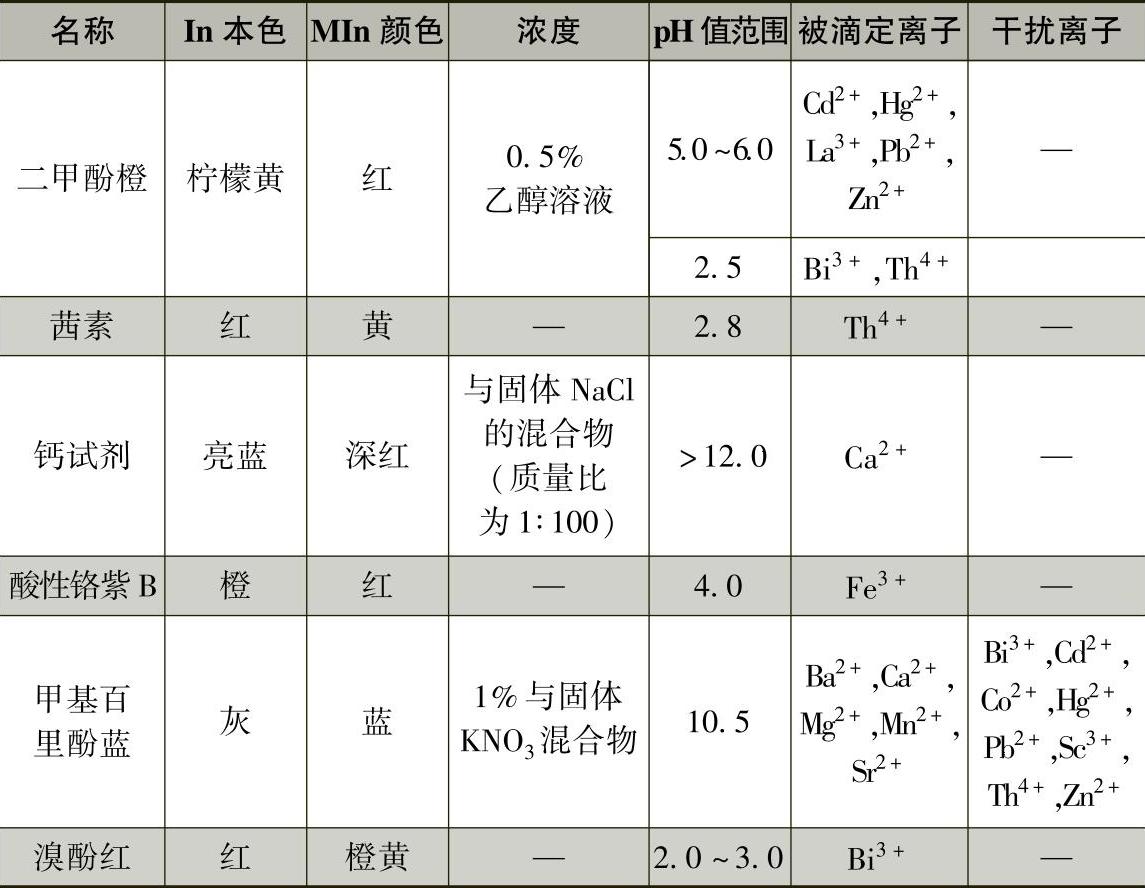
注:表中百分含量为体积分数。
5.吸附指示剂
吸附指示剂是一类有机染料,用于沉淀法滴定。当它被吸附在胶粒表面时,由于形成了某种化合物而导致指示剂分子结构的变化,从而引起颜色的变化。在沉淀滴定中,可以利用它的此种性质来指示滴定的终点。吸附指示剂可分为两大类:一类是酸性染料,如荧光黄及其衍生物,它们是有机弱酸,能解离出指示剂阴离子;另一类是碱性染料,如甲基紫等,它们是有机弱碱,能解离出指示剂阳离子。几种常用的吸附指示剂见表1-5-9。
表1-5-9 几种常用的吸附指示剂

(续)

免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




