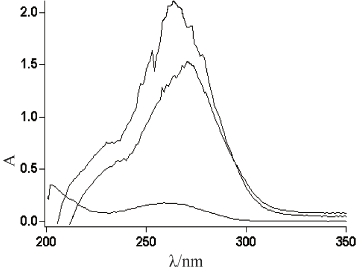
图3.2.1为9.18×10-4mol/L[Cu(phendione)(DAP)]2+与3.03×10-5mol/L dsDNA在0.02 mol/L pH 7.4 Tris-HCl相互作用的紫外光谱图,由曲线a和c可知单纯的铜配合物和DNA在265 nm 处和260 nm 处各有一个最大特征吸收峰,前者归属于配合物中配体间的π→π*跃迁;而后者为DNA的特征吸收峰。考察二者相互作用时,由于它们的特征吸收峰较近,为避免互相产生干扰,我们以相同量的dsDNA溶液为空白,扫描后得到二者混合液充分反应后的紫外吸收光谱曲线,如图3.2.1b所示。由图可以看到,与dsDNA反应后,配合物的特征吸收峰出现明显的降低,减色率为39.1%,表明二者发生了相互作用,这可能是配合物配体的π*空轨道与碱基的π电子轨道发生偶合,偶合后的π*轨道因部分填充电子,使π→π*跃迁几率减少,从而导致吸收峰的降低,同时,在295 nm处出现一个等吸收点证实了二者之间的相互作用,生成了新的复合物。另外,与dsDNA作用后除了特征吸收峰的减色效应,配合物在265 nm的吸收峰位置还红移了-7 nm,表明二者的结合模式可能为嵌插作用[136],该结果得到了下面荧光光谱实验的证实。
 (https://www.xing528.com)
(https://www.xing528.com)
图3.2.1 [Cu(phendione)(DAP)]2+与dsDNA相互作用的紫外吸收光谱图
图3.2.2为[Cu(phendione)(DAP)]2+与dsDNA相互作用的荧光光谱图。由图可知配合物在600 nm处有一个荧光峰,当溶液中逐渐加入不同量dsDNA后,配合物的特征荧光峰随着dsDNA的增大逐渐增强,这与Barton[197]等首次报道的[Ru(bpy)2(dppz)]2+“光开关”现象类似,且许多具有吡啶环的配合物在加入dsDNA后都具有这种荧光增强效应,比如[Co(bpy)2(ODHIP)]3+(ODHIP=(3,4-二羟基-咪唑[4,5-f][1,10]邻菲罗啉)[198]和[Ru(tap)2dppz]2+(tap=1,4,5,8-四氮菲)[199]。Barton等将这种荧光增强效应归因于配合物与dsDNA之间的氢键作用和能量转移[197]。因此,在本实验中,我们也推测配合物与dsDNA之间也存在着类似的相互作用和能量转移:当配合物溶液中加入dsDNA后,配合物的多吡啶配体通过疏水性嵌插作用进入dsDNA双螺旋结构与dsDNA内部的碱基对发生叠加,这种疏水性环境降低了外界水分子与配合物的接触机会,从而提高了配合物本身的荧光量子产率,导致配合物的荧光增强效果。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




