制造石英光纤预制棒最重要的原料是四氯化硅和四氯化锗,四氯化硅的分子式为SiCl4,又名氯化硅,英文名为“Silicon tetrachloride”,四氯化锗的分子式为GeCl4。它们的分子结构分别为如图2.3.1和图2.3.2所示的四面体结构。
(1)四氯化硅在常温常压状态下为无色或浅黄色发烟液体,有刺激性气味,易潮解,物理性能见表2.3.1。

图2.3.1 四氯化硅分子结构
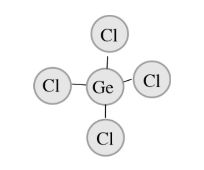
图2.3.2 四氯化锗分子结构
表2.3.1 四氯化硅特性

四氯化硅无闪点,在空气和氧气中不燃烧。四氯化硅可混溶于苯、氯仿、石油醚等有机溶剂。无水时,四氯化硅对金属极为稳定,甚至对金属钠也不起反应,这为四氯化硅的包装、运输以及提纯等方面带来便利。
四氯化硅具有腐蚀性,有窒息气味,被列入我国危险化学品管理。
四氯化硅化学性能活泼,能与许多物质发生化学反应,在400℃以上时能与空气中的氧气反应生成SiO2:
SiCl4+O2=SiO2+2Cl2(https://www.xing528.com)
在潮湿的空气中四氯化硅会水解生成二氧化硅和氯化氢气体而发烟,有强烈的刺激性气味;遇水则剧烈反应释放出大量的热,生成SiO2和盐酸:
SiCl4+2H2O=SiO2+4HCl
四氯化硅与醇反应生成硅酸酯,如与甲醇或乙醇反应可生成硅酸四甲酯和硅酸四乙酯:
SiCl4+4ROH=Si(OR)4+4HCl
四氯化硅还可与许多金属氧化物反应生成相应氯化物,与氨作用生成四氨基硅,与氢或其他还原剂反应,生成三氯氢硅和其他氯代硅烷。
(2)四氯化锗作为石英光纤中为了提高纤芯折射率以满足全反射通光条件的重要掺杂剂,其质量和纯度对光纤的性能指标具有非常重要的影响。通常要求四氯化锗中主要金属杂质的总质量分数在7.0×10-9以下,含氢化物的质量分数在在1.0×10-9以下。
四氯化锗的英文名为Germanium tetrachloride,分子式为GeCl4,又称氯化锗(Germanium chloride)。GeCl4蒸气以单分子形式存在,分子呈四面体结构。
四氯化锗为无色透明易于流动的液体,有刺激性气味,具有腐蚀性,在潮湿的空气中发烟。
四氯化锗不溶于浓盐酸,也不与浓硫酸反应,溶于稀盐酸、乙醇、乙醚、二硫化碳、氯仿、苯等。四氯化锗对热稳定,950℃仍不分解,但遇水分解为GeO2,放出有毒的腐蚀性烟气,反应式如下:
GeCl4+2H2O=GeO2+4HCl↑
四氯化锗对人的上呼吸道有刺激作用,可引起支气管炎和肺炎,对皮肤也有刺激作用,在空气中最高允许浓度为1mg/m3[Ge]。在生产操作中需要佩戴化学安全防护眼镜和橡皮手套等进行安全防护。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




