如图3.9-28(a)所示,电池是一种能量转化与存储的装置,它将化学能或物理能转化为电能,具有正极和负极。电池的电路符号如图3.9-28(b)所示,一般用字母GB表示。
电池由电极、电解质、隔离层和容器4个基本部分组成。电极由参加电化学反应的活性物质和导电材料等组成,是电池的核心部分。

图3.9-28 电池
电极分为正极(用+表示)和负极(用-表示)。电解质是酸、碱、盐的水溶液或有机电解质溶液,在电池内部正、负极间担负着传递带电离子的作用,有些电池中,电解质还参与电化学反应。隔离层位于电池正、负极之间,起隔离作用,防止内部发生短路而消耗贮存的电能。容器即电池的外壳,起保护和容纳电池组分的作用,有些电池的外壳同时又是电池的电极。
电池放电时,电子由负极经过外电路流入正极,在电池内部的电解质溶液中,正、负离子分别向两极做定向移动形成电流。两个电极上同时发生化学反应,负电极发生氧化反应,正电极发生还原反应。蓄电池充电时,电极上发生放电反应的逆反应,活性物质获得再生,将电能以化学能的形式重新贮存起来。
一、电池的分类
电池的分类方法很多,详细分类见表3.9-3。根据电池转化能量的不同,可以将电池分为化学电池和物理电池。化学电池就是将化学能转化为电能的装置,俗称电池。它由两种不同成分的电化学活性电极分别组成正、负极,由一种能提供媒体传导作用的化学物质作为电解质,当连接在某一外部载体上时,通过转换其内部的化学能提供电能。物理电池就是将物理能转化为电能的装置。
电池按其使用性质的不同,可分为原电池、蓄电池、贮备电池、太阳能电池和燃料电池等几大类。
原电池又称一次电池,一旦它的活性物质耗尽,该类电池不能通过充电的方式恢复。电解液不流动的原电池称为干电池。原电池是最常见的民用电池,如普通锌锰电池、碱性锌锰电池、锌银电池等。
蓄电池又称二次电池,这类电池可通过充电多次重复使用,如铅酸蓄电池、镉镍电池、氢镍电池、锂离子电池等都是常用的蓄电池。
贮备电池是为了使电池有较长的贮存期,贮存时将电池的其他部分与电解质分别贮存,使用时再注入电解质溶液进行活化,通常应用于军事等特殊场合。
燃料电池是一种电化学能量转换装置,它利用氢或含氢载体和氧之间的直接反应产生电能,没有直接燃烧的过程,活性物质通过装置的外部得到补充。
表3.9-3 电池的分类
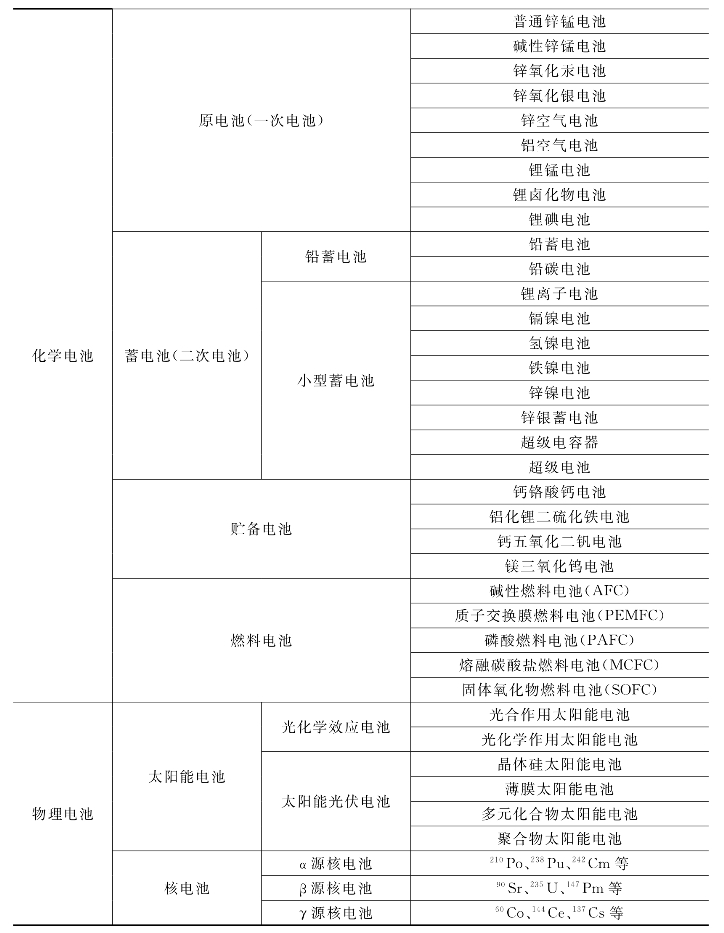
太阳能电池又可细分为太阳能光伏电池和太阳光化学电池。太阳能光伏电池通常归类为物理电池,目前实际应用的太阳能光伏电池是一种半导体器件,它受到太阳光照射时能够产生光伏效应,将太阳光能转变成直流电能,包括晶体硅太阳能电池、单晶硅太阳能电池、多晶硅太阳能电池、非晶硅太阳能电池、化合物半导体太阳能电池等。太阳光化学电池是利用光化学反应,将太阳能转换为化学能,主要有两种方法:光合作用和光化学作用。
下面介绍几种常用的电池。
1.锌锰电池(Zinc-Manganese Dry Battery)

图3.9-29 锌锰电池
如图3.9-29所示,锌-二氧化锰干电池简称锌锰电池,是采用二氧化锰作正极活性物质,锌作负极活性物质的原电池。电池采用氯化铵和氯化锌或氢氧化钾的水溶液作电解质,浆层纸或专用膜纸作隔离层,电解质溶液通常制成凝胶状或被吸收在隔离层等载体上,呈不流动状态,所以又称干电池。锌锰电池的标称电压为1.5V。按使用电解质溶液的不同分为氯化铵型、氯化锌型和碱性3种。氯化铵型和氯化锌型锌锰电池又称中性锌锰电池、碳性电池或碳锌电池。
锌锰电池根据其外形尺寸和电化学体系命名,按电池的外形分为圆柱形(用R表示)和非圆柱形电池(用P表示)两种。这里所说的外形尺寸不是指整体电池的外形尺寸,而是指其中的单体电池的外形尺寸。例如6LR61电池的整体外形是矩形的,但其中的单体电池LR61是圆柱形的,因此电池的型号是按单体电池的外形R来命名。由几个扁平形锌锰单体电池串联叠合而成的电池,通常也称为叠层式电池。
中性锌锰电池按隔离层的区别可分为糊式电池和纸板电池;按电池容量的高低可分为普通(用S表示)、高容量(用C表示)和高功率(用P表示)3个等级,中性锌锰电池无电化学体系代号。碱性锌锰电池在外形代号前要加上电化学体系代号L表示。
锌锰电池是历史最悠久的原电池,目前仍然是民用电池的主导产品。随着市场需求变化,中性锌锰电池产量已逐步下降,碱性锌锰电池产量则逐年增长。表3.9-4至表3.9-6列出了常见锌锰电池的型号和参数。
表3.9-4 常见锌锰电池型号及对照

表3.9-5 圆柱形碱性锌锰电池型号及对照
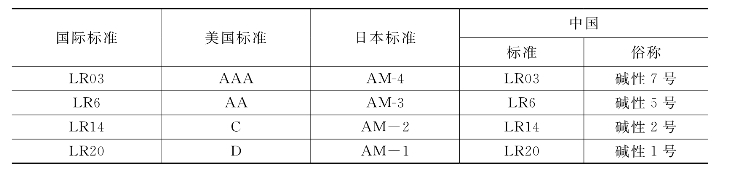
表3.9-6 1.5V扣式碱性锌锰电池型号及性能

2.锌-氧化银扣式电池(Zinc-Silver Oxide Battery)
如图3.9-30所示,锌-氧化银扣式电池外形像钮扣,是以银的氧化物作正极活性物质,锌作负极活性物质的碱性电池,分一次电池和蓄电池两类。一次电池的正极通常将氧化银与石墨混合后模压而成;二次电池一般将活性物质和导电骨架压合在一起,再经烧结而成。锌氧化银电池一般采用氢氧化钾水溶液作电解质,为改善电池性能,通常还加入一些添加剂。
锌-氧化银扣式电池标称电压为1.5V,用SR表示,其后加上电池的尺寸,直径在前,由一到两位数组成,取整数;高度在后,由两位数组成,取一位整数和第一位小数。
锌-氧化银扣式电池具有比能量高、放电电压平稳、贮存性能好、能高倍率放电等优点,但电池成本较高,常用于电子手表、计算器、小型仪表等微型电器作电源。

图3.9-30 锌-氧化银扣式电池
3.铅酸蓄电池(Valve-Regulated Lead-Acid Battery,VRLA Battery)
如图3.9-31所示,铅酸蓄电池是一种电极主要由铅及其氧化物制成,电解液是硫酸溶液的蓄电池。铅酸电池放电状态下,正极主要成分为二氧化铅,负极主要成分为铅;充电状态下,正负极的主要成分均为硫酸铅。
一个单格铅酸电池的标称电压是2V,能放电到1.5V,能充电到2.4V;在应用中,经常用6个单格铅酸电池串联起来组成标称是12V的铅酸电池,还有24V、36V、48V等。

图3.9-31 铅酸蓄电池
铅酸蓄电池的优点是电动势大、结构简单、技术成熟、循环寿命长、价格低廉,在交通、通信、军事、航海、航空等领域都有着广泛的应用。
4.镉镍电池(Nickel-Cadmium Battery,Ni-Cd Battery)
如图3.9-32所示,镉镍电池是采用金属镉作负极活性物质,氢氧化镍作正极活性物质的碱性蓄电池。正、负极材料分别填充在穿孔的附镍钢带或镍带中,经拉浆、滚压、烧结或涂膏、烘干、压片等方法制成极板;用聚酰胺非织布等材料作隔离层;用氢氧化钾水溶液作电解质溶液;电极经卷绕或叠合组装在塑料或镀镍钢壳内。
镉镍电池的分类方法很多,按密封方式可分为开口式、密封式和全密封式;按输出功率可分为低倍率型(用D表示)、中倍率型(用Z表示)、高倍率型(用G表示)和超高倍率型(用C表示);按电极结构可分为极板盒式(或袋式电极)、烧结式、黏结式、发泡式和纤维式;按外形可分为圆柱密封式(KR)、扣式(KB)、方形密封式(KC)等。
镉镍电池的优点是使用寿命长,循环次数可达几千甚至几万次,自放电小,温度范围广,耐过充、过放,放电电压平稳,缺点是烧结式电极有记忆效应、有镉污染。
大型袋式和开口式镉镍电池主要用于铁路机车、矿山、装甲车辆、飞机发动机等作启动或应急电源;圆形密封式镉镍电池主要用于电动工具等便携式电器;小型扣式镉镍电池主要用于小电流、低倍率放电的电动玩具。由于废弃镉镍电池对环境有污染,该系列的电池已逐渐被性能更好的金属氢化物镍电池所取代。

图3.9-32 镉镍电池

图3.9-33 金属氢化物镍电池
5.金属氢化物镍电池(Nickel-Metal Hydride Battery,Ni-MH Battery)(https://www.xing528.com)
如图3.9-33所示,金属氢化物镍电池是采用金属氢化物作负极活性物质,氢氧化镍作正极活性物质的碱性蓄电池,简称氢镍电池。从外形上可分为圆柱形、小方形和扣式3种。圆柱形电池是由正极、隔膜、负极卷绕而成;小方形和扣式电池则是由层状的正极、负极及中间的隔膜叠合而成。在圆柱形和小方形电池的正极端均装有安全阀,当电池内部的气体压力增大时,气体可以从此阀释放出去。
氢镍电池标称电压为1.2V,比能量约是镉镍电池的1.5~2倍,标称容量采用5小时率容量表示,定义为在(20±5)℃条件下以5小时率放电至终止电压的容量,由电池内部正负极中活性物质的填充量决定,容量的单位为m Ah或Ah。与镉镍电池相比,氢镍电池具有较高的比能量、良好的耐过充、过放能力以及无污染等特点,可与镉镍电池互换,但电池的自放电率较高。
按封口方法分类,氢镍电池可分为开口式、密封式(液密)和全密封式(气密);按电极分类,氢镍电池可分为袋式、黏结式、烧结式和泡沫式等。
高功率型氢镍电池主要用于直流电动工具(如枪钻、电锤、切割机)、遥控玩具、电动车、家用电器(如吸尘器、电动剃须刀、电动牙刷)等;高容量型氢镍电池主要用于无绳电话、子母机等;高温型氢镍电池主要作为车站、码头、宾馆、商场、医院等公共场合使用的消防应急灯具内的备用直流电源。
圆柱形密封氢镍单体电池型号由HR开头,后续以斜线分开的直径和高度,单位为mm。例如,HR15/51表示该氢镍电池直径为15mm、高度为51mm。
小型方形氢镍单体电池型号由HF开头,后续以斜线分开宽度、厚度和高度,单位为mm。例如,HF18/07/49表示该氢镍电池宽度为18mm、厚度为7mm、高度为49mm。
模块化方形镍氢电池使用数字为开头,表示每个模组有多少个单体电池,后续以QNF表示方形镍氢电池,以数字表示其标称容量,单位为Ah。例如,6QNF8表示该模块化镍氢电池有6个单体方形电池,额定容量为8Ah。
6.锂离子电池(Lithium Ion Battery,Li Battery)
如图3.9-34所示,锂离子电池是采用锂嵌入碳作负极,钴酸锂、镍酸锂或锰酸锂等氧化物作正极,聚乙烯、聚丙烯膜作隔离层,锂盐溶于有机溶剂作电解质的锂二次电池。锂钴等氧化物、碳黑等材料与黏结剂混合制浆,涂覆在集流体铝箔上,经烘干、辊压制成正极片;石墨等负极材料涂覆在铜箔上,采用与正极相同的方法制成负极片;正、负极片间插入微孔聚丙烯等薄膜作隔离层,卷绕成柱形或矩形,装入电池壳,焊接引电极、焊盖,再加入电解质溶液封口。锂离子电池有圆柱形、方形、扣式等多种形状。

图3.9-34 锂离子电池
锂离子电池的工作电压为3.6V,循环寿命达500次以上,具有比能量和工作电压高、工作温度范围宽、循环寿命长、能快速充电、无记忆效应等优点。锂离子电池广泛用于移动电话、笔记本电脑、摄像机、医疗仪器等。大容量、高功率的动力型锂离子电池逐步成为电动车辆和储能系统的理想配套电源。
聚合物锂离子电池(Polymer Lithium Ion Battery)是将有机电解质吸附在聚合物材料中形成一种聚合物电解质的锂离子电池。电池的正、负极活性物质与锂离子电池相同,电池结构简单,采用塑料制膜技术和层压技术,制成较薄的塑料电极膜,将压合层分切成需要的外形和尺寸,经活化后用铝塑膜包装成产品。
聚合物锂离子电池不仅具有锂离子电池的优良特性,还具有超轻、超薄等特点。电池的电极和电解质膜都有聚合物骨架支撑,可以自由切割制成任意形状,还可制成超薄电池。电池中没有游离电解液,消除了液体电解质电池的漏液问题。
7.铁镍电池(Nickel-Iron Battery,Ni-Fe Battery)
如图3.9-35所示,铁镍电池的负极活性物质为金属铁,正极活性物质为氧化镍,电解质为含有氢氧化锂的氢氧化钾溶液。
传统铁镍电池的结构为管式或有极板盒式铁镍电池,活性物质填充在冲孔的镀镍钢管中。将钢管固定在一定尺寸的端板上,然后将正负极板交错叠放组装成单体电池。电池外壳采用镀镍钢板制造。可在注塑尼龙槽中将单体电池组装成电池组。为了相互绝缘,钢制的电池外壳外表可涂覆一层塑料或橡胶,或者垫上绝缘垫。
铁镍电池可应用于叉车、地下采矿车、矿灯、铁路车辆、信号系统、应急照明、储能系统等,其优点是结构强度极好,放电状态下搁置无损害,循环寿命长,能承受过充电、过放电、短路等。

图3.9-35 铁镍电池

图3.9-36 太阳能电池
8.太阳能电池(Solar Cell)
如图3.9-36所示,太阳能电池是利用光伏效应将太阳光的辐射能直接转变为电能的装置。太阳能电池经过串联后进行封装保护可形成大面积的太阳能电池组件,再配合上功率控制器等部件就形成了光伏发电装置。
太阳能是人类取之不尽用之不竭的可再生清洁能源。在太阳能的有效利用中,太阳能的光电利用是近年来发展最快、最具活力的研究领域,太阳能电池已广泛应用于交通、通信、广播、石油、海洋、气象、照明、发电等领域。
太阳能电池按材料可分为晶体硅太阳能电池(单晶硅和多晶硅)、薄膜太阳能电池、多元化合物半导体太阳能电池(如砷化镓、硫化镉太阳能电池等)、聚合物太阳能电池等。
单晶硅太阳能电池是原子结构有序排列的硅太阳能电池。单晶硅太阳能电池转换效率最高,技术也最为成熟。在大规模应用和工业生产中仍占据主导地位,但由于单晶硅成本高,大幅度降低其成本很困难,为了节省硅材料,发展了多晶硅薄膜和非晶硅薄膜作为单晶硅太阳能电池的替代产品。
多晶硅太阳能电池是原子结构无序排列的硅太阳能电池。多晶硅太阳能电池兼具单晶硅电池的高转换效率和长寿命以及非晶硅薄膜电池的制备工艺简单等优点,其转换效率稍低于单晶硅太阳能电池,没有明显效率衰退问题,并且有可能在廉价衬底材料上制备,生产成本远低于单晶硅电池,效率高于非晶硅薄膜电池。因此,多晶硅薄膜电池已逐渐在太阳能电池市场上占据主导地位。
9.燃料电池(Fuel Cell)
如图3.9-37所示,燃料电池实质上是电化学反应发生器。燃料电池的反应机理是将燃料中的化学能不经燃烧直接转化为电能,实际上就是一个电解水的逆过程,通过氢氧的化学反应生成水并释放电能。氢气和氧气分别是燃料电池在电化学反应过程中的燃料和氧化剂。
燃料电池的发电不受卡诺循环的限制。理论上,它的发电效率可达到85%~90%,但由于工作时各种极化的限制,目前燃料电池的能量转化效率为40%~60%。若实现热电联供,燃料的总利用率可高达80%以上。
燃料电池以天然气等富氢气体为燃料时,二氧化碳的排放量比热机过程减少40%以上,采用纯氢为燃料时,没有二氧化碳排放。另外,由于燃料电池的燃料气在反应前必须脱硫,而且按电化学原理发电,没有高温燃烧过程,几乎不排放氮和硫的氧化物。
燃料电池的燃料范围广,只要含有氢原子的物质都可以作为燃料,例如天然气、石油、煤炭、沼气、酒精、甲醇等,因此,燃料电池非常符合能源多样化的需求,可减缓主流能源的耗竭。
当燃料电池的负载有变动时,它会很快响应。无论处于额定功率以上过载运行或低于额定功率运行,它都能承受且效率变化不大。由于燃料电池的运行高度可靠,可作为各种应急电源和不间断电源使用。
目前,燃料电池最大的应用领域是燃料电池汽车,随着其应用领域的不断扩展,已经出现了燃料电池飞机、燃料电池船舶等。

图3.9-37 燃料电池
10.超级电容器(Ultracapacitor)
如图3.9-38所示,超级电容器是通过极化电解质来储能的一种电化学元件,是一种介于传统电容器与电池之间、具有特殊性能的电源。
根据储能机理的不同,超级电容器可以分为双电层电容器、法拉第准电容器、混合型超级电容器等。
双电层电容器是在电极、溶液界面通过电子或离子的定向排列造成电荷的对峙而产生的。通常由两个高比表面积的活性碳电极构成,通过吸附电解液中的离子形成双电层,充放电过程中只涉及离子的吸附和解离,不存在氧化还原反应。
法拉第准电容器是在电极表面和近表面或体相中的二维或准二维空间上,电活性物质进行欠电位沉积,发生高度可逆的化学吸脱附(即吸附和脱附)和氧化还原反应,产生与电极充电电位有关的电容。法拉第准电容储存电荷的过程不仅包括双电层上的存储,而且包括电解液离子与电极活性物质发生的氧化还原反应。
混合型超级电容器也称非对称超级电容器,一极是形成双电层电容的活性碳电极材料构成,另一极是利用法拉第准电容储能的金属氧化物电极(即一个二次电池的电极,例如铅酸电池的二氧化铅电极),充放电过程中,二次电池的电极发生氧化还原反应,活性碳电极发生离子的吸附和解离。混合型超级电容器比能量较单纯的双电层电容器的电容量大幅提高,具有较高的比功率和循环寿命。
超级电容器主要是利用电极、电解质界面电荷分离所形成的双电层,或借助电极表面快速的氧化还原反应所产生的法拉第准电容来实现电荷和能量的储存,具有秒级高倍率充放电、循环性能优异、寿命长、安全性高等优点。
超级电容器可以与铅蓄电池或锂离子电池组成复合电源,用于电动公交车、混合动力电动车等电动车辆;可作为辅助电源回收车辆、电梯等设备减速、停止或变向时消耗的能量,再次用于设备的运行中。
微型超级电容器已经在小型机械设备上得到了广泛应用,例如照相机、音频设备和间歇性用电的辅助设施;而大尺寸的柱状超级电容器则多用于汽车和采矿业。
二、电池的检测
可以使用万用表对电池进行初步检测。将万用表置于直流电压量程合适的挡位,红、黑表笔分别接电池的正、负极,测量电池的直流电压。若测得的电压值为零,则说明电池已损坏;若测得的电压值低于或远低于其标称电压值,则说明电池电量下降明显或几乎耗尽;若测得的电压值近似甚至高于其标称电压值,则说明电池电动势正常,如果要判断其电量是否饱满则需要外接负载测量。
一般情况下,测量电池空载时的电压不能准确判断电池的电量情况。化学电池电能耗尽的主要表现是电池内阻增加,接上负载后,电池内阻有一个明显电压降。电池外接负载时,如果测得的路端电压值近似标称电压值,则说明电池电量充足;如果测得的路端电压值明显小于标称电压值,则说明电池的电量不足。

图3.9-38 超级电容器
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




