虽然纯金属在工业生产上获得了一定的应用,但由于其强度一般都很低,如铁的抗拉强度约为200 MPa,而铝还不到100 MPa,显然都不适合作结构材料。因此,目前应用的金属材料绝大多数是合金。所谓合金,是指两种或两种以上的金属,或金属与非金属,经熔炼或烧结,或用其他方法组合而成的具有金属特性的物质。例如,应用最广泛的碳钢和铸铁是由铁和碳组成的合金,黄铜是由铜和锌组成的合金等。
2.2.1 合金中的相
组成合金最基本、独立的物质叫作组元,或简称元。一般说来,组元就是组成合金的元素,也可以是稳定的化合物。例如,铜和锌是黄铜的两个组元,Fe3C和铁是碳钢和铸铁的两个组元。由两个组元组成的合金称为二元合金,由三个组元组成的合金称为三元合金,由三个以上组元组成的合金称为多元合金。
由若干个给定的组元,按照不同的比例配制成一系列成分不同的合金,这一系列合金就构成一个合金系统,简称合金系。两个组元组成的为二元系,三个组元组成的为三元系,三个以上组元组成的为多元系。
当不同的组元经熔炼或烧结组成合金时,这些组元间由于物理的和化学的相互作用,形成具有一定晶体结构和一定成分的相。相是指合金中结构相同、成分和性能均一并以界面相互分开的组成部分。如纯金属在固态时为一个相(固相),在熔点以上为另一个相(液相)。而在熔点时,固体与液体共存,两者之间有界面分开,它们各自的结构不同,所以此时为固相和液相共存的混合物。由一种固相组成的合金称为单相合金,由几种不同固相组成的合金称为多相合金。
在金属与合金中,由于形成条件的不同,可能形成不同的相,相的数量、形态及分布状态也可能不同,从而形成不同的组织。相是组织的基本组成部分,当相的形态和分布不同时,就会出现不同的组织,使材料表现出不同的性能。
2.2.2 合金的相结构
不同的相具有不同的晶体结构,合金相的种类极为繁多,但根据相的晶体结构特点可以将其分为固溶体和金属化合物两大类。
1.固溶体
合金组元之间以不同比例相互混合后形成的固相,其晶体结构与组成合金的某一组元的相同,这种相就称为固溶体,这种组元称为溶剂,其他的组元即为溶质。
按溶质原子在晶格中所占的位置可以将固溶体分为间隙固溶体和置换固溶体两类。
1)间隙固溶体
间隙固溶体是指溶质原子不是占据溶剂晶格的正常节点位置,而是填入溶剂晶格的一些间隙中所形成的固溶体,如图2-15(a)所示。
2)置换固溶体
置换固溶体是指溶质原子位于溶剂晶格的某些节点位置所形成的固溶体,犹如这些节点上的溶剂原子被溶质原子所置换一样,因此称为置换固溶体,如图2-15(b)所示。

图2-15 固溶体的两种类型
金属元素彼此之间一般都能形成置换固溶体,但溶解度大小往往相差悬殊。溶解度的大小主要取决于溶质元素和溶剂元素的原子尺寸、晶格类型和化学元素周期表中的位置。一般说来,溶质原子和溶剂原子尺寸差别越小,溶解度就越大。如果溶质元素和溶剂元素在化学元素周期表中的位置靠近,且晶格类型相同,往往按任意比例配置都能相互溶解,形成无限固溶体。
由于溶剂晶格的间隙一般都很小,因此形成间隙固溶体的溶质元素,都是一些原子半径较小的非金属元素,如氢、氮、碳、硼,而溶剂元素则都是过渡族元素。溶剂晶格的间隙是有限的,因此能溶入的溶质原子数量也有限,故间隙固溶体都是有限固溶体。
3)固溶体的性能
虽然固溶体仍保持着溶剂的晶格类型,但随着溶质原子的溶入,由于溶质原子与溶剂原子的尺寸不可能完全相同,必然导致在溶质原子附近的局部范围内造成晶格畸变,并因此形成一个弹性应力场,如图2-16所示。晶格畸变使位错移动时的阻力增大,变形抗力增加,结果导致金属的强度、硬度提高。这种在固溶体中,随着溶质浓度的增加,固溶体的强度、硬度增加,而塑性、韧性有所下降的现象,称为固溶强化。

图2-16 固溶体晶格畸变示意图
2.金属化合物
合金组元间相互作用,除可形成固溶体外,当超过固溶体的固溶度极限时,还可形成金属化合物,又称为中间相。金属化合物的晶体结构及性能均不同于任一组元,一般可以用分子式来大致表示其组成。金属化合物的原子间结合方式是金属键与离子键或共价键相混合的方式,因此它具有一定的金属性质,所以称之为金属化合物。如碳钢中的Fe3C、黄铜中的CuZn、铝合金中的CuAl2等都是金属化合物。
金属化合物一般具有较高的熔点、硬度和脆性,当合金中出现金属化合物时,将使合金的强度、硬度、耐磨性及耐热性提高,因此金属化合物已是新的功能材料中不可缺少的合金相。
金属化合物的种类很多,下面主要介绍三种。
1)正常价化合物
正常价化合物通常是由金属元素与周期表中ⅣA、ⅤA、ⅥA族元素组成的,例如MgS、MnS、Mg2Si、Mg2Sn、Mg2Pb等。正常价化合物具有严格的化合比,成分固定不变,可用化学式表示。这类化合物一般具有较高的硬度,脆性较大。
2)电子价化合物
电子价化合物是由ⅠB族或过渡族金属元素与ⅡB、ⅢA、ⅣA族元素形成的金属化合物,它不遵守原子价规律,而是按照一定的电子浓度的比值形成。电子浓度不同,所形成的化合物的晶体结构也不相同。所谓电子浓度,是指化合物中价电子数与原子数的比值。例如电子浓度为3/2(21/14)时,具有体心立方结构,称为β相(CuZn);电子浓度为21/13时,为复杂立方结构,称为γ相(Cu5Zn8);电子浓度为7/4(21/12)时,则为密排六方结构,称为ε相。电子价化合物虽然可以用化学式表示,但其成分可以在一定范围内变化,因此可以把它看作是以化合物为基的固溶体。电子价化合物通常具有很高的熔点和硬度,但脆性很大。
3)间隙相和间隙化合物
间隙相和间隙化合物一般是由原子尺寸较大的过渡族金属元素(铁、铬、钼、钨、钒)与原子直径较小的非金属元素(氢、碳、氮、硼等)组成的。根据金属元素(以x表示)与非金属元素(以m表示)原子半径的比值,可将其分为两类:当rx/rm<0.59时,形成具有简单结构的化合物,称为间隙相;当rx/rm>0.59时,则形成具有复杂晶体结构的化合物,称为间隙化合物。
间隙相具有简单的晶体结构,如面心立方、体心立方、密排六方或简单六方等,金属原子位于晶格的正常节点上,非金属原子则位于晶格的间隙位置。间隙相具有极高的熔点和硬度,具有明显的金属特性。它们是硬质合金的重要相组成,用硬质合金制作的高速切削刀具、拉丝模及各种冷冲模已得到广泛的应用。
间隙化合物一般具有复杂的晶体结构,Cr、Mn、Fe的化合物均属此类。它的种类很多,其中渗碳体是钢铁材料中的一种基本组成相。间隙化合物也具有很高的熔点和硬度,但与间隙相相比,其熔点和硬度都要低些,而且加热时也较易分解。
2.2.3 二元合金相图
纯金属结晶后只能得到单相的固体,合金结晶后,既可获得单相的固溶体,也可获得单相的金属化合物,但更常见的是获得既有固溶体又有金属化合物的多相组织。组元不同,获得的固溶体和化合物的类型也不同,即使组元确定之后,结晶后所获得的相的性质、数目及其相对含量也随着合金成分和温度的变化而变化,即在不同的成分和温度时,合金将以不同的状态存在。为了研究不同合金系中的状态与合金成分和温度之间的变化规律,就要利用相图这一工具。
相图是表示在平衡条件下合金系中合金的状态与温度、成分间关系的图解,又称为状态图或平衡图。利用相图,可以一目了然地了解到不同成分的合金在不同温度下的平衡状态,它存在哪些相,相的成分及相对含量如何,以及在加热或冷却时可能发生哪些转变等。显然,相图是研究金属材料的一个十分重要的工具。
1.二元合金相图的建立
1)二元合金相图的表示方法
合金存在的状态通常由合金的成分、温度和压力三个因素确定,合金的化学成分变化时,则合金中所存在的相及相的相对含量也随之发生变化;同样,当温度和压力发生变化时,合金所存在的状态也要发生改变。由于合金的熔炼、加工处理等都是在常压下进行的,所以合金的状态可由合金的成分和温度两个因素确定。对于二元系合金来说,通常用横坐标表示成分,纵坐标表示温度,如图2-17所示。横坐标上的任一点均表示一种合金的成分,如A、B两点表示组成合金的两个组元,C点的成分为wB=40%,wA=60%,D点的成分为wB=60%,wA=40%等。
在成分和温度坐标平面上的任意一点称为表象点,一个表象点的坐标值表示一个合计的成分和温度,如图2-17中的E点表示合金的成分为wB=60%,wA=40%,温度为500 °C。
2)二元合金相图的测定方法
目前使用的相图一般都是通过试验的方法得到的,现以Cu-Ni合金为例,说明用热分析试验法测定及绘制合金相图的过程。

图2-17 二元合金相图的坐标
(1)配制一系列不同成分的Cu-Ni合金,如表2-1所示。
(2)用热分析试验法测出各成分Cu-Ni合金的冷却曲线,如图2-18(a)所示。
表2-1 Cu-Ni二元合金的成分和试验结果
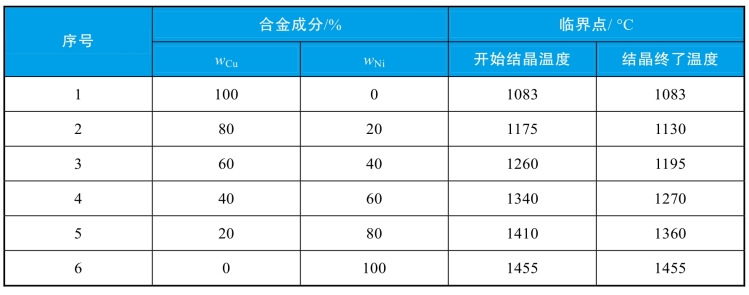

图2-18 Cu-Ni二元合金相图的测定
(3)找出各冷却曲线上的相变点。可以看出,纯铜和纯镍的冷却曲线都有一水平阶段,表示其结晶的临界点。其他四种合金的冷却曲线都没有水平阶段,但有两次转折,两个转折点对应的温度表示两个临界点,表明这四种合金都是在一定温度范围内结晶的,温度较高的临界点是结晶开始的温度,温度较低的临界点是结晶终了的温度,如表2-1所示。
(4)将各个合金的临界点分别标注在温度-成分坐标图中相应的合金线上。
(5)连接各意义相同的临界点,就可得到如图2-18(b)所示的Cu-Ni相图。其中上临界点的连线称为液相线,表示合金结晶的开始温度或加热过程中熔化终了的温度;下临界点的连线称为固相线,表示合金结晶的终了温度或加热过程中开始熔化的温度。
从上述测定合金相图的方法可知,配制的合金数目越多,所用金属纯度越高,热分析时冷却的速度越缓慢,则测得的合金相图越精确。目前,已通过试验的方法测定出了许多二元合金相图和三元合金相图,其形式一般都比较复杂,然而复杂的合金相图可以看作是由若干个简单的基本相图组成的。
2.相律及杠杆定律
1)相律及其应用
相律是检验、分析和使用相图的重要工具,所测定的相图是否正确,要用相律检验。在研究和使用相图时,也要用到相律。相律是表示在平衡条件下,系统的自由度数、组元数和相数之间的关系,是系统的平衡条件的数学表达式。相律可用下式表示:
![]()
式中,F为平衡系统的自由度数;C为平衡系统的组元数;P为平衡系统的相数。
相律的含义是:在只受外界温度和压力影响的平衡系统中,它的自由度数等于系统的组元数和相数之差再加上2。平衡系统的自由度数是指平衡系统的独立可变因素(如温度、压力、成分等)的数目。这些因素可在一定范围内任意独立地改变而不会影响到原有的共存相数。当系统的压力为常数时,相律可表达为(https://www.xing528.com)
![]()
此时,合金的状态由成分和温度两个因素确定。因此,对纯金属而言,成分固定不变,只有温度可以独立改变,所以纯金属的自由度数最多只有1个。而对二元系合金来说,已知一个组元的含量,则合金的成分即可确定,因此合金成分的独立变量只有1个,再加上温度因素,所以二元合金的自由度数最多为2个,依次类推,三元系合金的自由度数最多为3个,四元系为4个……
下面讨论应用相律的几个例子。
(1)利用相律确定系统中可能共存的最多平衡相数。
例如,对单元系来说,组元数C=1,由于自由度不可能出现负值,所以当F=0时,同时,共存的平衡相数应具有最大值,代入相律公式,即得
![]()
可见,对单元系来说,同时共存的平衡相数不超过2个。例如,纯金属结晶时,温度固定不变,自由度为零,同时共存的平衡相为液、固两相。
同样,对二元系来说,组元数C=2,当F=0时,P=2-0+1=3,说明二元系中同时共存的平衡相数最多为3个。
(2)利用相律解释纯金属与二元合金结晶时的一些差别。
例如,纯金属结晶时存在液、固两相,其自由度为零,说明纯金属在结晶时只能在恒温下进行。二元合金结晶时,在两相平衡条件下,其自由度F=2-2+1=1,说明温度和成分中只有一个独立可变因素,即在两相区内任意改变温度,则成分随之而变,反之亦然。此时,二元合金将在一定温度范围内结晶。如果二元合金出现三相平衡共存,则其自由度F=2-3+1=0,说明此时的温度不但恒定不变,而且三个相的成分也恒定不变,结晶只能在各个因素完全恒定不变的条件下进行。
2)杠杆定律
在合金的结晶过程中,随着结晶过程的进行,合金中各个相的成分以及它们的相对含量都在不断地发生着变化。为了了解某一具体合金中相的成分及其相对含量,需要应用杠杆定律。在二元系合金中,杠杆定律主要适用于两相区,因为对单相区来说无此必要,而三相区又无法确定,这是由于三相恒温线上的三个相可以以任何比例相平衡。
要确定相的相对含量,首先必须确定相的成分。根据相律可知,当二元系处于两相共存时,其自由度为1,这说明只有一个独立变量。例如温度变化,那么两个平衡相的成分均随温度的变化而改变;当温度恒定时,自由度为零,两个平衡相的成分也随之固定不变。两个相成分点之间的连线(等温线)称为连接线。实际上两个平衡相成分点即为连接线与两条平衡曲线的交点,下面以Cu-Ni合金为例进行说明。
如图2-19(a)所示,在Cu-Ni二元相图中,液相线是表示液相的成分随温度变化的平衡曲线,固相线是表示固相的成分随温度变化的平衡曲线,含Ni量为%x的合金在温度Tx时,处于两相平衡状态,即![]() ,要确定液相L和固相α的成分,可通过温度Tx作一水平线段x1xx2,分别交液相线和固相线于两点,此两点在横坐标上的投影为x1和x2,即含量为x的合金在Tx温度时相互平衡的液相和固相的化学成分含量。
,要确定液相L和固相α的成分,可通过温度Tx作一水平线段x1xx2,分别交液相线和固相线于两点,此两点在横坐标上的投影为x1和x2,即含量为x的合金在Tx温度时相互平衡的液相和固相的化学成分含量。
下面计算液相和固相在温度Tx时的相对含量。设合金的总质量为1,液相的质量为wL,固体的质量为wα,则有
![]()
此外,该合金中的含镍量应等于液相中镍的含量与固相中镍的含量之和,即
![]()
由式(2-6)、(2-7)可以得出

如果将该合金成分的x点看作支点,将wL、aα看作作用于x1和x2的力,则按力学的杠杆原理就可得出式(2-8)。因此将式(2-8)称为杠杆定律,但这只是一种比喻。杠杆原理示意图如图2-19(b)所示。
式(2-8)也可以换写成下列形式:

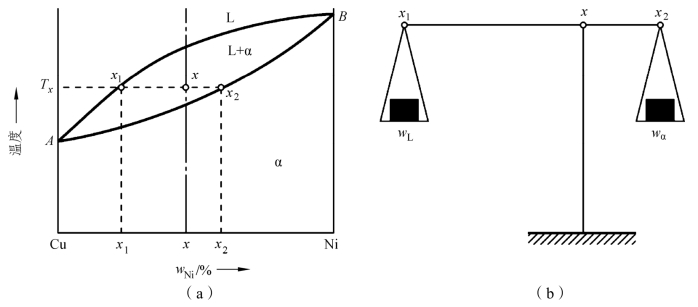
图2-19 杠杆定律的证明及力学比喻
这两式可以直接用来求出两相的含量。
值得注意的是,在推导杠杆定律的过程中,并没有涉及Cu-Ni相图的性质,而是基于相平衡的一般原理导出的。因而不管怎样的系统,只要满足相平衡的条件,那么在两相共存时,其两相的含量都能用杠杆定律确定。
3.匀晶相图
两组元不但在液态无限互溶,而且在固态也无限互溶的二元合金系所形成的相图,称为匀晶相图。具有这类相图的二元合金系主要有:Cu-Ni、Ag-Au、Cr-Mo、Cd-Mg、Fe-Ni、Mo-W等。现以Cu-Ni相图为例进行分析。
Cu-Ni二元合金相图如图2-20所示,该相图十分简单,只有两条曲线,上面一条是液相线,下面一条是固相线,液相线和固相线把相图分成三个区域,即液相区L、固相区α以及液、固两相并存区L+α。

图2-20 Cu-Ni合金相图及结晶过程分析
平衡结晶是指合金在极缓慢冷却条件下进行结晶的过程。下面以wNi=30%的Cu-Ni合金为例进行分析。
从图2-20(a)中可以看出,当合金自高温缓慢冷却至t1温度时,开始从液相中结晶出α固溶体,此时液相成分为L1,固相成分α1的含量为零。说明在温度t1时,结晶刚刚开始,实际固相尚未形成。当缓慢冷却至t2温度时,便有一定数量的α固溶体结晶出来,此时固相成分为α2,液相成分为L2,当冷却至t3温度时,最后一滴液体结晶成固溶体,结晶终了,得到了与原合金成分相同的α固溶体。图2-20(b)示意地说明了该合金平衡结晶时的组织变化过程。
4.共晶相图
两组元在液态时相互无限互溶,在固态时相互有限互溶,发生共晶转变,形成共晶组织的二元系相图,称为二元共晶相图。Pb-Sn、Pb-Sb、Ag-Cu、Pb-Bi等合金系的相图都属于共晶相图,在Fe-C、Al-Mg等相图中,也包含有共晶部分。下面以Pb-Sn相图为例,对共晶相图进行分析说明。
图2-21为Pb-Sn二元共晶相图,图中AEB为液相线,AMENB为固相线,MF为Sn在Pb中的溶解度曲线,也叫固溶度曲线,NG为Pb在Sn中的溶解度曲线。
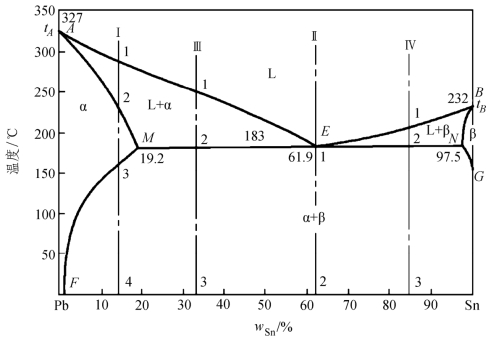
图2-21 Pb-Sn二元共晶相图
相图中有三个单相区:即液相L、固溶体α相和固溶体β相。α相是Sn溶于Pb中的固溶体,β相是Pb溶于Sn中的固溶体。各个单相区之间有三个两相区,即L+α、L+β和α+β。在L+α、L+β与α+β两相区之间的水平线MEN表示α+β+L三相共存区。
在三相共存水平线所对应的温度下,成分相当于E点液相LE同时结晶出与M点相对应的αM和N点对应的βN两个相,形成两个固溶体的混合物。这种转变的反应式为
![]()
这一转变是在恒温下进行的,而且三个相的成分是恒定值,在相图上的特征是三个单相区与水平线只有一个接触点,其中液相单相区在中间,位于水平线之上,两端是两个固相单相区。这种在一定温度下,由一定成分的液相同时结晶出成分一定的两个固相的转变过程,称为共晶转变或共晶反应。共晶转变的产物为两个固相的混合物,称为共晶组织。
相图中的MEN水平线称为共晶线,E点称为共晶点,E点对应的温度称为共晶温度,成分对应于共晶点的合金称为共晶合金,成分位于共晶点E以左、M点以右的合金称为亚共晶合金,成分位于共晶点E以右、N点以左的合金称为过共晶合金。
图2-21中的合金Ⅱ即为共晶合金,合金Ⅲ为亚共晶合金,合金Ⅳ为过共晶合金,从相图中可以看出,在缓慢冷却时,都会发生共晶转变。
5.包晶相图
在一定温度下,由一个液相包着一个固相生成另一新固相的反应称包晶转变或包晶反应。当两组元在液态下相互无限溶解,在固态下相互有限溶解并发生包晶反应时所构成的相图称作包晶相图。具有包晶转变的二元合金系有Pt-Ag、Sn-Sb、Cu-Sn、Cu-Zn等。下面以Pt-Ag合金系为例,对包晶相图及其合金的结晶过程进行分析。
Pt-Ag二元合金相图如图2-22所示。图中ACB为液相线,APDB为固相线,PE及DF分别是Ag溶于Pt中和Pt溶于Ag中的溶解度曲线。

图2-22 Pt-Ag合金相图
相图中有三个单相区:即液相L及固相α和β。其中α相是Ag溶于Pt中的固溶体,β 相是Pt溶于Ag中的固溶体。单相区之间有三个两相区,即L+α、L+β和α+β。两相区之间存在一条三相(L、α、β)共存水平线,即PDC线。
水平线PDC是包晶转变线,所有成分在P与C范围内的合金在此温度都将发生三相平衡的包晶转变,这种转变的反应式为
![]()
这种在一定的温度下,由一定成分的固相与一定成分的液相作用,形成另一个一定成分的固相的转变过程,称为包晶转变或包晶反应。根据相律可知,在包晶转变时,其自由度为零(F=2-3+1=0),即三个相的成分不变,且转变在恒温下进行。在相图上,包晶转变区的特征是:反应相是液相和一个固相,其成分点位于水平线的两端,所形成的固相位于水平线中间的下方。
相图中的D点称为包晶点,D点所对应的温度(tD)称为包晶温度,PDC线称为包晶线。
2.2.4 合金力学性能与相图的关系
当合金形成单相固溶体时,合金的力学性能与组元的性质、溶质元素的含量有关。对于一定的溶剂和溶质,溶质含量越多,则合金晶体中的晶格畸变程度越严重,合金的强度、硬度越高,但能保持较好的塑性与韧性。固溶体合金的强度、硬度变化规律如图2-23所示。
当合金形成两相混合物时,其力学性能随合金成分的改变而呈直线关系在两组成相的性能之间变化。当合金形成共晶组织时,力学性能还与组织的细密程度有关,共晶组织越细密,合金的强度、硬度越高。两相混合物合金的硬度变化规律如图2-24所示。
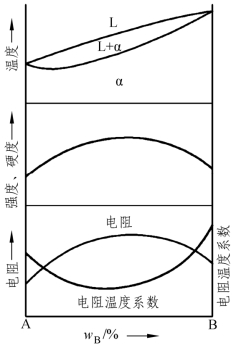
图2-23 固溶体合金的强度、 硬度和电阻与相图间的关系

图2-24 两相混合物合金的硬度、温度 和电阻与相图间的关系
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




