为防止镁溶液的氧化燃烧,生产中一直采用在熔剂层保护下的熔炼。镁合金熔剂有两种作用:①覆盖作用,熔融的熔剂借助表面张力的作用,在镁熔体表面形成一连续、完整的覆盖层,隔绝空气,阻止Mg-O2、Mg-H2O反应,防止了镁的氧化,也能扑灭镁的燃烧;②精炼作用,熔融的熔剂对非金属夹杂物具有良好的润湿、吸附能力,并利用熔剂与金属的密度差,把金属夹杂物随同熔剂自熔体中排除。
镁或镁合金熔剂应当具有的性质:①低于纯镁或镁合金的熔点;②足够高的液体流动性和表面张力,以便在熔融的金属上造成连续的覆盖膜;③黏滞性,以便熔剂能够在合金的浇注温度与金属分离,防止熔剂进入铸型中;④润湿坩埚壁和炉底的能力;⑤精炼的能力,即从合金液中除掉非金属夹杂物的能力;⑥在700~800℃时,密度要大于合金的密度,以保证熔剂质点由合金液中沉淀下来;⑦不与镁及其合金的其他组分起化学反应;⑧不与炉子材料起化学反应。几种熔化镁的保护熔剂的成分配比见表3-4。
表3-4 几种熔化镁的保护熔剂的成分配比
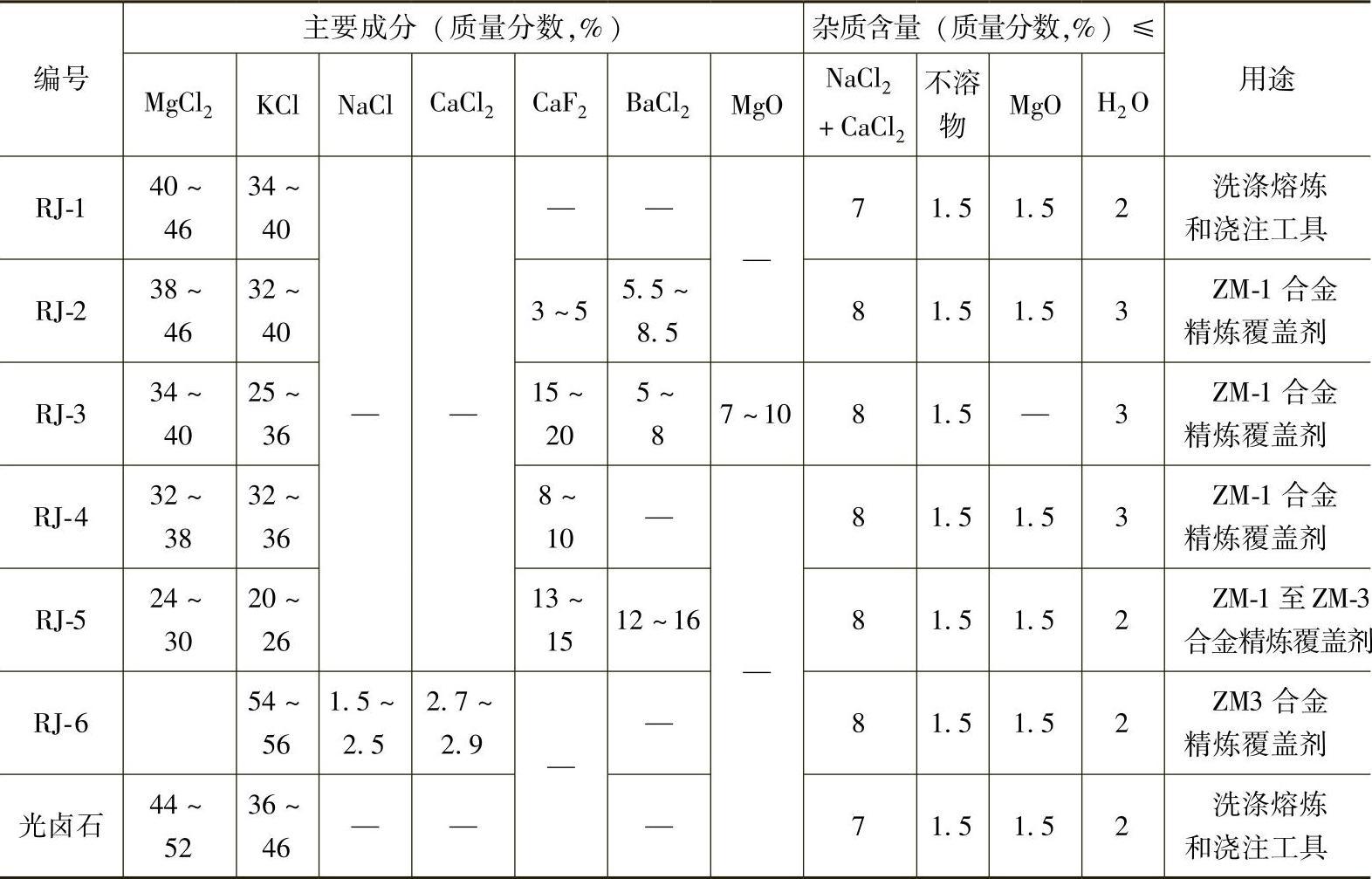
镁合金熔剂主要是由MgCl2、KCl、CaF2、BaCl2等氯盐、氟盐的混合物组成的。熔剂中采用碱金属和碱土金属的卤化物是因为它们的化学稳定性高。几种盐按一定比例混合,使熔剂的熔点、密度、黏度及表面性能均能较好地满足使用要求。
镁合金熔剂的主要成分是MgCl2,它对镁熔体具有良好的覆盖作用及一定的精炼能力。MgCl2的熔点为708℃,易与其他盐混合形成低熔点盐类混合物,如无水光卤石[w(MgCl2)=44%~52%,w(KCl)=32%~46%],其熔点仅为400~480℃,因此流动性好,在镁熔体表面能够迅速地铺展成一层连续、严密的熔剂层。MgCl2也能很好地润湿熔体表面的氧化镁,并将其包覆后转移到熔剂中去,消除了由氧化镁所产生的绝热作用,使镁在氧化中产生的热量能较快地通过熔剂层散出,避免镁熔体表面温度急剧上升。MgCl2还能与空气中的氧及水汽反应生成HCl、Cl2、H2等,其反应式见式(3-13)~式(3-17)。反应生成的Cl2、HCl又能迅速和镁反应生成一层Mg2Cl2,盖住无熔剂的镁熔体表面。这样,HCl、Cl2、H2等保护性气氛及MgCl2薄层覆盖均能有效地阻止镁与氧、水的作用,防止氧化,抑制燃烧。试验证明,在镁熔体表面撒上一层干的MgCl2粉,即使没有形成连续的覆盖层,同样也能扑灭燃烧,而其他熔剂只能起到机械隔绝的作用。MgCl2的良好精炼作用在于液态的MgCl2对MgO、Mg3N2的润湿性好,能有效地吸附悬浮于熔体中的这些夹杂。此外,MgCl2还具有化学造渣的作用,见式(3-17),形成的产物MgCl2·5MgO能从熔体中沉淀出来。可见,MgCl2在精炼过程中起主要作用。
2MgCl2+O2==2MgO+2Cl2 (3-13)
MgCl2+H2O==MgO+2HCl (3-14)
2HCl+Mg==MgCl2+H2 (3-15)
Mg+Cl2==MgCl2 (3-16)
MgCl2+5MgO==MgCl2·5MgO (3-17)
在MgCl2中加入KCl后,能够显著降低MgCl2的熔点、表面张力和黏度。KCl的另一作用是提高熔剂的稳定性,即减少高温时MgCl2的蒸发损失,使MgCl2的蒸气压下降。KCl和MgCl2质量分数各占50%的熔剂蒸气压最小。KCl的存在还大大抑制MgCl2加热脱水的水解过程(部分转化为MgO和HCl),减少MgCl2在脱水操作时的损失。(https://www.xing528.com)
BaCl2的密度大,964℃液态时的密度为3.06g/cm3,20℃固态时的密度为3.87g/cm3。可作为熔剂的加重剂,以增大熔剂与镁熔体之间的密度差,使熔剂与镁熔体更易于分离。BaCl2的熔点为960℃,黏度较大,加到熔剂中也能加大熔剂的黏度。
CaF2比无水光卤石密度大,20℃时固态密度为3.18g/cm3,964℃时液态密度为2.53g/cm3,而光卤石的密度仅1.58g/cm3,故也可加大熔剂密度。CaF2加到KCl、NaCl、CaCl2等盐中,如加入量超过共晶点,则使熔剂的黏度剧增,故可用作增稠剂。在含有足够量MgCl2的熔剂中,加入CaF2可提高熔剂的稳定性和精炼能力,因两者之间可发生反应,见式(3-18)。
CaF2+MgCl2==MgF2+CaCl2 (3-18)
MgF2在氯盐中溶解度很小,它的存在改变了CaF2的溶解度随着温度变化而显著改变的特点。所以加入少量CaF2即可使熔剂稠化,也不会因温度波动而使熔剂性能不稳定。MgF2的存在,还可提高熔剂的精炼能力,其原因是MgF2对MgO有化合造渣的能力。也有人认为加入氯盐后,提高了MgO在熔剂中的溶解度。少量的氟离子可适当提高熔剂与镁熔体间的表面张力,改善精炼效果。因此,熔剂中一般均加入CaF2。
熔剂对镁熔体的铺展、覆盖、精炼能力的好坏和熔剂的成分配比有着密切关系。配制好的合格熔剂如保存不当,吸湿后(熔剂吸湿性强,特别是MgCl2)使含水量超过标准,加到镁熔体中就会产生大量氧化夹杂。熔剂中的MgCl2与水作用生成MgO,在液面上结成小团,不能很好地铺展、覆盖,失去了精炼的作用。水量较多时,熔剂与镁熔体接触会产生火花,甚至会引起镁熔体的飞溅性爆炸。
镁合金熔炼过程中使用的材料还有硫黄、硼酸(HBO3)、氟附加物(NH4BF4·NH4HF·NH4F)、烷基磺酸钠(RSONa)等,用以防止镁熔体在浇注及充填铸型时发生氧化、燃烧。
硫与镁接触时,一方面受热蒸发(硫的沸点为444.6℃)形成SO2防护性气体;另一方面与镁熔体反应,在其表面形成严密的MgS膜(致密度系数α=0.95),以减缓镁熔体的氧化。
HBO3受热后即脱水生成硼酐(B2O3),它与镁反应还原出硼,与镁形成致密的Mg3B2保护膜。B2O3还可与溶液表面的MgO反应,生成MgO·B2O3,它是致密的秞质保护膜,能防止镁熔体的燃烧。
氟附加物与镁熔体接触后即分解出HF、NH4等防护性气体,并在镁熔体表面形成致密的MgF2及Mg3N2保护膜,具有良好的防护作用。但由于产生大量的氟化物气体,这些有害气体严重损害人的身体健康,腐蚀厂房设备,污染环境,近年来已基本被RSONa所取代。
型砂中加入质量分数为2%~4%的RSONa和1.5%~2.5%的HBO3,可防止镁在充填铸型过程中的燃烧,因为RSONa受热后既能分解出SO2、CO2等防护性气体,又能与镁熔体反应生成MgS等致密膜。
镁合金熔体一般不用石墨坩埚或耐火材料炉衬(坩埚),因为SiO2与镁生成不溶于镁熔体的Mg2Si,这是镁合金中最有害的杂质,能降低合金的塑性和耐蚀性。故炉料中的砂粒必须清理干净,以防止硅进入镁熔体中。生产上一般使用铸钢或钢板焊接坩埚,因为铁在镁熔体中的溶解度极小。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




