氢的原子半径甚小,在自然界中它是唯一可渗透进固体金属的气体。镁与氢的作用可分为四个过程:表面吸附、扩散、溶解和化学作用。
1.表面吸附
氢气分子首先在金属表面聚集,气态分子以极小的力完成其物理吸附。而活性吸附的力,相当于化学作用力。活性吸附是在更高温度下进行的。气体的吸附量与其蒸气压和温度有关。
2.扩散
扩散是气体原子进入金属纵深的一个基本过程。它是固态金属原子无序热运动的结果。吸附是扩散的前提,向金属进行扩散的气体,只有具有活性吸附能力才有可能实现扩散。
应当指出,氢在金属中的扩散速度比其他气体快得多。[H]扩散穿透金属是以原子和离子形式进行的。[H]扩散容易的原因就在于其原子半径小于金属的结晶晶格常数。温度的升高能加速[H]的迁移过程。
金属的表面和组织对扩散过程实际也有影响。表面粗糙程度的增加将增大吸附面积,因此在低压情况下将大大提高其扩散速度。表面的氧化膜影响[H]的渗透。
3.溶解
[H]在镁中的溶解度比铝大得多,它们一般相差两个数量级。氢的主要来源是潮气,即
Mg+H2O==MgO+2[H] (3-1)
4.化学作用(https://www.xing528.com)
[H]和镁不形成化合物,它在镁中呈间隙固溶体存在。但[H]和镁合金中的其他组元可形成稳定的化合物。
在室温下[H]和铈可生成CeH3。在473~573K时氢化速度最大。973K前为CeH3,高于973K时则形成CeH2,该氢化物在1073~1173K时实际上仍是稳定的。
[H]和锆形成稳定的化合物ZrH2,ZrH2析出时呈微细的六角形或直角形的薄片。锆使[H]在镁中的溶解度增大,而[H]又使锆在镁合金中的溶解度减小,因为ZrH2在镁合金中是不溶解的。[H]对锆在镁合金中溶解度的影响见表3-3。
表3-3 [H]对锆在镁合金中溶解度的影响

(续)
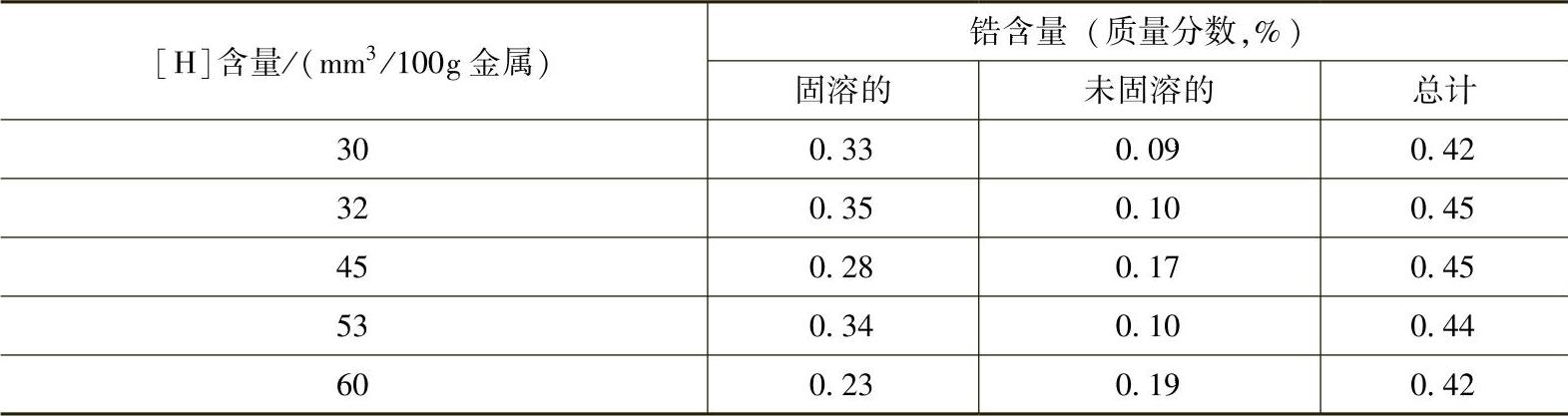
从表3-3可以看出,随着[H]含量增加,锆在镁合金中的溶解度减小,锆的损失增大。
[H]的有害作用是在镁合金的凝固过程中,随着温度降低其溶解度减小,使合金产生显微疏松。不少研究者得出结论,在工业条件下,当氢含量大于15cm3/(100g金属)时,则能在Mg-Al-Zn系合金中出现显微疏松。
镁合金中的气体问题曾有一阶段未引起足够重视,这是由于在最常用的标准类镁合金中疏松问题比较严重,疏松与气孔很难截然分开,因此常常掩盖了气孔存在的问题。而且由于镁合金熔体凝固时氢在其中的溶解度的相对变化值比较小,仅为氢在铝中溶解度变化相对值的几十分之一,因此在冷却较快的铸件薄壁处氢很易过饱和地溶于镁合金中而不形成气孔,铸件厚壁处在使用冷铁飞冒口时易使部分氢被排至冒口中,部分则过饱和地溶于较快冷却的铸件表层中。因此,气孔问题在生产中表现得不突出。但由于对镁合金质量的要求日益增高,而镁合金中的气体常常加剧了疏松,故对镁合金熔体的除气也显得非常重要。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




