这里主要介绍硅片清洗、刻槽与化学镀,其余工序其他章节都已经介绍,不再重复。
1.硅片清洗 硅片表面有损伤层,油脂。太阳电池制备首先要去掉油脂和损伤层;然后进行标准的RCA清洗(美国无线电公司清洗技术)。
硅片上的油脂、松香、蜡等有机物,可用有机溶剂去除。常用的有机溶剂有甲苯、丙酮、乙醇等。根椐“结构互溶原理”用有机物清洗时,应该按照甲苯-丙酮-乙醇-纯水的顺序进行,而不能打乱顺序。甲苯去污能力最强,但不易用水冲洗,遇水易形成“液珠”;所以要用丙酮继续处理,使残留油脂溶解,甲苯也跟着溶解;乙醇用于处理残留后的丙酮;最后用高纯水将乙醇除尽,达到彻底去油的目的。
接下来的清洗是标准的RCA清洗,主要是清除污染,去除微粒、有机物及无机物金属离子等杂质。这些杂质的污染源来自环境、机台设备、水、化学物品及容器等。在硅片清洗过程中,微粒的去除是最重要的,也是最困难的工作。微粒的来源有诱发性的,也有自发性的。标准的RCA清洗液配方见表7-18。
表7-18标准的RCA清洗液配方
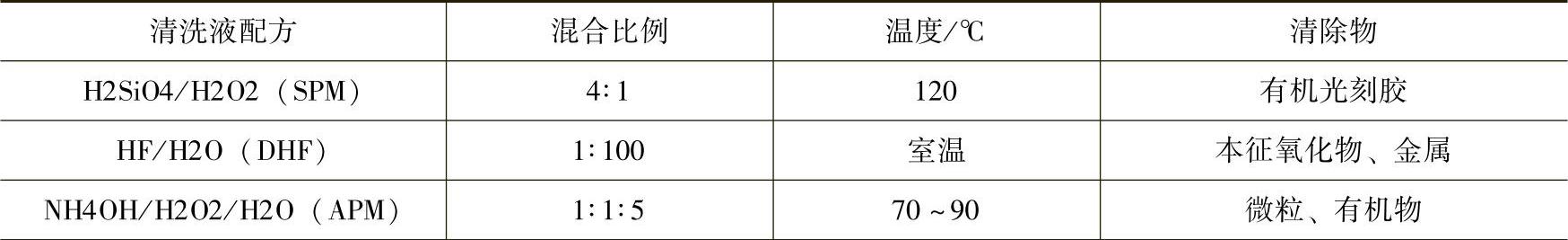
(续)
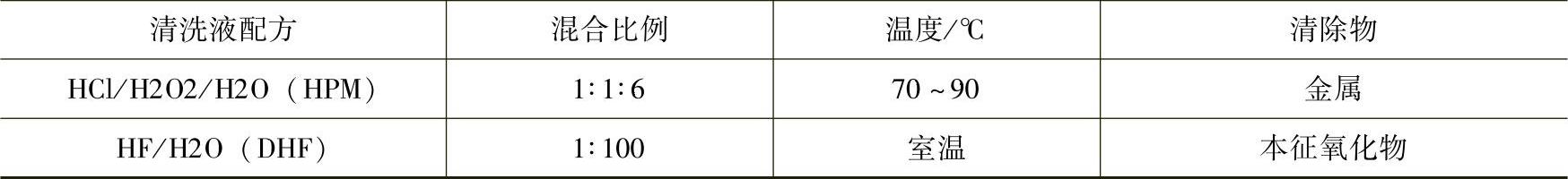
在离子水清洗槽中,超纯水不宜直接冲洗晶片表面。这是因为硅片与岩石、砂土类似,有水蚀作用,遇水喷淋冲洗时易产生微粒污染,而使硅片污染。
2.钝化 用碘酒和氢氟酸(HF)钝化单晶硅表面。晶硅的少子寿命对性能具有很大影响。为了准确测试少子寿命值,必须对晶硅表面进行钝化,减少表面复合的影响。碘酒和氢氟酸具有较好的表面钝化功能。能够很好地复合掉硅体表面的复合中心,其中0.08mol/L的碘酒溶液钝化效果最好,但其稳定性远不如氢氟酸(HF)的钝化效果。
3.刻槽 硅片为FZ单晶硅,掺硼,P型,(100)晶向,电阻率为0.1~1Ω·m,双面抛光,厚度为150~200为μm。。
(1)激光刻槽。采用固体Nd∶YAG-50数控激光划片机,激光波长为1.064μm,利用激光对表面的破坏而形成刻槽。激光打在硅片表面上,为一定深度的硅所吸收,产生高温,发生汽化、溶化现象,在硅片表面上刻出槽来。槽宽主要由激光聚焦系统的好坏决定,槽深主要由激光能量的大小决定。调节激光电流为7.6A,激光前进速度为45mm/s,划出细栅线。主栅线激光电流也为7.6A,激光前进速度也为45mm/s,激光步进长度为45μm,重复六次,刻出合格的主栅线槽。
(2)机械刻槽。采用电子工业中标准的划片机;在满足电流收集要求的基础上,沟槽宽度应尽可能小,但沟槽宽度受划片机刀片厚度制约,刀厚为15μm。沟槽宽度在去除了损伤层后为20~25μm。沟槽的深度应细心控制,以不超过120μm为宜,太深不仅化学镀时间长,硅片在工艺过程中破损率也高,同时过大的金属/半导体接触面会增加界面复合,对电池性能不利。
机械刻槽与激光刻槽比较见表7-19。
表7-19机械刻槽与激光刻槽比较

(3)测试
1)测试条件:光谱质量AM1.5,温度25℃。
2)测试结论:开路电压Voc=681.92mV,短路电流Isc=56.13mA/cm2,填充因子FF=82.02%,转换效率η=20.47%,电池面积A=4cm2。
由前面介绍的工艺流程可知,硅表面织构化(金字塔)→扩散淡磷(POCl3,制成p-n结)→制SiO2(掩膜及反射膜)→机械(激光)刻槽...。经过织构化后,(111)面被暴露出来,并形成随机的金字塔,其尺寸在3~7μm,这种表面织构是光的良好捕集器。刻槽前的工艺是制SiO2(掩膜及反射膜)。SiO2膜具有多种作用:可防止在机械刻槽时污染硅片;可作为化学镀的掩膜;可作为电池发射区的钝化膜。
4.化学镀 正面埋栅及背面电极采用化学镀同时完成。金属电极的要求是:电导率高;与n型硅、p型硅都能形成欧姆接触;与硅粘接性好,不会发生反应;抗电化学能力强。用镍、铜、银为正面电极材料。
(1)化学镀的原理。化学镀依据氧化还原反应原理,利用强还原剂在含有金属离子的溶液中,通过可控制的氧化还原反应,将金属离子还原成金属而沉积在各种材料表面,形成致密镀层。化学镀只需简单地把衬底浸入溶液中,不需要外部电势。
化学镀的优点如下:
1)不需要通电,不需要制作阳极。
2)镀层与基体的结合强度好。
3)可降低电极串联电阻,提高填充因子。
4)成品率高。
5)无毒。
6)投资小,溶液可循环使用。
(2)化学镀镍。化学镀镍与硅结合的牢固程度,取决于硅的表面形态和镍的力学性能。激光刻槽后,槽内残余物的处理、磷硅玻璃的彻底清理,是硅镀镍后良好表面形态的可靠保证。镀镍的力学性能则受到镀液组分、镀镍时的温度、反应速率等因素的影响。化学镀镍液中的主要反应物为金属镍盐和还原剂。还原剂可用次亚磷酸钠。
1)反应式
① 化学沉积Ni-P合金镀液,在加热时不起反应,而是通过镀液的催化作用,次亚磷酸根离子(H2 PO2-)在水溶液水脱氢形成亚磷酸根离子(HPO2-3),同时放出初生态原子氢,即
H2PO2-→PO2-+2[H]
PO2-+H2O→HPO23-+H+
将两式合并,得
H2PO2-+H2O→HPO23-+H++2[H] (7-37)
② 初生态原子氢被吸附到催化金属表面,使其活化,从而使镀液中的镍阳离子(Ni2+)还原,在催化金属表面上沉积金属镍,即
Ni2++2[H]→Ni+2H+
由A和B两个过程的反应机理可以看出:镍阳离子被还原,次亚磷酸根离子被氧化,总反应式为
Ni2++H2PO2-+H2O→HPO23-+3H++Ni (7-38)
2)化学镀镍液类型。有酸性镀镍液和碱性镀镍液两种类型。酸性镀镍液比较稳定,易于控制,虽然用氨水调节pH值,但是在酸性介质中,氨水不易挥发。
碱性镀镍液可使用的pH值比较宽,但是对杂质比较敏感。在反应中温度比较高,其中所含的氨水易挥发,需要不断补充进行调整。
3)化学镀镍溶液的组分及其作用
① 主盐(即镍盐)。一般采用氯化镍或硫酸镍,有时也采用胺基磺酸镍、醋酸镍等无机盐。早期采用氯化镍,但氯化镍会增加镀层应力,现大多采用硫酸镍。
② 还原剂。化学镀镍的反应过程是一个自催化的氧化还原过程。可用的还原剂有次亚磷酸钠、硼氢化钠、烷基胺硼烷及肼等。在这些还原剂中,以次亚磷酸钠用得最多,因为价格便宜,镀液容易控制,镀层抗腐蚀能力好。
③ 络合剂。化学镀镍溶液中的络合剂,除了能控制可供反应的游离镍离子的含量外,还能抑制亚磷酸盐的沉淀,提高镀液的稳定性,延长镀液的使用寿命。有的络合剂还能起到缓冲剂和促进剂的作用,提高镀液的沉积速度。化学镀镍的络合剂一般含有羟基、羧基、氨基等。在镀液配方中,络合剂的量不仅取决于镍离子的含量,而且也取决于自身的化学结构。在镀液中每一个镍离子可与六个水分子微弱结合,当它们被羟基、羧基、氨基取代时,则形成一个稳定的镍配位体。
④ 缓冲剂。由于在化学镀镍反应过程中,副产物氢离子的产生,导致镀液pH值下降。试验表明,每消耗1mol的Ni2+,同时生成3mol的H+,即在1L镀液中,若消耗0.02mol的硫酸镍,就会生成0.06mol的H+。由反应式中可以看出,反应中生成H+会造成pH值的下降,因此必须在溶液中造成酸碱缓冲体系。为了稳定镀速和保证镀层质量,镀液必须具备缓冲能力。缓冲剂能有效地稳定镀液的pH值,使镀液的pH值稳定在正常范围内。另外,为了使反应稳定进行,维持较为稳定的Ni2+含量是十分必要的。为此在溶液中加入络合剂以形成镍络合物。可用柠檬酸盐作为缓冲剂,一方面柠檬酸是三元弱酸,在溶液中柠檬酸离解的各种形态(H3Cit、H2Cit-、HCit2-和Cit3-)同时存在于溶液中,具有良好的缓冲性能,可以在一定范围内维持反应溶液的pH值;另一方面,柠檬酸盐与镍形成弱络合物,随着反应的进行,Ni2+的不断消耗,镍络合物不断解析出Ni2+,可以保持溶液中Ni2+含量在合适的范围。
⑤ 稳定剂。化学镀镍液是一个热力学不稳定体系,当镀液中产生一些有催化效应的活性微粒———催化核心时,镀液容易产生激烈的自催化反应,即自分解反应,产生大量镍、磷黑色粉末,导致镀液寿命终止。在镀液中加入一定量的吸附性强的无机或有机化合物当稳定剂,含量适当时,将会被优先吸附在溶液中形成的微小颗粒上,防止颗粒上继续生成沉淀物,抑止催化反应,从而稳定镀液。钼、铅等重金属离子即为有效的稳定剂,但必须严格控制稳定剂的含量,以防止正常反应被中止。另外必须注意的是,稳定剂是一种化学镀镍毒化剂,即负催化剂,不能使用过量。
⑥ 推荐镀镍液有NiSO4-6H2O、(NH4)2SO4、柠檬酸铵、NaH2PO2及NH3H2O。其中,NH3H2O用来调节溶液中的pH值为8~9,配液的pH值越高,反应速度就越快。镀镍在80℃中的水浴中进行。
⑦ 由于还原剂用次亚磷酸钠,化学镀镍层并不是纯镍,而是含有一定数量磷的镍磷合金,其中磷的含量强烈地受到pH值的影响,含磷量随着pH值的减小而增大。常用的酸性镀镍液产生的沉积镍,含磷的质量分数为7%~10%;常用的碱性镀镍液产生的沉积镍,含磷的质量分数为5%~7%。
在化学镀镍层中不希望有高的拉伸应力,因为它可能导致镀层脱皮、裂纹和起泡,影响槽内硅与镍的结合牢固度。化学镀镍层的拉伸应力随镀液pH值的提高而增加,即随着镀层中磷含量的减少而增加。因此选用pH值低的酸性镀镍液将增加镀层中磷的含量,从而减少镀镍层的内拉伸应力。
从反应式中还可以看出,生成物有亚磷酸盐,因此有可能生成微溶的亚磷酸镍沉淀,妨碍溶液的化学平衡,沉淀物进入镍层还将影响镀层的质量。更为严重的是沉淀物将触发溶液的自发反应,使溶液不稳定。因此可引入合适的螯合剂,减缓沉淀的趋势,保持镀液的稳定性。
4)其他镀镍工艺措施
① 虽然化学镀可以在小孔或槽内形成均匀的镀层,但是反应液必须搅拌,以去除反应形成的气泡,使槽内的溶液及时流动并得到更新。采用空气搅拌不仅可以达到搅拌的目的,而且在溶液中引入空气,与在溶液中加入少量含氧酸盐的阴离子一样,对一般的分解具有稳定作用。(https://www.xing528.com)
② 反应液的pH值越低,生成的镀镍层中的磷含量越高,镍的内拉伸应力越小,因而有利于镍和硅结合的牢固度;但是pH值过低,反应将中止。可将pH值控制在4.6的条件下,这样既能有效提高镍的含磷量,又可使反应在槽内各个部位同时启动。为了使槽内反应均匀进行,并形成致密的镀镍层,可适当降低温度,以减慢反应速度。
③ 为了维持镀液的稳定性,必须保持镀液的适当的负荷(150cm2/L)。D对溶液进行过滤。
5)镀镍后的处理。镀镍后进行烧结,形成的镍硅化合物不仅可以形成良好的屏障,防止铜扩散,而且可以在镍硅间形成良好的机械结合,并减少接触电阻。镍硅化合物NiSi的电阻率为14μΩ·cm。在镀铜前对镍进行活化,增加镍铜之间的结合强度。
6)结果及分析
① 镍层一方面可以改善电极与硅的接触性能,另一方面充当阻挡层,防止铜电极扩散到硅当中。由于镍不是化学镀电极中的主要金属,因此它的厚度不易太厚,浸镀时间为10min为宜。
② 据文献报道,镀镍后在氮气环境中,350~400℃退火5~10min,不仅促进了镍硅化合物的形成,而且改善镍硅的接触性能,改善了电池的填充因子。
③ 镍能否被浸镀到槽内至关重要,镍层质量好坏直接关系到后续能否镀上铜。
(3)化学镀铜
1)溶液配方:硫酸铜(CuSO4.5H2O)8g/L;酒石酸钾钠(EDTA.2Na)42g/L;甲醛(HCHO)(37%)12mL/L;氢氧化钠(NaOH)8g/L;稳定剂适量;十二烷基磺酸钠2g/L。
2)工艺条件:温度25~35℃;pH值11.5~12.5;镀铜时间12h;通气搅拌。
3)溶液配制顺序:先把硫酸铜溶液和酒石酸钾钠溶液混在一起;然后在搅拌的情况下慢慢加入所需要的氢氧化钠;随后用氢氧化钠溶液将其调整至规定的pH值,配成适当的体积;最后加入需要量的甲醛溶液即可。
4)施镀工艺过程:硅片放入溶液后,超声3~4h,施镀工艺过程一直通氧。为了防止氧化亚铜的生成,经12h取出后立即镀银,防止新生态的铜发生氧化。
5)镀铜时的反应机理。化学反应镀铜的历程可概括如下:
自催化反应为
Cu2++2HCHO+4OH-→Cu0+2HCOO-+H2↑+2H2O (7-39)
式(7-39)反应中的阴极反应为Cu2++2e→Cu0
阳极反应为2HCHO+4OH-→2HCOO-+H2↑+2H2O+2e-
除上述主反应外,还会发生如下副反应:
2Cu2++HCHO+5OH-→Cu2O↓+HCOO-+3H2O (7-40)
Cu2O+H2O→Cu0+Cu2++2OH- (7-41)
反应式(7-40)为化学镀铜液中均相氧化还原反应,所产生的Cu2O在碱性溶液中还会发生式(7-41)的歧化反应,而形成铜原子。氧化亚铜粉和金属铜分散在镀液中,将成为镀液自发分解的催化核心,这是化学镀铜液不稳定的根本原因。反应式(7-40)是不可避免的,加入适当的络合剂,可使一价铜成为可溶性的络合物,避免Cu2O的存在和式 (7-41)的歧化反应的发生。另外,甲醛在碱性液中还会发生分子间的氧化还原反应,即康尼查罗反应。
2HCHO+NaOH→CH3OH+HCOONa (7-42)
此反应是一个可逆反应,反应向右进行则消耗甲醛,而且温度越高,平衡常数越大。为了减少甲醛的消耗,可加入反应产物甲醛加以抑止,所以常常在化学镀铜液中增加甲醛量。
6)镀铜液各组分的作用
① 铜盐。提供被沉积的铜离子,可用硫酸铜、醋酸铜或氯化铜等可溶性铜盐。硫酸铜便宜,使用最多。当镀液的pH值保持在工艺范围内时,提高铜盐含量,沉积速度有所增加,但铜盐自分解的倾向也随之加大。
② 还原剂和pH值。目前化学镀铜都以甲醛作为还原剂,而且甲醛的还原能力与镀液的pH值关系很大,pH值越高,则甲醛还原能力越强,沉积速度越快。但同时也增加了铜液自分解的倾向。通常保持pH值在11.5~12.5。当pH值超过13,反应速度过快,则镀液极易分解。
③ 络合剂。添加络合剂的目的,是防止在碱性中发生氢氧化铜沉淀,将铜离子变成络离子状态。常用的络合剂是酒石酸盐和EDTA钠盐。EDTA具有很强的螯合能力,能和多种金属离子发生螯合,在生化实验里经常用到。
④ 稳定剂。镀液不稳定是化学镀铜的最大缺点。在化学镀中,沉积速度同镀液的稳定性往往是相矛盾的,即沉积速度高的化学镀铜,通常稳定性差。
⑤ 附加盐。氢氧化钠是造就化学镀铜的碱性条件,是速度的控制因素,最好的pH值控制范围是12~13,不超过13。
十二烷基磺酸钠为表面活性剂。
(4)化学镀银
1)溶液配方:硝酸银(2%)的体积分数为10%;葡萄糖2∶1(体积比);稀氨水(2%)适量;稀盐酸1∶10(体积比)。
2)工艺条件:温度为水浴加热40℃;镀银时间为10min左右。
3)溶液配制顺序:在2%的硝酸银中,逐滴加入2%稀氨水,直到析出的沉淀恰好溶解为止,所得的澄清溶液即为银氨溶液;然后按比例加入10%的葡萄糖溶液;最后用1∶1的稀盐酸调节pH值为4。
4)施镀工艺过程:把溶液放在聚四氟乙烯材料的容器中,放入硅片,水浴加热到40℃左右,施镀时间10min。
银电极主要用来焊接和防止铜电极被腐蚀。
镀银的速度非常快,2min即可。施镀时应把溶液放进聚四氟乙烯容器,防止银镀在容器器壁上,镀完银后立即用水冲洗,用氮气吹干。
镀银后的SEM照片和镀铜后的SEM照片基本相同,因为镀铜后的镀银层非常薄,施镀时间也短。由EDS图也可以分析银层非常薄,图中可以看出槽的边缘镀层外翻为正常现象。
(5)化学镀存在的问题及解决办法
1)化学镀铜
① 槽内施镀情况。发现槽内出现空洞没有镀满,直接造成电极串联电阻增大。原因是由于沟槽较窄,容易出现毛细现象,开始铜在槽口镀速较快,造成搭桥现象,把槽口遮住。解决的办法是加超声波,加了超声波后镀铜效果很好,见图7-25中,a图未加超声波,与b图加超声波的比较。
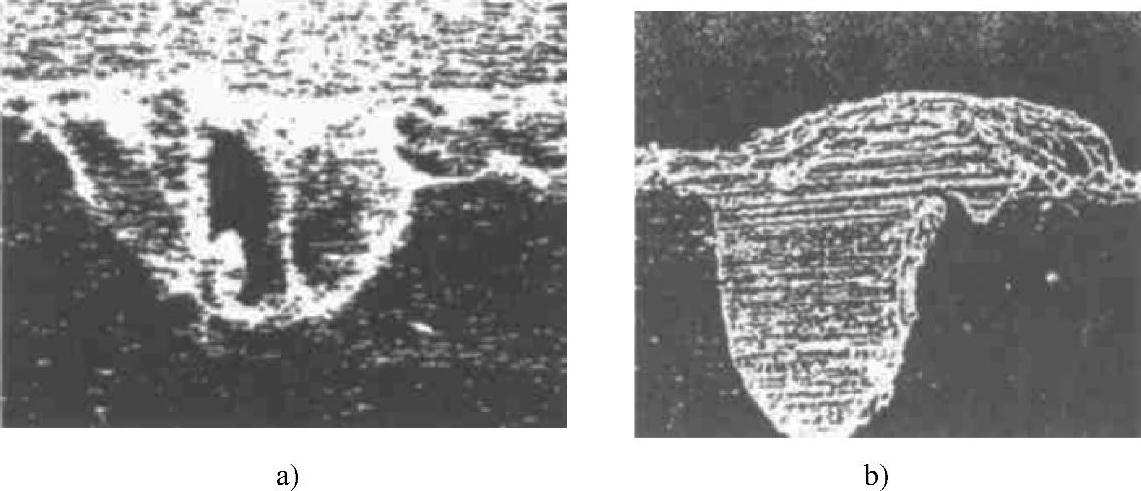
图7-25 化学镀铜
a)未加超声波 b)加超声波
② 化学镀铜最好在聚四氟乙烯容器里进行,这样可降低镀液对槽壁的润湿性,从而可减少金属在其上沉积的可能性,延长镀液的使用寿命。
③ 由于铜是化学镀中的主导金属,所以镀铜时要考虑施镀时间和速度。
④ 如镀铜温度过高,会引起施镀速度加快,且溶液稳定性显著下降,而使槽内出现空洞现象。室温21℃时镀铜需持续12h。如施镀时间太短,则会引起槽内所镀的铜层不满的现象。空洞和镀层不满直接造成电极串联电阻增大,所以激光刻槽时,槽的宽不易太窄。
2)化学镀银。银较易沉积在玻璃上,故用玻璃作容器会导致硅片镀不上银的情况。采用聚四氟乙烯材料的容器,银不易沉积,较易施镀。另外,用氨水作络合剂,使银离子在溶液中以络离子状态出现,可较好地控制反应速度,容易施镀。
5.BCSC制备注意事项
(1)SiO2薄膜的厚度在350~450nm为佳,栅线距离为(1.5±0.2)mm为宜。必须保证NaOH清槽干净,否则后续的化学镀无法进行;铝背场厚度在2μm以上。化学镀镍铜银是高效刻槽埋栅电池(BCSC)制备过程的关键工艺。
(2)激光刻槽时,要求硅片表面平整光滑,而侧壁垂直陡峭。刻槽后的硅片中,由于激光的烧蚀作用,使硅发生熔融,然后冷却而形成损伤层;另外两槽之间的SiO2层上附着大量的残渣,用腐蚀液可以充分地把由于激光刻槽而产生的残留硅渣清除掉,同时对突起的有SiO2薄层保护的基区几乎没有腐蚀。采用体积分数为12%NaOH溶液,55℃条件下清槽。清槽不净则影响化学镀,清槽过度则槽形变形,所以清槽时间的长短要把握好。用BHF溶液
HF∶NH4F∶H2O=3∶6∶10时间太长氧化层腐蚀的厚度增加。氧化层的腐蚀速率非常快,一旦表面的金字塔绒面裸露出来,则前功尽弃。腐蚀速率为1.47nm/s。
(3)氧化层减薄。激光刻槽埋栅的制备工艺结束后,在测试之前还要将氧化层厚度调到最佳值。氧化层作为单层减反射膜,由nd=λ/4知,其最佳厚度d为110nm。另外,要将电池的边缘去掉,以防短路无法准确测试电池的相关性能。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




