进入还原炉的SiHCl3最多只有15%左右转化为多晶硅,剩下的85%用尾气干法回收工艺(CDI)回收利用。干法回收工艺有如下特点:
1)尾气组分回收率高,对主要组分回收率达98%以上。
2)尾气处理量从0%~100%可调。
3)系统自动化程度高。
4)整个系统设备均为常规设备,可靠性高,便于维护。
5)系统温度最低-40℃,对设备材质要求不苛刻。
6)无有毒害废弃物排放。
7)回收物料的品质高,有益于物料再循环利用。
1.尾气干法回收基本知识
1)吸收。吸收是指利用气体混合物在液体中溶解度的差异,使气体中不同组分分离的操作。
2)再生。净化剂使用一段时间后,吸附量达到饱和,因此采用一定的工艺,将净化剂中的杂质和水分除去,使之复活,以便能够再次连续使用,这种复活的过程称为再生。
3)吸附。某些物质的界面,能从周围介质中,把能够降低界面张力的物质,自动地聚集到自己的表面上来,使得这种物质在相表面上的浓度,大于相内部的浓度,这种特性叫吸附。
4)脱吸(解吸)。吸收得到的溶质气体从液体中取出来,这种溶质从溶液里脱离过程称为脱吸(解吸)。
2.干法回收工艺原理 还原尾气中含有H2、HCl、SiHCl3、SiCl4等成分,采用干法回收工艺原理是:冷凝气体分离SiCl4、不凝气体分离H2、HCl利用。
(1)冷凝气体分离SiCl4。还原尾气中的H2、HCl、SiHCl3、SiCl4等成分,经鼓泡、氯硅烷喷淋洗涤、加压并冷却到一定的温度,其中SiHCl3和SiCl4几乎被全部冷凝下来。冷凝后的氯硅烷混合物,经分离塔分离后,分别得到SiHCl3和SiCl4。SiHCl3直接返回还原工序生产多晶硅;SiCl4经氢化部分转化为SiHCl3,再经分离提纯返回还原工序生产多晶硅。
(2)不凝气体分离H2。压缩、冷凝后的不凝气体是H2、HCl。其中的HCl在加压或低温条件下,用SiCl4作为吸收剂,使其溶解在SiCl4中,即HCl被SiCl4所吸收,从而H2被分离出来。被分离出来的H2仍含有微量的HCl,为了避免HCl影响多晶硅的沉积速度,将H2再通过吸收塔,除去微量的HCl,即获得无水分、无其他杂质的纯H2,返回还原工序重复使用。
(3)HCl利用。被SiCl4所吸收的HCl,在升温或减压条件下,可以从SiCl4中脱吸出来。被脱吸出来的HCl在一定压力下冷却至一定温度,可使其中的SiCl4残余组分达到允许程度后,送往氯化合成工序合成SiHCl3,脱吸后的SiCl4用于吸收塔再循环。
3.干法回收工艺流程 图5-50示出干法回收工艺流程。
4.四氯化硅的氢化 冷凝后的氯硅烷混合物,经分离塔分离后,分别得到SiHCl3和SiCl4。SiHCl3直接返回还原工序生产多晶硅;SiCl4经氢化,部分转化为SiHCl3,再经分离提纯返回还原工序生产多晶硅。四氯化硅的氢化是干法回收工艺中的重要部分。
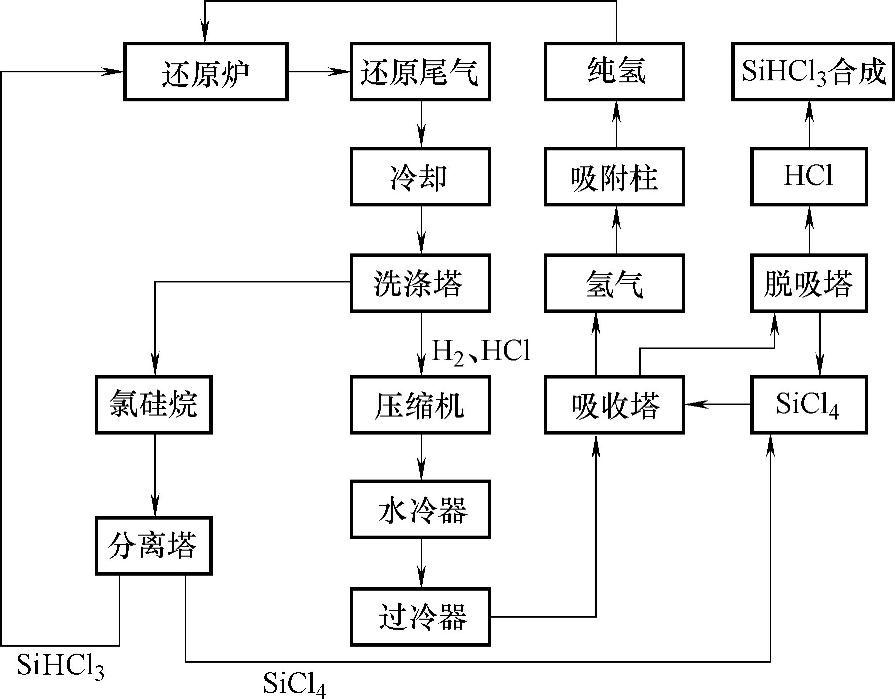
图5-50 干法回收工艺流程
(1)四氯化硅的性质
1)四氯化硅的物化特性
国际编号 81043
CAS号 10026-04-7
中文名称 四氯化硅
英文名称 Silicon Tetrachloride
别名 氯化硅;四氯化矽
分子式 SiCl4
外观与性状 无色或淡黄色发烟液体,有刺激气,易潮解
相对分子量 169.90
蒸气压 55.99kPa(37.8℃)
露点 -70℃
沸点 57.6℃
溶解性 可混溶于苯、氯仿、石油醚等多数有机溶剂
密度 相对密度(水=1)1.48;相对密度(空气=1)5.86
稳定性 稳定
危险标记 20(酸性腐蚀品)
主要用途 用于制取纯硅、硅酸乙酯等,也用于制取烟幕剂
2)四氯化硅对环境影响
①对人体健康的影响。吸入、食入、经皮肤吸收四氯化硅,对眼睛及上呼吸道有强烈刺激作用;高浓度的四氯化硅可引起角膜浑浊、呼吸道炎症,甚至肺水肿;皮肤接触后可引起组织坏死。
②对环境的影响。四氯化硅受热或遇水分解放热,放出有毒的腐蚀性烟气。燃烧产生氯化氢、氧化硅对环境造成有害的影响。
3)监测方法。采用气相色谱法进行色谱分析。具体方法见《分析化学手册》[1]。
(2)四氯化硅的冷氢化。用西门子法生产工艺制备多晶硅,每生产1kg产品,要产生10kg左右的四氯化硅。冷氢化就是将四氯化硅、硅粉和氢气在一定温度、压力及摩尔配比下,使四氯化硅部分转化为三氯化硅。这种方法实际上就是三氯化硅热分解的逆过程。
1)原理。主要反应如下:
3SiCl4+Si+2H2=4SiHCl3 (5-80)
平衡常数Kp为
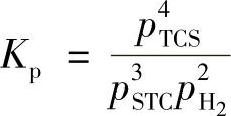
式中pTCS———三氯氢硅的分压;(https://www.xing528.com)
pSTC———四氯化硅的分压;
pH2———氢气的分压。
2)工艺流程。图5-51示出四氯化硅氢化工艺流程。将H2和SiCl4按规定配比和压力进入混合器,在混合器内加热到120℃左右;然后在预热器内加热H2和SiCl4混合气体到400℃左右,气体进入氢化反应炉(流化床),在适当的温度和压力下,与干燥硅粉(含催化剂)进行反应;从氢化反应炉出来的气体(粉尘、SiHCl3、SiCl4、H2),经除尘过滤,然后依次进入水冷器、一级深冷(-30℃)、二级深冷(-45℃),得到的液态硅氢化物进入分离塔,未反应的SiCl4循环使用,未反应的H2经活性炭吸附后循环使用。
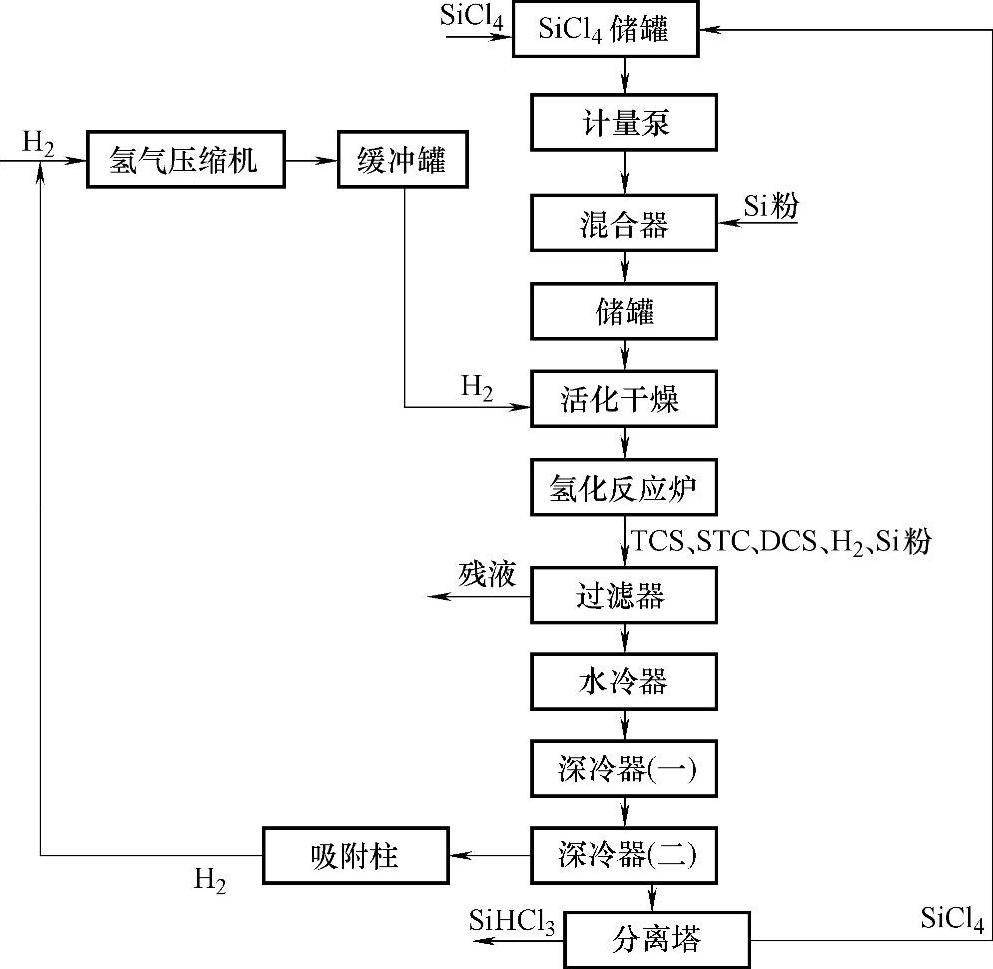
图5-51 四氯化硅氢化工艺流程
3)工艺条件
①反应温度。温度太高,则三氯化硅容易分解,对催化剂的损害较大;温度太低,则反应速率过低,催化剂的催化作用不明显。所以需要选择适当的温度,以提高四氯化硅的转化率。温度控制范围在500℃左右。
②压力。对于有气体参加的反应,根据化学反应平衡原理,生成三氯化硅反应是气体分子数减少的反应,也就是体积减小的反应,因此加压有利于三氯化硅的生成。压力为1.3~1.5MPa。
③物料配比。H2∶SiCl4=2∶1(摩尔比);SiCl4∶Si(粉)=3∶1(摩尔比);催化剂:Si(粉)=2%(质量比)。
④接触时间≥20s。
4)主要原辅材料技术要求如下:
①SiCl4含量(质量分数,下同)≥98%。
②Si(粉)粒度约80目(约190um),硅含量﹥99%。
③氢气露点≤-40℃,氧含量≤5×10-6,压力1.5MPa。
④氮气(N2)含量≥99.95%,露点-40℃。
⑤活性炭粒度8~24目,含量﹥95%,充填密度﹥0.3kg/cm3,干燥减量≤10%。
⑥苯吸附量≥450mL/cm3,强度(球磨法耐破碎性)≥90%,pH=7。
⑦催化剂平均粒度比硅粉大20目(Ne-9-2有机加氢催化剂)。
⑧蒸气压力0.3~0.5MPa(表压),温度140℃。
5)在目前工艺条件下,每生产1kg SiHCl3的原料消耗量如下:硅粉0.08~0.15kg/kg(SiHCl3);氢气(标准状况)0.4~0.8m3/kg(SiHCl3);氮气(标准状况)0.08~0.15m3/kg(SiHCl3);蒸气8~10kg/kg(SiHCl3);催化剂0.003~0.005kg/kg(SiHCl3);电4.5~5kW·h/kg(SiHCl3)。
6)主要设备:氢气压缩机、冷冻机、气体混合器(H2和SiCl4)、氢化反应炉(流化床)、除尘过滤器(袋式过滤器)、列管式冷凝器、分离塔(湍流式筛板塔)。
7)操作要求
①开车前严格按规定进行试压检漏。
②开车前必须用氮气赶气。
③首次开车必须向氢化反应炉(流化床)内加入适量的硅粉。
④H2、SiCl4、SiH2Cl2易燃、易爆,一旦着火,必须用干粉或氮气灭火,严禁用水灭火。
⑤粉尘和废气必须淋洗后放空,废水排放要达到标准:pH=6.5~7.5,悬浮物≤70mg/L。
5.干法回收工艺主要设备 其主要设备包括鼓泡系统、压缩和过冷系统、吸收塔系统、活性炭吸附系统、脱吸塔系统的设备。
(1)鼓泡系统的设备。有鼓泡气-气换热器、鼓泡塔、氯硅烷储罐、氯硅烷泵、氯硅烷换热器、氯硅烷计量泵。
作用:还原尾气中的H2、HCl、SiCl4、SiHCl3等通过以上设备,在一定压力、温度、流量、液位下,得到充分的鼓泡、洗涤后,将大部分氯硅烷冷却至氯硅烷储罐;当储罐达到一定液位时,将氯硅烷输送到分离塔;根据SiHCl3和SiCl4的沸点不同(31.5℃,57℃),在分离塔中把SiHCl3分离出来。返回还原工序生产多晶硅,SiCl4送氢化工序转化为SiHCl3,提纯后返回还原工序生产多晶硅。还原尾气中的H2、HCl沸点低,鼓泡系统的压力、温度不能将其冷凝,从而达到气、液分离。经过鼓泡、洗涤后的H2、HCl和少量的氯硅烷进入干法回收工艺的压缩部分。
(2)压缩和过冷系统的设备。有氢压机、水冷器、压缩气-吸收气换热器、压缩过冷器。
作用:把不凝气体H2、HCl和少量的氯硅烷升压,以满足吸收塔的工艺要求,同时将少量的氯硅烷冷凝下来,余下H2、HCl气体进入吸收塔。
(3)吸收塔系统的设备。有吸收塔、富液储罐、富液泵、一级富液、贫液交换器、二级富液、贫液交换器。
作用:H2、HCl进入吸收塔内,在一定压力、温度、流量下,用SiCl4作为吸收剂,使其溶解在其中,即HCl气体被吸收,从而H2被分离出来。被分离出来的H2中仍含有微量的HCl,需进入活性炭吸附柱,除去微量的HCl。
(4)活性炭吸附系统的设备。有三套吸附柱、热油泵、冷油泵、水冷器、膨胀油槽。
作用:除去H2中微量的HCl。为了避免HCl影响多晶硅的沉积速度,从而得到无水分、无其他杂质、满足还原工序生产的高纯H2。活性炭在正常生产过程中,使用一段时间后,吸附量会接近或达到饱和,吸附HCl的能力会降低,影响生产质量。为了保证活性炭的活性,在生产中,吸附柱轮流使用,吸附能力下降的吸附柱随即使之再生。
(5)脱吸塔系统的设备。有脱吸塔、再沸器、冷凝器、冷凝液储罐、汽化器、水冷却器、贫液过冷器、贫富液交换器。
作用:在一定压力、温度、流量下,将HCl从SiCl4中脱吸出来。被脱吸出来的HCl又在一定压力下冷凝至一定温度,可使其中的氯硅烷残余组分达到允许程度后,将HCl送氯化氢合成工序合成SiHCl3。脱吸后的SiCl4(贫液)用于吸收塔再循环,作为吸收剂溶解HCl。
6.四氯化硅的热氢化 热氢化又名直接氢化。即将四氯化硅和氢气按一定配比,在一定压力、温度条件下,使SiCl4部分转化为SiHCl3。其主要化学反应如下:
SiCl4(g)+H2(g)=SiHCl3(g)+HCl(g)(5-81)
(1)工艺流程。图5-52示出热氢化工艺流程。氢气(H2)和四氯化硅(SiCl4)经缓冲罐进入四氯化硅汽化器,使SiCl4汽化。SiCl4与H2的混合气进入氢化反应炉,反应尾气H2、HCl、SiCl4、SiHCl3经冷凝器冷却之后,进入干法回收系统(CDI)。该系统对H2、HCl、SiCl4、SiHCl3进行分离,H2和SiCl4循环使用,SiHCl3送多晶硅制备工艺,HCl进入三氯化硅合成工艺,废气进淋洗塔处理后放空。
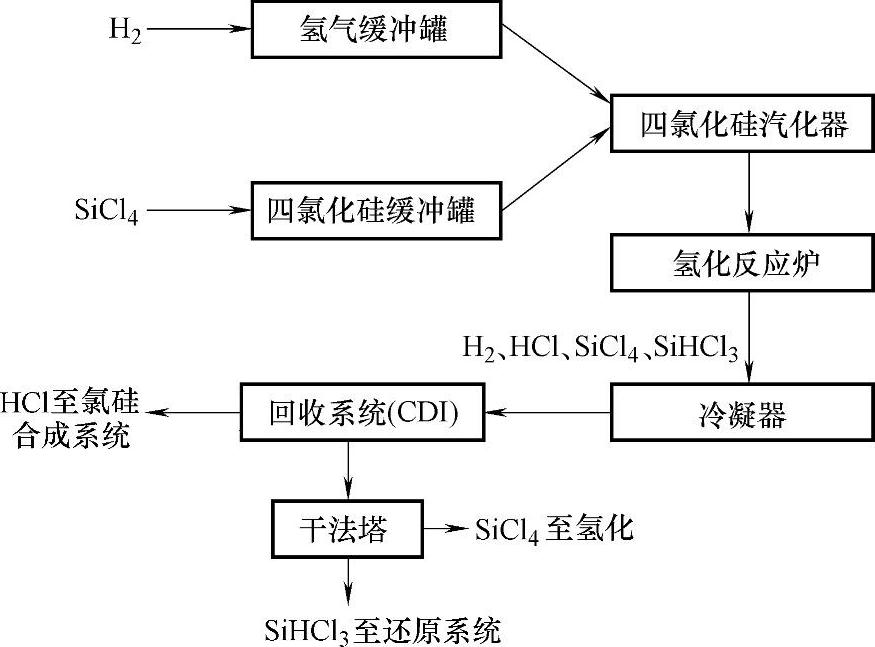
图5-52 热氢化工艺流程
(2)主要设备。有氢气压缩机、SiCl4输送泵、SiCl4汽化器、氢化反应炉、冷凝器和一个很大的干法回收系统(CDI)。
氢化反应炉为钟罩式,内有保温套和加热器(石墨加热器)。干法回收系统(CDI)包括氢气压缩机、冷冻机(螺杆式)、吸收塔、解吸塔、吸附柱、过滤器及干法塔等设备。
(3)主要原辅材料技术要求。四氯化硅(SiCl4)含量(质量分数,下同)﹥96%;氢气露点≤-60℃,氧含量≤5×10-6,压力0.6MPa。
(4)每千克SiHCl3耗电。按SiCl4转化率14%计算(转化率一般在12%~18%之间),每千克SiHCl3耗电约为10kW·h。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




