氢气是生产多晶硅的基本原料。制备多晶硅首先要掌握氢气的制备技术。
氢是元素周期表中的一号元素。1766年,英国的物理学家和化学家卡文迪什(H.Cavendish)用六种相似的反应制出了氢气,即用锌、铁、锡等与盐酸或稀硫酸反应制出氢气。他认为氢气是一种“可燃空气”。1785年,化学家拉瓦锡(A.L.Lavoisier)指出,水是氢和氧的化合物,氢是一种元素,他将“可燃空气”命名为“Hydrogen”,元素符号为“H”。
1.氢气的物理化学性质
(1)氢气的物理性质。H2,单质氢,以双原子形式存在,无色、无味、难溶于水,是密度最小的气体。在标准状况下,1L氢气的质量是0.0899g,比空气轻得多;在10.1MPa压强下,温度-252.87℃时,氢气可转变成无色的液体,-259.1℃时变成雪状固体。
(2)氢气的化学性质。氢分子H-H键能较高,为432kJ/mol,所以常温下很稳定。加热时有许多化学性质:可燃性、还原性、氧化性、化合反应、金属氢化物等。
1)氢的可燃性。氢气燃烧时是无声的,同时会产生蓝色的火焰。氢气是一种很有用的燃料。在煤气中就含有超过百分之五十的氢。氢气燃烧时所产生的高温,足以把金属熔化。工业上常用氢气切割或焊接金属。氢气在空气里的燃烧,实际上是与空气里的氧气发生反应,生成水。
2H2+O2=2H2O (5-22)
这一反应过程中有大量热放出,是相同条件下汽油的三倍。因此可用作高能燃料,在火箭上使用,我国长征3号火箭就用液氢燃料。不纯的H2点燃时会发生爆炸,但有一个极限,当空气中所含氢气的体积占混合体积的4%~74.2%时,点燃都会产生爆炸,这个体积分数范围叫爆炸极限。用试管收集一试管氢气,然后用燃着木条放到试管口,如果听到轻微的“噗”声,表明氢气是纯净的。如果听到尖锐的爆鸣声,表明氢气不纯,这时需要重新收集和检验。
2)还原性。氢气与氧化铜的反应为
CuO+H2=Cu+H2O (5-23)
反应的实质是氢气夺取氧化铜中的氧生成水,使氧化铜变为红色的金属铜。在这个反应中,氧化铜失去氧变成铜,氧化铜被还原了,即氧化铜发生了还原反应。这种含氧化合物失去氧的反应,叫做还原反应。能夺取含氧化物里的氧,使它发生还原反应是的物质,叫做还原剂。
3)氧化性氢可以与活泼金属相互反应,生成离子型氢化物。例如钠与氢反应,生成氢化钠,氢接受电子生成负一价氢离子,显示氢的氧化性。

4)有机化合物及金属氢化物。在适当温度及催化剂的条件下,氢可以和一氧化碳合成一系列有机化合物;氢气可以与某些金属反应,生成外观似金属的金属型氢化物。
5)聚变反应。氢元素中的重氢(又称氘)是制造氢弹的主要原料,它们的原子核聚合到一块所释放的聚变能很大。1kg氘通过聚变反应释放的能量,与12t标准煤相当,比核电站反应堆里发生的裂变反应的能量大4倍。海水里含有几十万亿吨氘,按世界上目前的能耗水平计算,海水中的氘可供人类使用几百亿年。
2.氢气的工业制备 氢气的工业制备有很多种方法,有电解水、高温电解水蒸气、热化学分解水、生物制氢、氨分解制氢、水煤气制氢、甲醇裂解制氢等。表5-5列出氢气制备方法。
表5-5氢气制备方法

多晶硅企业一般是用电解水工艺制氢,由电解槽阴极生成的氢气导入氢气总管,然后净化处理。电解槽是电解水制氢的关键设备,是发生电化学反应的地方,有碱式电解槽、聚合物薄膜电解槽和固体氧化物电解槽等,比较实用的是碱式电解槽。
碱式电解槽主要由电源、电解槽箱体、电解液、阴极、阳级和横隔膜组成。电解液是氢氧化钾(KOH)溶液,浓度为20%~30%,其作用是增大水的电导率。横隔膜最早由石棉组成,其作用是分离气体。电极是由金属组成,其作用是分解水。图5-17示出碱性电解槽原理。
在70~100℃温度、100~3000kPa压力下,阴极两个水分子(H2O)被分解为两个氢离子(H+)和两个氢氧根离子(OH-);氢离子得到电子生成氢原子(H),并进一步生成氢分子(H2);两个氢氧根离子则在阴、阳极之间的电场作用下,穿过多孔的横隔膜,到达阳极,在阳极失去两个电子,生成一个水分子和1/2个氧分子
阴极产氢2K++2H2O+2e-→2KOH+H2 (5-25)
阳极产氢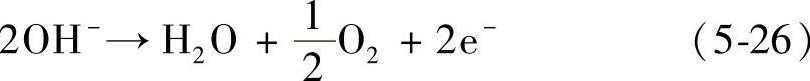 (https://www.xing528.com)
(https://www.xing528.com)
实际使用的双极碱性电解槽见图5-18。双极碱性电解槽电极是串联的,结构紧凑,减小了因电解液的电阻而引起的损失。为了提高电解槽的效率,需要减小电解槽电压。采取的技术措施有:采用新的电极材料,如Raney Nickel(雷尼镍)、Ni-Mo(镍-钼)、Ni-Cr-Fe(镍-铬-铁),能有效加快水的分解;新的横隔膜材料采用聚合物,聚合物化学、力学性能稳定,气体不易穿透。
3.氢气的净化 氢气的净化就是要除去氢气中的氧气、水及杂质。氢气的净化方法分物理法和化学法。物理法有净化剂吸附、变压吸咐、低温分离、膜分离和钯金属;化学法有金属氧化物法。具体方法要根据工业氢气中的杂质种类来选用。电解水的杂质较少,因此采用吸附法,即常用的催化剂脱氧吸附干燥法。其原理是利用氢和氧在Ni-Cr催化剂作用下转化为水;然后通过各种吸附剂将水等杂质吸附,并通过过滤器除去氢气中的固体微粒,从而达到提纯氢气的目的。工艺如下:
H2→阻火器→除油器→Ni-Cr催化→水冷器→加热器→硅胶→钯催化→水冷器→硅胶→分子筛→粗过滤→精过滤→纯H2
净化剂必须是高纯度的,不与氢气发生反应;净化速度快,能连续使用,便于活化和再生。净化剂的安装顺序是先脱氧后除水,工作中严禁空气吸入净化系统。新装的净化剂由于在空气中氧化或吸水,使用前应进行活化。再生方法与再生程度决定于净化剂的性质,再生的程度和时间应根据净化剂性能与能量、吸水量等条件确定,一般以彻底除去杂质为原则。
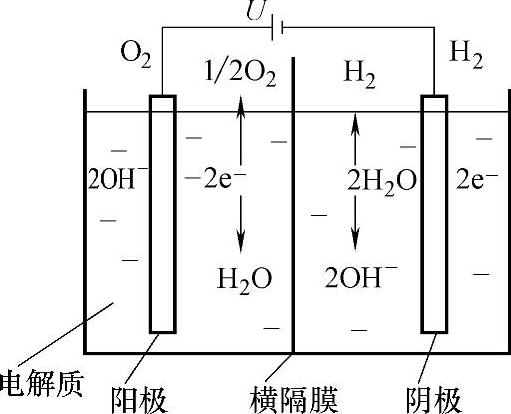
图5-17 碱性电解槽原理
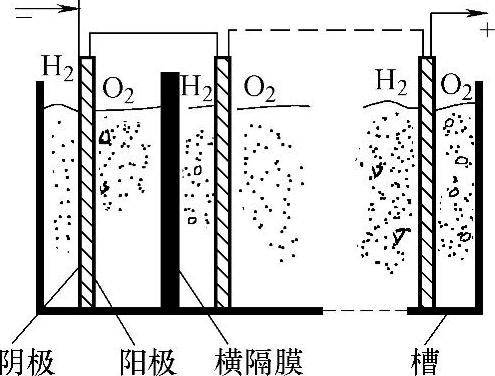
图5-18 双极碱性电解槽
4.氢气的贮存运输
(1)贮存。主要有液化贮存和氢化金属贮存。
1)液化贮存。将氢气冷却到-253℃,即呈液态。可将其贮存在高真空的绝热容器中。但贮存成本高,安全技术较复杂,用于宇航中。
二氧化硅微珠液氢贮存罐不用抽真空,优于高真空的绝热容器。这种二氧化硅微珠直径为30~150μm,空心的,壁厚1~5μm,热导率极小,可抑制颗粒间的对流换热;在部分微珠上镀1 um的铝,以3%~5%的比例,混入不镀铝的微珠中,可有效地切断辐射传热。
2)氢化金属贮存。贮存原理:氢与氢化金属之间可以进行可逆反应,当氢和氢化金属构成氢化物时,氢就以固态结合的金属氧化物形式贮存;当外界有热量加给金属氧化物时,它就分解为氢化金属并放出氢气。氢化金属有四种:铁-钛系、稀土镧镍、镁系、钒铌锆多元素系。
①铁-钛系。贮氢量大,每千克可贮氢612L;价格低,活性大,在常温常压下释放氢。
②稀土镧镍。每千克可贮氢153L。
③镁系。储氢量最大,但要在287℃下才能释放氢,且吸收氢十分缓慢。
④钒铌锆多元素系。本身是稀有金属,只适用于特殊场合。
(2)运输。主要有管道氢气运输和高压气瓶运输。
1)管道氢气运输。氢气可以像天然气一样用管道运输,但是氢气压缩泵功率是天然气压缩泵功率的三倍,且氢气管道密封要严于天然气管道密封。这主要是两种气体密度不一样,导致气体扩散效果不一样。
2)高压气瓶运输。将氢气在15.2~40.5MPa压力下装进高压气瓶运输,方便可靠。该法效率低,氢气重量在运输工具重量中只占2%~4%,40.5MPa压力下只能装2.5kg的氢气。
5.氢气的安全使用 氢气与其他气体按一定的比例混合将发生爆炸,使用时要制定严格的管理制度和安全措施。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




