巨噬细胞是粥样硬化斑块的主要成分,由血液单核细胞形成。在粥样硬化病变的早期,巨噬细胞出现在病变区域,在斑块发展的进程中,巨噬细胞渗入斑块纤维帽导致基质金属蛋白酶(Matrix Metalloproteinases,MMPS)释放,使得纤维帽脆弱进而导致斑块破裂[43]。很明显,巨噬细胞的分布和活动提供了斑块进展的重要信息,因此需要开发对斑块的细胞成像方法。
在IVPA成像中,可以通过引入造影剂进一步增强动脉组织不同成分之间的光吸收差异。相对于传统的染料,金属纳米粒子的光吸收效率更高,且可以通过改变纳米粒子的形状和大小对其吸收光谱进行调整,它们趋向于聚集在斑块活跃的巨噬细胞体内,对于分子IV-PA成像而言是一种有效的造影剂[44]。Wang等[45]分别在532nm和680nm处对含4个内室的动脉模型成像,其中4个内室分别含有一定浓度的金纳米粒子、明胶、含有金纳米粒子的小鼠巨噬细胞和不含金纳米粒子的小鼠巨噬细胞。IVUS/IVPA组合图像说明在532nm处在含有金纳米粒子的巨噬细胞和金纳米粒子内室处均有IVPA信号,在680nm时只有含金纳米粒子的巨噬细胞处有IVPA信号,这是因为金纳米粒子在装载进巨噬细胞后其光谱发生了变化。他们分别在700nm、750nm、800nm下,对在内膜和外膜均注射了含金纳米粒子巨噬细胞的兔粥样硬化动脉进行IVUS/IVPA组合成像。结果表明在700nm处,注射了巨噬细胞的位置有强IVPA信号;而在800nm处,注射位置的IVPA信号几乎不可见,如图6-5所示。上述结果说明可以通过使用造影剂对巨噬细胞进行分子成像,了解斑块进展程度。此后,该研究小组又用波长为680 nm的激光,对4个内室均为含金纳米粒子的巨噬细胞的动脉模型进行IVUS/IVPA组合成像,4个内室中每个细胞内的金纳米粒子数不同且细胞浓度不同。结果表明单个细胞内金纳米粒子多的内室IVPA信号强,而且他们的实验还证明在有金纳米粒子这种高光吸收物时IVPA成像仍是安全的[46]。
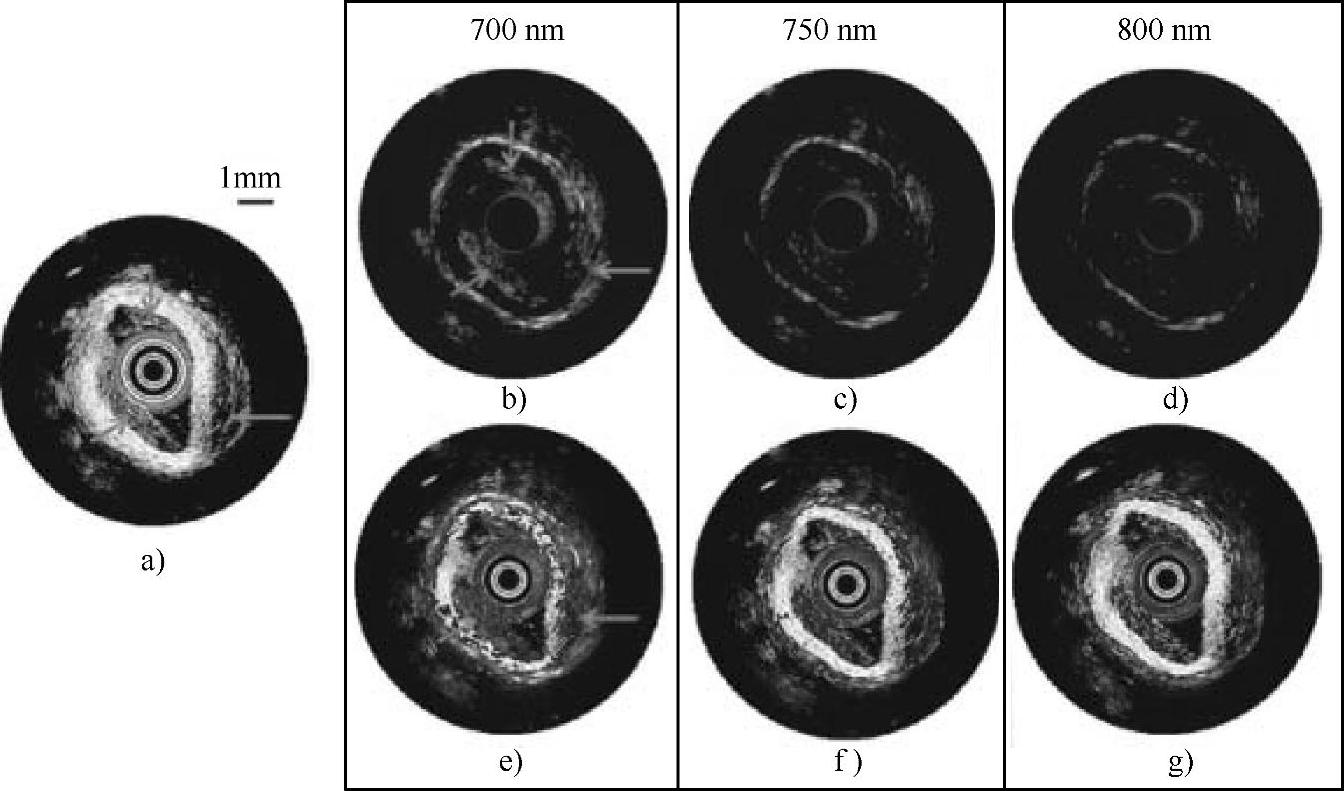
图6-5 内膜和外膜均注射了含金纳米粒子巨噬细胞的兔粥样硬化动脉图像(箭头标记的为注射位置)[45](https://www.xing528.com)
a)IVUS图像 b)~d)不同波长的IVPA图像 e)~g)不同波长的IVUS/IVPA组合图像
Doug等[47]在实验中发现二氧化硅包裹的金纳米棒被红外激光照射导致的温度变化与IVPA信号强度有线性关系,且斜率比样本组织的斜率大。证明在IVUS/IVPA组合成像中,金纳米粒子可在激光照射期间用于局部温度监测,将连续激光器与集成导管结合可有选择地加热金纳米粒子造影剂,并同时对斑块进行温度监测。
虽然使用造影剂可以提高光声图像的对比度,但由于背景组织的内源性生色团体积较大,其光学吸收仍会显著降低光声成像的对比度和分辨率。脂质体纳米粒子(Liposomal NanoParticle,LNP)同时具有光吸收性和磁性,Qu等[48]介绍了使用LNP的磁光声(Magne-toPhoto-Acoustic,MPA)组合成像,即磁超声和PA成像的组合。他们将LNP注入小鼠体内的肿瘤中,由于肿瘤附近组织和LNP之间显著的磁特性差异,LNP的磁动超声(Magneto-Motive UltraSound,MMUS)信号抑制了背景组织产生的PA信号,从而提高了成像的对比度。该实验说明使用双对比纳米粒子可得到高对比度的MPA图像,将其应用于血管内的粥样硬化斑块成像,可提高图像对比度。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




