偶极矩的理论计算是根据正负电荷中心距离与电量的乘积得到,所以仅简单地反映单分子的极化性质,对解释分子的电荷分布具有重要意义。所有化合物在激发态的偶极矩都主要是由X轴方向(即横向)电子重排引起偶极矩增大且电荷中心位置的变化而强于基态,激发过程伴随着偶极矩的增加,其中偶极矩差距最大的是E和E*。
当分子从基态E被激发到E*时,分子内部的电荷从羟基转移至胺基,改变了分子内氢键中氢的“受力平衡”,质子给体(羟基)所带的负电荷减少,基团酸性增强;而质子受体(胺基)所带的负电荷增加,基团碱性增强,促使激发态平衡结构的改变,以便质子转移过程的顺利进行。同时,质子转移也是一个偶极矩增大、正负电荷中心分离的过程,所以激发态的反应更容易受到溶剂极化作用[293-295]。极性增大,利于电荷的分离,可以推测极性溶剂中将更利于质子转移的进行。这是由于能发生质子转移的分子从基态跃迁至激发态时,存在偶极矩变化,因此在与其包围的溶剂分子的偶极-偶极相互作用下,激发态分子发生几何变形且能量降低。推测随着溶剂极性的增加,分子基态至激发态的跃迁与衰变将变得容易,其吸收、发射光谱发生红移。
激发引起的成键原子的结构变化可以从电子跃迁涉及的轨道成键性质的变化来解释。电子跃迁引起了电子的重排、电子密度的重新分配,从而影响分子结构[296]。同时,根据福井谦一提出的前线轨道理论,分子能级的跃迁又和前线轨道性质密切相关:对于大多数化学反应而言,反应在一个反应物的HOMO(最高占有分子轨道轨道)与另一个反应物的LUMO(最低未占有分子轨道)能够产生最大的重叠位置及方向上发生。亲核反应物主要以其HOMO参与反应,亲电反应物主要以其LUMO参与反应,含有单占据分子轨道(SOMO)的反应物以其HOMO或LUMO或两者同时参与反应,这些特殊的分子轨道统称为前线轨道。当HOMO→LUMO跃迁引起的成键性质消失时,相关的键变长;反之,相关的键变短。在HF和CIS水平下得到的烯醇式分子在基态和激发态的HOMO和LUMO的定性表示(如图3.5)。比较分子在基态和激发态的前线轨道的成分即可定性而直观地判断其S1态的电荷转移方向和大小。
主要选取了目标化合物C1、C3、C5、C7、C9的偶极矩以及前线轨道理论计算结果作为研究代表,从偶极矩结果看到,由于目标化合物均由脂肪链链接,其柔软性要好很多,相应的共轭性就差很多,所以整个分子的电子流转也不如芳香环取代的分子,其在偶极矩上仅表现出来较微小的差距,其中C9分子由于脂肪链端含有一个苯环,所以其电荷分散程度稍大一点(ΔμE [D]≈0.25)。我们推测其受溶剂极性的影响稍大一些,但总体上来说,此类分子在相同化学环境下的化学性质不会有特别明显的变化。
表3.2 化合物C1、C3、C5、C3、C7在基态和激发态时各互变异构体的偶极矩 (https://www.xing528.com)

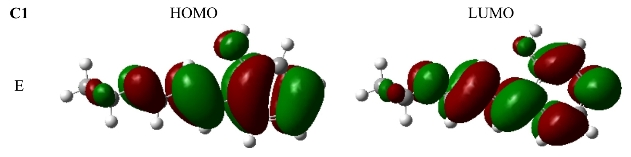
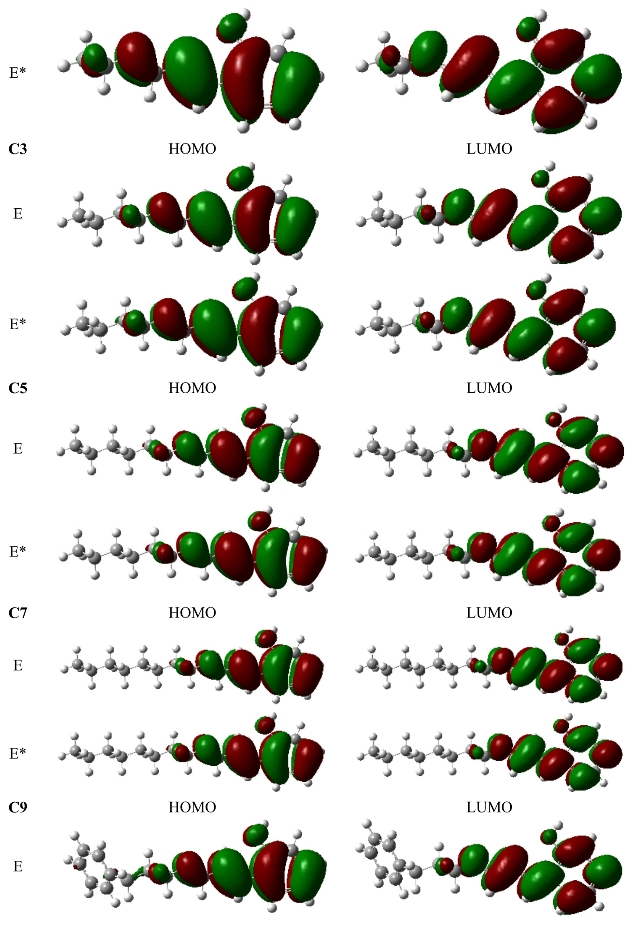
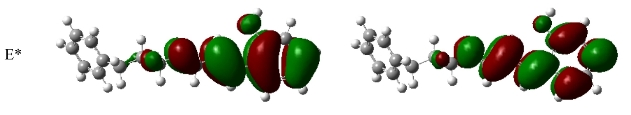
图3.5 化合物C1、C3、C5、C7、C9在基态和激发态时的前线轨道定性表示
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




