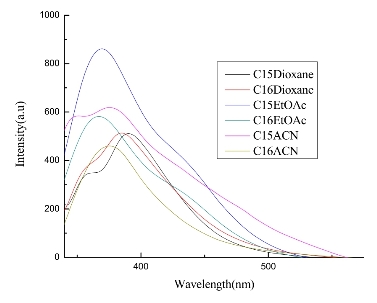
图2.22 化合物C15和C16在多种非质子性溶剂中的荧光发射光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为5/10 nm)
基于化合物C11—C18的紫外吸收光谱图,选择了320 nm作为激发波长,以目标化合物C15/C16为例研究其在极性相对较低的非质子性溶剂中的单光子荧光发射光谱(如图2.22)。可以发现其在极性相对较小的非质子溶剂中,在350~450 nm范围内均有一个荧光发射带,这是由于分子的CT*→CT的辐射跃迁引起的,属于正常的荧光发射带。但是在DMF、DMSO等极性较大的非质子性溶剂中,目标化合物除了表现出正常的荧光发射峰外,还在525 nm处展现出一个新的发射峰(详情如图2.21)。
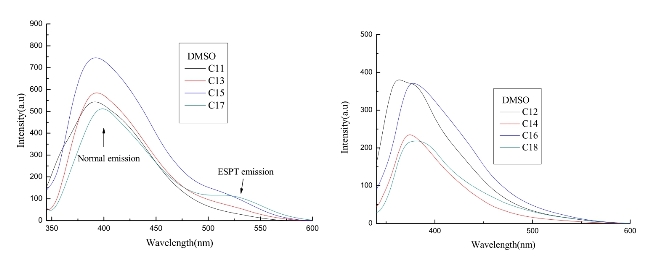
图2.23 化合物C11—C18在DMSO溶剂中的荧光光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为5/10 nm)
以DMSO溶剂为例,考察不同目标化合物在强极性的非质子溶剂中的荧光发射光谱(如图2.23,表2.7—2.10)。化合物C11、C13、C15、C17均展现出独特的双荧光发射带。其一是激发态分子电荷转移峰(CT*→CT),而第二个荧光发射带较第一个有100 nm左右的红移,这是因为在强极性的DMF、DMSO溶剂中,由于N、S等杂原子的存在,导致目标化合物分子间氢键作用增强,进而发生了ESPT反应引起的K*-K的非正常荧光发射峰。另外,作为参比化合物的C12、C14、C16、C18均表现出单一的CT*→CT荧光发射带。通过对比化合物结构也可以发现,由于目标化合物亦存在-OH、-C=N基团,其存在形成了分子间氢键的客观条件,这也是参比化合物不具备的。
从图2.23中可以看到,在DMSO中化合物C11的最大荧光发射波长为390/519 nm,IE*/IN* 值为0.0676,化合物C12的最大荧光发射波长为372 nm;化合物 C13的最大荧光发射波长为392/522 nm,IE*/IN*值为0.127,化合物C14的最大荧光发射波长为379 nm;化合物C15的最大荧光发射波长为393/523 nm,IE*/IN* 值为0.168,化合物C16的最大荧光发射波长为378 nm;化合物C17的最大荧光发射波长为399/525 nm,IE*/IN* 值为0.221,化合物C18的最大荧光发射波长为380 nm。可以看到目标化合物在随着分子烷基链的增长,IE*/IN* 值也逐渐变大,可见其分子间氢键作用在不断增强,因此发生ESPT反应的能力也相应增大。
随着分子中脂肪链的增长,化合物分子间-OH、-C=N键相互作用的位阻就变小了,更利于之前设想的由分子间氢键链接的“二聚体”或者类似“三明治”结构的多聚体的形成。由于目标化合物结构相似,所以其荧光发射带也没有太大变化。另外,还看到参比化合物展现的单一的正常荧光发射峰的位置在372~380 nm之间,随着分子中非共轭碳链的增加也发生了较小的红移,这主要是因为参比化合物整个分子碳链的增长电子转移难度增大,但分子空间位阻减小,对称性更好了所致。
值得指出的是,非共轭的双邻羟基-苯基乙烯基亚氨基片段取代化合物(C11—C18),在强极性的DMF、DMSO等溶剂中发生ESPT反应的能力随着非共轭碳链的增长而增大(C11<C13<C15<C17);而同类型单取代的目标化合物(C1—C8)则恰恰相反(C7<C5<C3<C1)。这主要是因为在双取代目标化合物中,非共轭碳链的增长减少了分子内氢键作用的可能性,而且非共轭碳链越长,双羟基-亚胺基间位阻也越小,因此越有利于ESPT反应的发生。相反在单取代目标化合物中,由于单取代非共轭碳链的增长,其柔软性增加,碳链卷曲或者扭转的可能性更大,空间位阻也可能越大,因此发生ESPT反应的能力相应减弱,结合化合物C1和C9的单晶数据也可以证明。
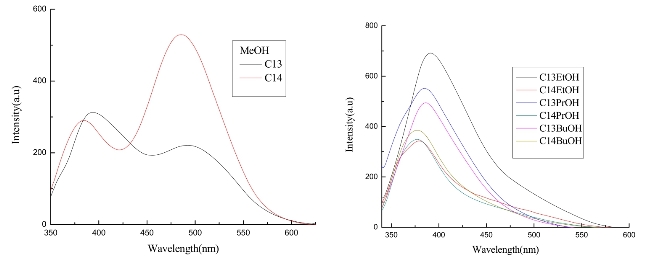
图2.24 化合物C13和C14在质子性溶剂中的荧光光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为5/5 nm)
此外,本节还研究了化合物在不同质子性溶剂中的荧光光谱图(如图2.24)。同样以目标化合物C13和C14为例进行分析,可以看到在甲醇中化合物C13的最大荧光发射波长为393/495 nm,C14的最大荧光发射波长为385/484 nm;乙醇中化合物C13的最大荧光发射波长为391 nm,C14的最大荧光发射波长为380 nm;丙醇中化合物C13的最大荧光发射波长为386 nm,C14的最大荧光发射波长为378 nm;丁醇中化合物C13的最大荧光发射波长为385 nm,C14的最大荧光发射波长为377 nm。可以看到目标化合物在所有质子性溶剂中的荧光发射峰较参比化合物均发生一定程度的红移。这是由于在质子性溶剂中存在目标化合物分子间氢键作用导致的。
另外还看到,在甲醇溶剂中,所有目标化合物与参比化合物均展现出双荧光发射带。这和单取代苯基乙烯基亚氨基片段的化合物一样,同样的,这是由于甲醇分子的强极性造成的溶剂中醇羟基活泼型增大,从而与化合物亚胺基团相互作用所致[269]。同样的,由于质子性溶剂中活泼氢较多,不利于目标化合物自身分子间氢键的形成,因此,随着在极性较大的质子性溶剂中,目标化合物C13等也没能发生明显的ESPT反应。但可以看到其在520 nm左右处有可能发生ESPT反应,只是没有明显的发射峰出现。
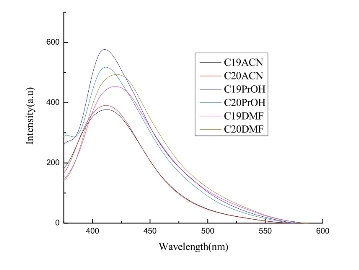
图2.25 化合物C19和C20在不同溶剂中的荧光光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为10/10 nm)
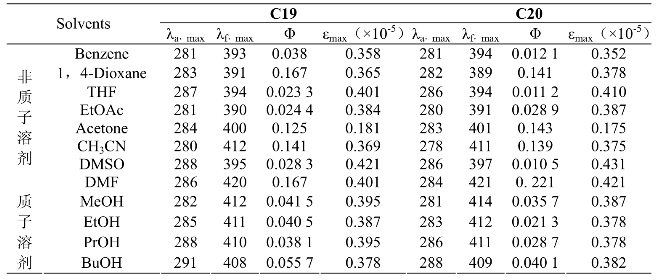
另外,本节还对参比化合物C19—C20进行了荧光光谱分析(如图2.25)。已经知道参比化合物的结构上只有一个-C=N生色团的存在,所以其分子荧光光谱也比较简单,仅表现出分子内电荷转移引起的正常荧光发射峰。可以看到,在不同溶剂中均没有,也不可能像同类目标化合物那样展现出质子转移峰。由于受到非共轭碳链长短的影响,分子表现出随着碳链增长荧光发射波长红移的现象,由于分子整体结构对称性良好而又没有其他吸供电子基团的影响,所以其红移范围也较小,为1~2 nm。(https://www.xing528.com)

图2.26 化合物C17在DMF溶液中不同浓度的荧光光谱(320 nm波长激发,狭缝宽度为10/10 nm)
为了更好地验证目标化合物存在分子间氢键作用,专门测试了目标化合物在不同浓度下的荧光发射光谱图,以化合物C17为例(如图2.26)。可以看到随着浓度的增大,IE*/IN* 值分别为0.000、0.1469、0.1662、0.3173、0.3213、0.4016、0.4141,呈现出逐渐增大的趋势,可见浓度增大,压缩了分子间距,从而有利于分子间氢键的结合,即有利于ESPT的发生。另外,必须指出的是由于浓度的增大,分子的荧光强度也发生了衰减现象,这是由于分子自吸收引起的荧光淬灭现象。
可以确定此类含非共轭双苯基乙烯基亚氨基片段目标化合物在极性较大的溶剂中,如DMF、DMSO可以发生ESPT反应。在自然状态下,目标化合物在固态下同样可以发生ESPT反应,以化合物C11/C12为例,对目标染料的固态荧光进行测试(如图2.27)。对比目标化合物的溶剂中的荧光发射光谱图可以看到,固态荧光下目标化合物在520 nm处也同样展现出一个新峰,即ESPT峰,而且可以看到这个峰比在溶剂中表现得更加明显且有一定程度的红移。这可能是在固态下分子间氢键作用的链接更加紧密、作用更加强烈导致的。
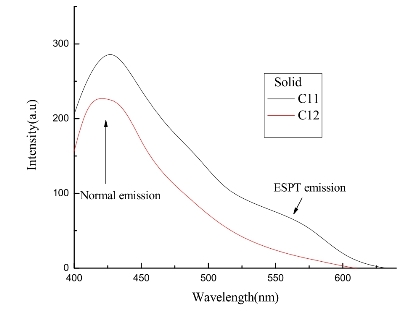
图2.27 化合物C11和C12固态的荧光光谱(320 nm波长激发,狭缝宽度为5/5 nm)
表2.7 化合物C11和C12在不同溶剂中的光谱数据(λ/nm,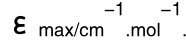 L)
L)
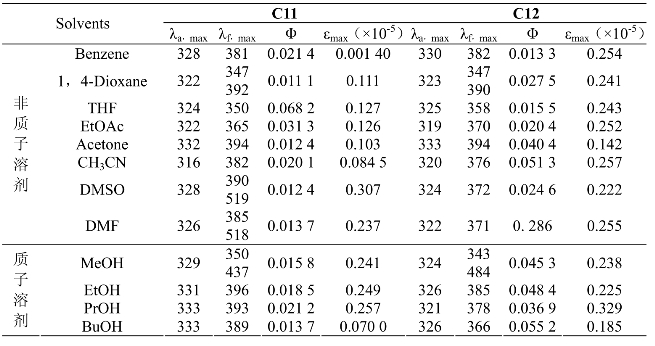
表2.8 化合物C13和C14在不同溶剂中的光谱数据(λ/nm,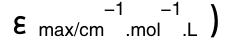
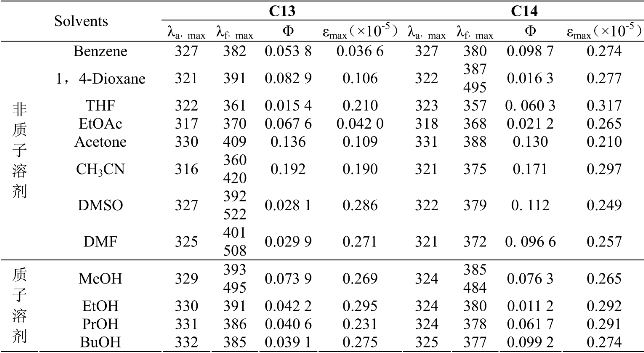
表2.9 化合物C15和C16在不同溶剂中的光谱数据(λ/nm,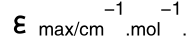 L)
L)
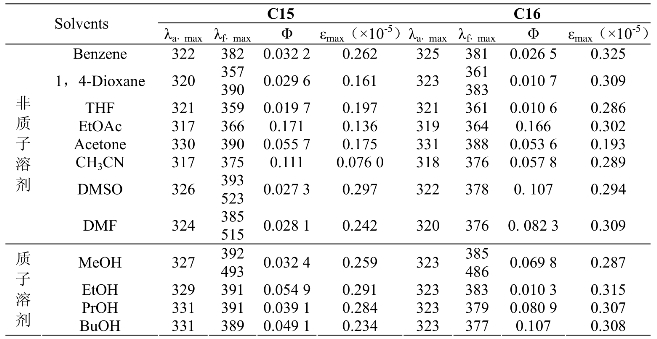
表2.10 化合物C17和C18在不同溶剂中的光谱数据(λ/nm,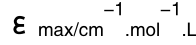 )
)
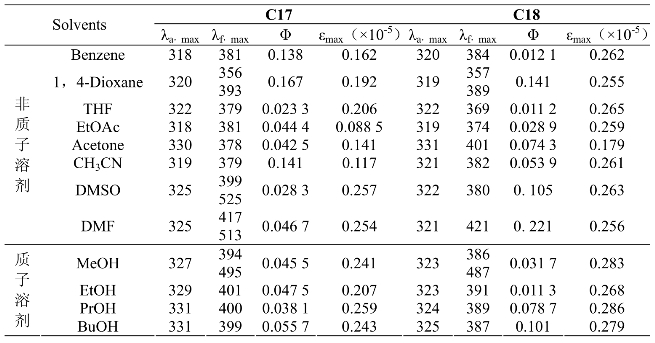
表2.11 化合物C19和C20在不同溶剂中的光谱数据(λ/nm,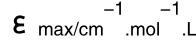 )
)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




