基于对目标化合物C1—C10紫外吸收光谱的研究,为了排除π-π*跃迁对荧光光谱的影响,选择了320 nm作为激发波长,研究化合物在不同非质子性溶剂与质子性溶剂中的单光子荧光发射光谱。研究发现,化合物的荧光发射光谱与紫外吸收光谱有较好的对应关系,但存在较大的Stocks位移。这是由于处于激发态的电子,通常以辐射跃迁方式或无辐射跃迁方式再回到基态。辐射跃迁主要涉及荧光、延迟荧光或磷光的发射等;无辐射跃迁则是指以热的形式辐射其多余的能量,包括振动弛豫(VR)、内部转移(IR)、系间窜越(IX)及外部转移(EC)等,在这一个过程能量的损失会造成HOMO、LUMO轨道能级差的减小,所以会发生一定程度的红移现象,各种能量损失发生的可能性及程度,与化合物本身的结构及激发时的物理和化学环境等因素有关。

图2.10 化合物C1和C2在多种非质子性溶剂中的荧光发射光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为5/10 nm)
以目标化合物C1/C2为例,研究其在极性相对较低的不同非质子性溶剂中的单光子荧光发射光谱(如图2.10)。可以看到其在不同溶剂中在325~425 nm范围内均展现出一个正常的荧光发射带,这是由于分子的CT*→CT的辐射衰变引起的[266-268]。对比化合物C1和C2在非质子性溶剂中的荧光发射光谱,可以看出其受溶剂极性的影响而表现出一般溶剂化效应。主要表现在由于溶剂极性的增大,分子内电荷转移能力增强,荧光峰会相应出现一定程度的红移。在非质子性溶剂中,目标化合物C1的荧光强度明显强于参比化合物C2,这是因为目标化合物可能存在激发态分子间氢键作用造成的。
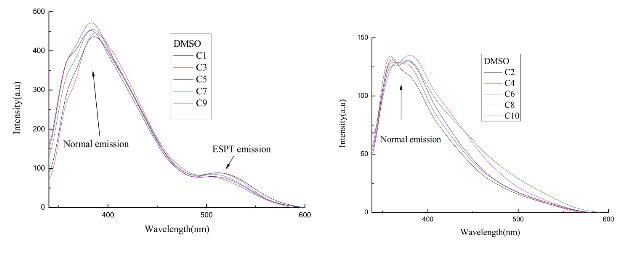
图2.11 化合物C1—C10在DMSO中的荧光光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为5/10 nm)
在极性较大的非质子性溶剂中,以DMSO溶剂为例研究其在同等条件下不同化合物的荧光发射光谱(如图2.11,表2.2—2.6)。可以发现化合物C1、C3、C5、C7、C9均展现出独特的双荧光发射带,其一是由电荷转移(ICT)引起的荧光发射带在400 nm处,另一个荧光发射带较之第一个荧光发射带有100 nm左右的红移,这是激发态分子间质子转移过程中K*→K的非正常发射带。而参比化合物C2、C4、C6、C8、C10,均只表现出由电荷转移引起的单一的荧光发射带。
另外,看到化合物C1的最大荧光发射波长分别为387/515 nm,IE*/IN* 值(ESPT峰荧光强度与正常荧光发射峰强度比值)为0.195,C2分子的最大荧光发射波长为378 nm,C3分子的最大荧光发射波长为383/515 nm,IE*/IN* 值为0.170,C4分子最大荧光发射波长为378 nm,C5分子的最大荧光发射波长为384/510 nm,IE*/IN* 值为0.176,C6分子的最大荧光发射波长为378 nm,C7分子的最大荧光发射波长为385/509 nm,IE*/IN* 值为0.175,C8分子的最大荧光发射波长为379 nm,C9分子的最大荧光发射波长为388/516 nm,IE*/IN* 值为0.193,C10分子的最大荧光发射波长为380 nm。
由于化合物C1—C8结构基本相似,其荧光发射带均没有太大的变化。而化合物C9和C10则由于连接的是苯丙亚胺基,其电子转移能力较烷基脂肪链分子稍强,故其荧光发射带相比有3 nm左右的红移。另外,对比目标化合物C1、C3、C5、C7的IE*/IN* 值,也可以看出增加碳链长度并没有改变其ESPT发生的能力。相反,在只有两个碳的时候其分子整体的共轭性更好,空间位阻较小,表现出ESPT能力更强一些。
通过对比化合物C1和C9的荧光数据,还可以看到化合物C1的ESPT能力比C9稍强一点。通过化合物C1与C9的单晶结构也可以看到化合物C1的乙基亚胺链比化合物C9的苯丙亚胺链的位阻稍小些,扭转能力稍强,更有利于分子间氢键的形成。另外,还看到参比化合物展现的单一的正常荧光发射峰的位置在378~380 nm,几乎没有发生Stocks位移。除此之外,还应该看到的是同一对化合物相比较,目标化合物由于分子间氢键的存在,其荧光强度明显大于相应的参比化合物。
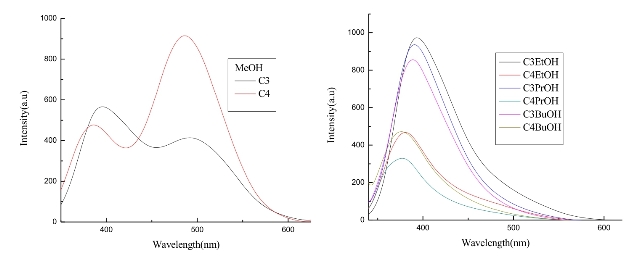
图2.12 化合物C3和C4在质子性溶剂中的荧光光谱(C=1×10-5mol·L-1,320 nm波长激发,狭缝宽度为5/5 nm)
研究目标化合物在不同质子性溶剂中的荧光发射光谱,仍以目标化合物C3和C4为例进行分析(如图2.12)。可以看到化合物C3在甲醇中分子的最大荧光发射波长为394/494 nm,C4的最大荧光发射波长为384/486 nm;乙醇中C3分子的最大荧光发射波长为393 nm,C4的最大荧光发射波长为380 nm;丙醇中分子的最大荧光发射波长为391 nm,C4的最大荧光发射波长为378 nm;丁醇中分子的最大荧光发射波长为389 nm,C4的最大荧光发射波长为376 nm。可以看到目标化合物在所有溶剂中的荧光发射峰较参比化合物均发生了一定程度的红移,这是由于目标化合物分子间氢键作用导致的。
随着不同质子性溶剂质子化程度的减小,化合物C3分子间氢键作用能力减弱,导致其荧光发射峰也出现了一定程度的蓝移。另外,目标化合物C3的荧光强度随着溶剂极性的增大依次增强,这是由溶剂诱导效应引起的。尽管溶剂极性的增大有利于目标化合物ESPT反应的发生,但是由于质子性溶剂中活泼氢较多,不利于目标化合物自身分子间氢键的形成,因此,随着在极性较大的质子性溶剂中,目标化合物C3等并没有表现出ESPT发射峰。
值得注意的是在甲醇中,无论是目标化合物与参比化合物,除光源峰外均展现出双荧光发射带。这是由于甲醇溶剂的强极性导致醇羟基的活泼型最大,从而与化合物分子之间形成特殊相互作用所致,而这主要是和化合物分子结构中的-C=N键间相互作用 [269]。
 (https://www.xing528.com)
(https://www.xing528.com)
图2.13 化合物C1在DMF溶液中不同浓度的荧光光谱(320 nm波长激发,狭缝宽度为10/10 nm)
单独测试了目标化合物在不同浓度下的荧光发射光谱(如图2.13)。以化合物C1为例,可以看到随着浓度的增大,IE*/IN* 值分别为0.1062、0.1371、0.1646、0.2085、0.2430、0.2500、0.3163,呈现出逐渐增大的趋势。也就是说,浓度增大有利于非正常辐射的发生,即有利于ESPT的发生。这一现象更有力地证明了目标化合物是存在分子间质子转移现象的,同时增大浓度有利于分子的聚集,从而有利于二聚体的生成,可见目标化合物是分子间的相互作用;另外,还看到由于浓度的增大,分子的荧光强度也发生了衰减现象,这是由于分子自吸收引起的荧光淬灭现象。
目标化和物C1不仅在DMF等强极性溶剂中展现了ESPT反应能力,在固态下同样可以发生ESPT反应(如图2.14)。在自然状态下的固态荧光情况,实验结果表明,目标化合物C1在无外界影响下,可以发生激发态分子间质子转移,而且比在溶液中表现更加明显。同样地,非共轭单取代的含邻羟基苯基乙烯基亚氨基有机染料固态时均可以发生ESPT反应,而相应的参比化合物由于不具备分子间氢键的形成条件,所以不能发生ESPT反应。

图2.14 化合物C1/C2固态的荧光光谱(320 nm波长激发,狭缝宽度为3/3 nm)
表2.2 化合物C1和C2在不同溶剂中的光谱数据(λ/nm, )
)

表2.3 化合物C3和C4在不同溶剂中的光谱数据(λ/nm, )
)

表2.4 化合物C5和C6在不同溶剂中的光谱数据(λ/nm, )
)

表2.5 化合物C7和C8在不同溶剂中的光谱数据(λ/nm, )
)

表2.6 化合物C9和C10在不同溶剂中的光谱数据(λ/nm, )
)

免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




