钠硫电池是以Na—beta—氧化铝(Al2O3)为电解质和隔膜,并分别以金属钠和多硫化钠为负极和正极的二次电池。钠硫电池通常是由正极、负极、电解质、隔膜和外壳等几部分组成。一般常规二次电池如铅酸电池、镉镍电池等都是由固体电极和液体电解质构成,而钠硫电池则与之相反,它是由熔融液态电极和固体电解质组成的,构成其负极的活性物质是熔融金属钠,正极的活性物质是硫和多硫化钠熔盐。由于硫是绝缘体,所以硫一般是填充在导电的多孔的炭或石墨毡里,固体电解质兼隔膜的是一种专门传导钠离子被称为Al2O3的陶瓷材料,外壳则一般用不锈钢等金属材料。其基本结构图如图3-11所示,其充放电原理图如图3-12所示。
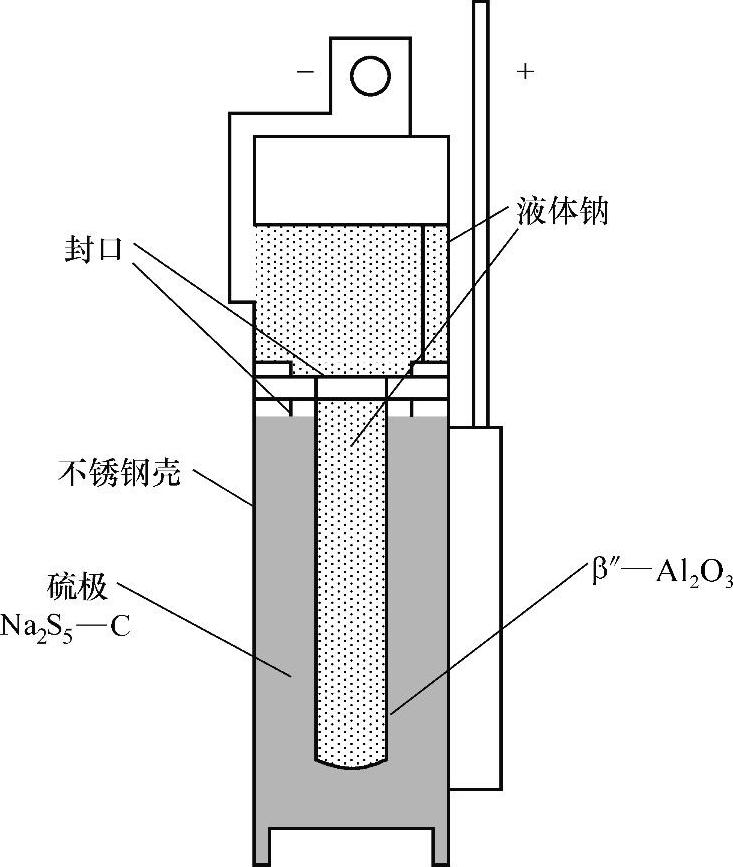
图3-11 钠硫电池结构图
含熔融钠的阳极腔用β—氧化铝或β″—氧化铝电解质管将含熔融硫的阴极隔开。电解质管能传导钠离子,同时又是电子绝缘体。阳极与阴极之间用α—Al2O3电绝缘体密封。电池的外壳用不锈钢制造。阴极的集流器由纤维石墨垫和阴极浸透的炭组成,而阴极腔内部则用电镀铬等耐腐蚀材料保护。电池中有插入电解质管中的保护管,用不锈钢支撑,从钠的贮存槽延伸到电解质管的底部,它与钠计量装置结合,在电解质管万一破裂时,以控制钠硫之间的放热反应速度,在失效时限制温度偏移,限制值为高出额定工作温度100℃左右。在高温下,硫的蒸气压很高,因此钠硫电池必须是密封结构。
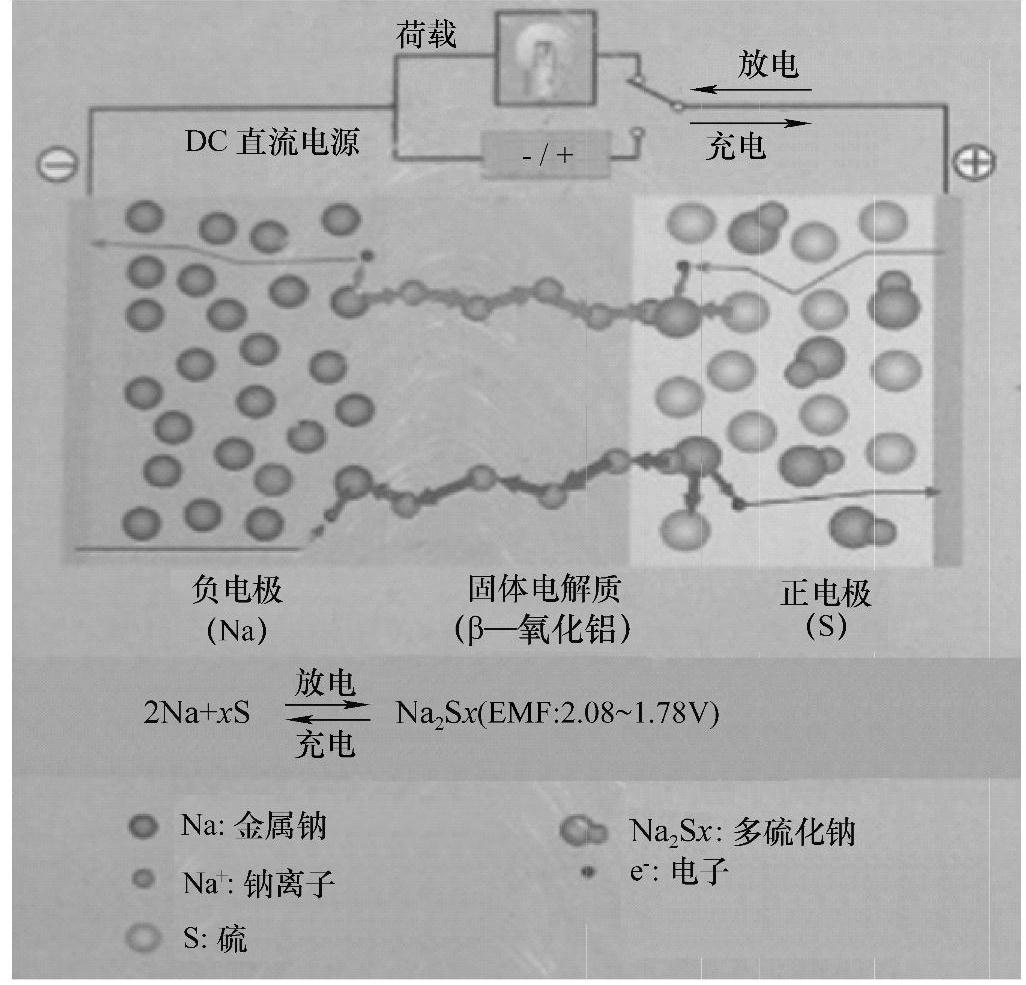
图3-12 钠硫电池充放电原理
工作中,放电时负极中的钠失去了电子成为Na+离子,由于含钠的β″—Al2O3陶瓷是钠离子导体,因而钠离子就能通过陶瓷管扩散到正极与硫反应。这时,接上负载就会有电流产生。
钠硫电池中两极的液相变化及化学反应如下:
放电初期,正极活性物质处在两液相区(金属钠和多硫化钠都处在液态),此时发生下述反应:
负极:2Na→2Na++2e-
正极:2Na++5S+2e-→Na2S5(L)
电池反应:2Na+5S=Na2S5(L)
电动势为: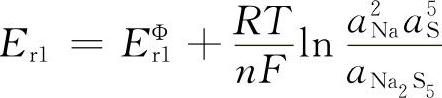
此时,一个液相为含少量硫的Na2S5,另一相为含少量Na2S5的S,这样aNa、aS、aNa2S5均看成1,则Er=EΦr=2.08V,几乎恒定不变。(https://www.xing528.com)
在放电中期,多硫化钠中的硫耗尽后,其电极反应为
负极:2Na→2Na++2e-
正极:2Na++4Na2S5+2e-→5Na2S4(L)
电池反应:2Na+4Na2S5=5Na2S4(L)
电动势为: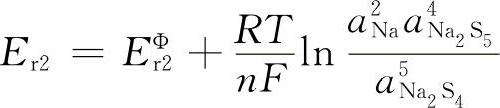
由于Na2S5和Na2S4都在熔液L中,它们的浓度是变化的,因而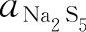 和
和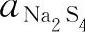 也是变化的。
也是变化的。
在放电后期,多硫化钠熔液中Na2S5耗尽后,其电极反应是
负极:2Na→2Na++2e-
正极:2Na++Na2S4+2e-→2Na2S2(L)
电池反应:2Na+Na2S4=2Na2S2(L)
电动势为: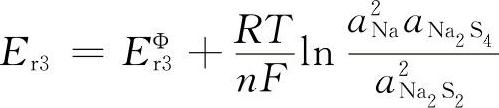
同样Na2S2和Na2S4都在熔液L中,Na2S4逐渐减小而Na2S2逐渐增多,其电动势呈下降趋势。
可以看出,放电时负极的钠逐渐消耗,正极形成多硫化物,体积和质量均增加。当放电超过一个点,进入两相平衡区,生成固态Na2S2,则会堵塞隔膜(β″—Al2O3),此时放电即终止。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




