本课题组张英豪博士和姚谦硕士合成并放大了4,5-二四唑基-1,2,3-三唑(BTTZ),同时研究了其在气体发生剂领域的应用。BTTZ与不同氧化剂的配方方案如表2-15所示。
表2-15 BTTZ与不同氧化剂的配方方案 单位:%(质量分数)
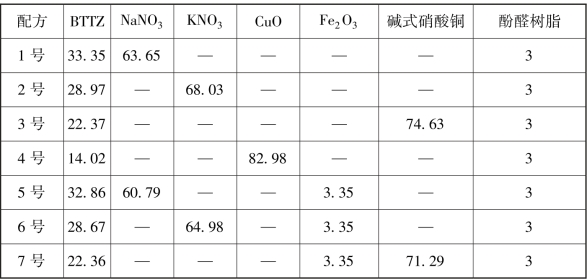
对于表2-15设计的7种气体发生剂配方,结合上面的生成焓用Real程序计算它们燃烧时的热力学参数和反应平衡组成,具体结果见表2-16。
表2-16 Real程序计算结果
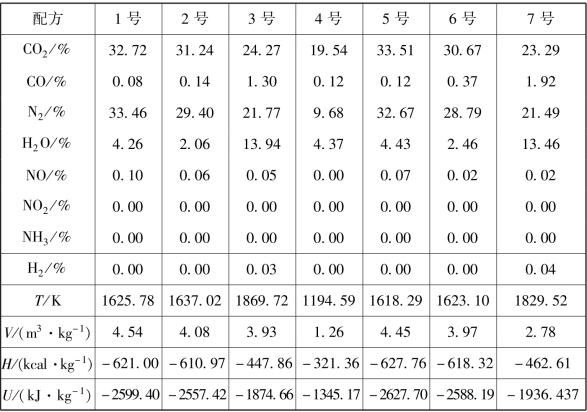
注:以上百分比均为质量分数且是占所有产物的分数(包含固体残渣)。
气体发生剂的比容是衡量气体发生剂性能的重要指标。所有配方均属于零氧平衡,主要区别为氧化剂的不同,对比前三个配方(1~3号)和后三个配方(4~6号),可以发现加入Fe2 O3之后气体的比容(产气量)均下降,那是由于虽然Fe2 O3也可以起到一定的氧化作用,但是其供氧能力不及其他常见氧化剂。对比1号和2号配方、5号和6号配方可以发现,使用硝酸钠的产气量都较使用硝酸钾的高,这是由于硝酸钠的相对分子质量小,单位质量的供氧能力强,反映到配方中就是氧化剂所占的质量分数小,从而可燃剂(产气剂)所占的比例就较大导致的。4号配方使用氧化铜的产气量最小。
燃烧温度也是很重要的参数,通过对比可以发现使用氧化铜的4号配方温度最低,同时燃烧放出热量也最少。使用碱铜的配方温度都较高,其次是硝酸钾和硝酸钠,可以看出温度高的放热反而少。
气体发生剂燃烧产物的组成是比较关注的问题。Real程序所计算的结果为质量分数,并且其中包含了固体残渣,不能很好地反映气体最终的成分比例。从最终冲气囊角度考虑更希望得到体积分数,通过换算可以对比两种计量方法,见表2-17。
表2-17 配方生成气体的质量分数和体积分数
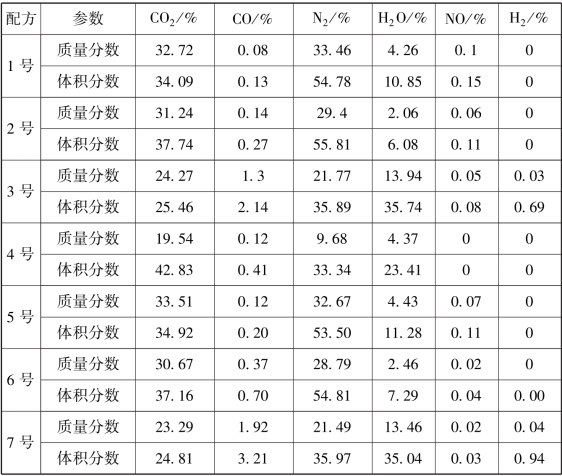
注:氨气、氮气和氢气均为零,不再进行罗列。
气体产物中N2含量最高的是使用KNO3的2号配方,使用CuO的4号配方CO2含量最高。使用了碱式CuNO3的配方含水量普遍较高,那是由于碱式硝酸铜本身含有三个羟基导致的,即使如此也比胍类30%~60%的含水率低很多。其他几个没有使用碱式CuNO3的配方含水量最小为6.08%,对应质量分数为2.06%,而唑类和偶氮四唑类最低为10.12%和10.65%,完全达到了低水蒸气的目标。将N2和CO2看作理想产物,理想产物含量最高的是2号配方,理想产物比例为93.55%。
关于有毒有害气体,所有配方均不含有NO2和NH3,使用碱式CuNO3和CuO配方中NO含量均很低,4号配方甚至不含有NO。(https://www.xing528.com)
燃烧温度的测试于第3章有详细阐述。在BTTZ配方中,燃烧温度的次序为:5号>3号>2号>1号>4号>6号>7号。
通过将药品放入密闭爆发器点燃的方式可以得到压力—时间曲线。该曲线可以间接评价气体发生剂的产气性能。实验所使用密闭爆发器为200 mL,点燃方式为电点火头点燃,数据记录使用示波器。测试样品选取具有代表性和1、3、4和7号配方进行测试,如图2-14~图2-17所示。
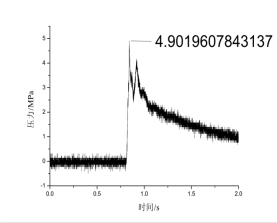
图2-14 1号配方5g药的压力—时间曲线
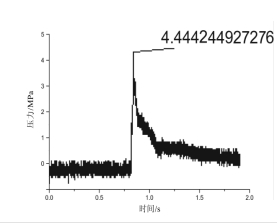
图2-15 1号配方3 g药的压力—时间曲线
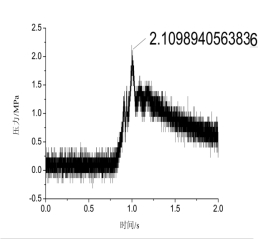
图2-16 3号配方3 g药的压力—时间曲线
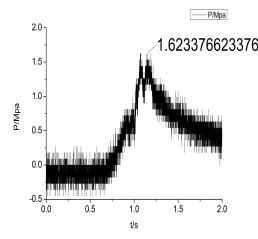
图2-17 7号配方3 g药的压力—时间曲线
从图可以看出,1号配方的压力值最大而且产气速度很快出现很陡峭的上升段,但是观察密闭爆发器中残渣,5g里面有很多白色没有燃烧的原料,又做了3g药量的,结果残渣明显减少,同时3g和5g药的压力值差距并不大。这是由于瞬间的产气量较大,将周围还未反应的物料直接喷溅到了容器壁,迅速冷却没有反应完全。
对比3号和1号配方可以看到压力值明显较少,结合Real计算,3号配方产气量较少;但同时观察曲线的坡度可以看到,3号配方的明显要缓很多。主要是由于碱式CuNO3配方的燃烧速度较慢,同时压力传感器检测较小的压差比较迟钝。
3号和7号配方相比坡度更缓,压力更小。主要是由于加入Fe2 O3之后,燃速变慢,产气量也相应较少导致的。
结合4号配方的压力—时间曲线,由于该配方燃烧速度很慢,没有陡然的产气过程,在示波器检测的2s内产气量并不大,最后残渣仍保持团状。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




