
图11-13 喷射氧化再生槽
1—槽体;2—分布板;3—喷射器(8支);4—环形溶液总管;5—液位调节器;6—排气孔;7—防虹吸管
由各种原料制取的原料气均含有大量的CO,且CO不是生产合成氨的原料,还对氨合成催化剂有毒,故在原料气送入氨合成塔之前必须彻底清除掉。生产中一般分两步清除CO:第一步是CO与H2O(g)作用生成CO2和H2的反应(即CO的变换反应),清除大部分的CO;第二步是采用铜洗、甲烷化、甲醇化等方法清除变换气中少量的CO(即原料气的精制)。
1.CO变换原理
CO变换反应方程式如下:
![]()
该反应的特点是放热、等体积的可逆反应,无催化剂时反应很慢,必须在催化剂的作用下反应速率才能加快。
从变换反应式可知:在反应过程中消耗的只是水蒸气,得到的是H2。因此,CO变换既是原料气的净化过程,又是原料气制备的继续。残余的少量的CO再通过其他净化方法加以脱除。
在实际生产中CO变换反应均在催化剂的作用下进行,式9.25在不同温度下分两步进行,第一步使用以Fe2O3为主体的变换催化剂,在操作温度为350~550℃范围内,使大部分CO转化为CO2和H2,使CO含量降至3%~4%(此过程亦称高温变换);第二步以CuO为主体的变换催化剂,在操作温度为180~260℃范围内,使CO含量降至0.3%~0.4%(此过程亦称低温变换)。
(1)变换反应的热效应。CO变换反应热效应如表11-8所示。由表11-8数据可知:变换反应为放热量不大的反应,低温有利于平衡向生成CO2和H2的方向移动。
表11-8 变换反应的热效应

(2)变换反应的化学平衡。
由式(11-25)可知,CO变换反应的平衡常数可表示为

式中 pCO、pCO2、pH2、pH2O——分别是CO、CO2、H2、H2O的分压;
yCO、yCO2、yH2、yH2O——分别是CO、CO2、H2、H2O的摩尔分数。
由计算表明:压力低于5MPa时,可不考虑压力对平衡常数Kp的影响,温度200~550℃变换反应的平衡常数如表11-9所示。
表11-9 CO变换反应平衡常数

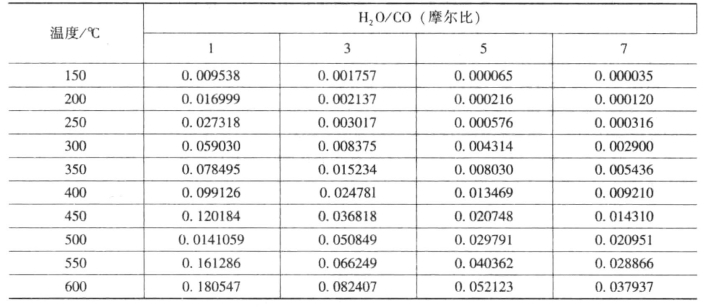
表11-10不同温度和水蒸气比例下,干变换气中CO的平衡含量(摩尔分数)。
表11-10 不同温度和水蒸气比例
从表11-9变换反应的平衡常数及表11-10变换反应的热效应分析,可得出结论:在压力一定时,平衡常数Kp随反应温度的升高,其Kp逐渐减小;而放热量也减少。故从热力学分析,温度较低有利于CO的变换反应。
从CO变换反应可知,H2O(g)是反应物,提高其用量可使CO平衡转化率提高,表11-10是压力一定、不同温度下随H2O/CO(摩尔比)增加,其干变换气中CO平衡含量的变化情况。
从表11-10不同温度及水蒸气比例下,干变换气中CO的平衡含量分析,可得出结论:
①同一H2O/CO比下,随温度的降低,其CO平衡含量也降低。
②同一温度下,增大H2O/CO比,其CO平衡含量降低。故低温,高H2O/CO比,可降低CO残余含量,但水蒸气属于物料消耗,须考虑经济因素。
(3)CO变换反应动力学。
①动力学方程。变换反应的动力学方程,因催化剂性能的差异及各研究者采用的实验条件的不同,其中温变换动力学方程有很多,在工艺计算中,较常用的有如下两种类型。
![]()
式中 rCO——反应速率,(Nm3CO/m3催化剂·h);
ya、 ——分别为CO的瞬时含量及平衡含量,摩尔分数;
——分别为CO的瞬时含量及平衡含量,摩尔分数;
kO——反应速率常数,h-1。
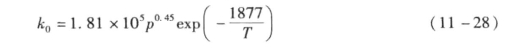
式中 p——压力,MPa;
T——温度,K。
式(11-28)是以CuO-gnO系低变催化剂在温度180~270℃、压力0.1~1.2MPa下做出的整理,如以此方程式计算催化剂用量则需乘以一个安全系数。

式中 k——反应速率常数,h-1;
ya、yb、yc、yd——分别为CO、H2O、CO2、H2的瞬时含量,摩尔分数。
②扩散过程的影响。
CO变换反应受内扩散影响较为显著,有时表现为强内扩散控制。催化剂的内表面利用率与反应温度、压力和组成以及催化剂的规格、结构、反应活性有关。图11-14表示中变催化剂内表面利用率与其影响因素的关系。
由图11-14分析可知:对同一规格的催化剂,同一压力下,随温度升高,CO的扩散速度有所增加,而催化剂表面反应的速度常数增加更迅速,总的表现出内表面利用率降低;在相同温度和压力下,小颗粒的催化剂内表面利用率较高。这是由于外表面大,内表面扩散易于进行,但其阻力相应增大,对同一规格的中变催化剂,在相同温度下,随着压力的提高,反应速度增大,而CO的有效扩散系数显著变小,因此内表面利用率迅速减小。故为了提高催化剂内表面的利用率,采用小颗粒的催化剂、较高的反应温度和较低的操作压力。(https://www.xing528.com)

图11-14 中(高)变催化剂在不同温度及压力下的内表面利用率
2.变换的催化剂
CO变换反应采用何种催化剂,要根据生产工艺要求和具体情况而定。变换催化剂依据变换温度可分中温变换和低温变换催化剂。
(1)中温变换催化剂
按组成可分为铁铬系和钴钼系两大类。前者活性高、机械强度高、耐热性能好、能耐少量硫化物、使用寿命长、成本低,在工业生产中得到广泛应用;后者突出的优点是具有良好的抗硫性能,适应于含硫化物较高的原料气,但价格较高。
①铁铬系催化剂。以Fe2O3、Cr2O3为主,同时还含有少量MgO、K2O、CaO等,其操作温度为315~485℃。其Cr2O3的加入对变换催化剂起一个结构稳定剂的作用,加入Cr2O3后,与Fe3O4形成固溶体,可有效防止或延缓高温烧结而使晶粒再结晶长大和表面积减小,提高催化剂的耐热能力和机械强度,延长催化剂的使用寿命;K2O和CaO能提高该催化剂的活性和热稳定性作用,是良好的助催化剂;MgO能增强催化剂的耐热和抗硫性能,使用时必须将Fe2O3还原成Fe3O4才具有活性。国产中温变换催化剂如表11-11所示。
表11-11 中温变换催化剂的主要特性和操作条件

②钴钼系催化剂(耐硫催化剂)。
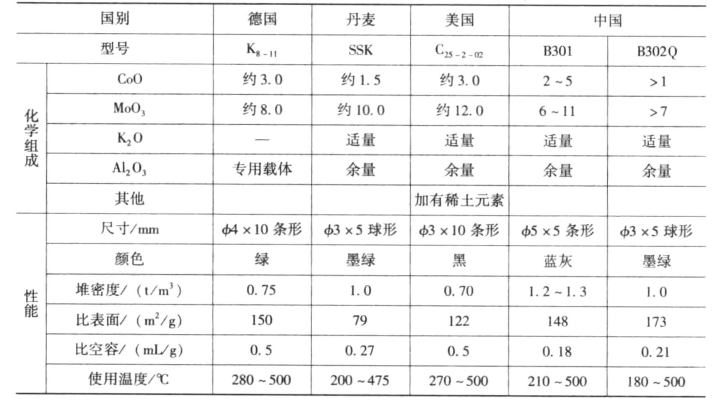
钴钼系催化剂是基于铁铬系催化剂耐硫性能差、活性温度范围窄的缺点而研发成功的。其主要成分为CoO、MoO、K2O和Al2O3,且以球形Al2O3为载体,采用浸渍法工艺制备而成。国内外耐硫变换催化剂的化学组成及性能如表11-12所示。耐硫催化剂的优点是:有很好的低温活性,一般为180~500℃;有突出的耐硫和抗毒性能;强度高,使用寿命可达5~10年;可再硫化。该催化剂的CoO、MoO3必须经硫化为CoS、MoS2才具有活性。
表11-12 国内外耐硫变换催化剂的化学组成及性能
(2)低温变换催化剂
目前工业上采用的低温变换催化剂均以CuO为主体的催化剂,经还原后具有活性组分的细小的铜结晶。CuO催化剂耐热性能差、易烧结、寿命短。加入ZnO、Cr2O3、Al2O3,将铜微晶有效地分隔开来,防止铜微晶长大,提高了催化剂的活性和热稳定性。按组成不同,低变催化剂分为铜锌系、铜锌铝系和铜锌铬系。国产低变催化剂的性能如表11-13所示。
表11-13 国产低变催化剂的性能

3.CO变换工艺条件的确定
依据变换反应的热力学、动力学及催化剂的分析,变换过程的条件主要有:温度、压力、H2O(g)/CO(汽/气比)。在分析确定工艺生产条件时,还应考虑安全生产,科学合理、经济,可操作性强。
(1)压力。从变换反应原理可知,压力对变换反应的平衡没有影响,而反应速率与总压约成0.45次方呈正比关系,故变换过程的空速随总压的提高而增大;另加压操作有利于降低能耗(因干原料气的体积小于干变换气的体积,故加压原料气变换比加压变换气时能量消耗要低);同时加压变换也提高了过量蒸汽的回收价值,但加压变换需要较高的蒸汽,对设备材质的要求相对较高。变换压力的大小具体地由压缩机各段压力分配来确定。
(2)温度。从动力学分析知:温度升高,反应速率常数增大;而变换反应是放热反应,其平衡常数随温度升高而减小。所以温度升高对反应速率有利,但对化学平衡的影响是不利的。对一定的催化剂和气相组成及对应每一个转化率时,必定对应有一个最大的反应速度,此最大反应速率对应的温度即为最适宜温度,用Tm表示。

式中 Tm、Te——分别为最佳温度及平衡温度,K;
R——气体常数,kJ/(kmol·K);
E1、E2——分别为正、逆反应活化能,kJ/(kmol·K)。
由于平衡温度随系统组成而改变,不同催化剂活化能也不相同,图11-15表明了对一定初始组成的反应系统,随着CO的变换率x的增加,平衡温度Te,及最佳温度Tm均降低;对同一变换率,最佳温度一般比相应的平衡温度低几十度。若工业反应器中按最佳温度进行反应,则反应速率最大,即在相同生产能力下所需催化剂用量最少。
但是在实际生产过程中完全按最佳温度线操作几乎不可能。在反应初期,因据平衡很远,即使离开最佳温度,仍有较高的反应速率。如反应开始(x=0%)、Tm很高,一般都超过了中(高)变催化剂允许使用的温度范围,而且随着反应的进行,温度应逐渐降低,所以需要不断从反应床层移出反应热,故变换过程的温度是综合各方面因素而确定的。随着CO变换过程的进行,最佳温度不断降低,这和绝热催化反应的温度升高互为矛盾。为解决这一矛盾,使变换反应尽可能控制在Tm附近进行,工业上对中(高)温变换,通常采用多段变换的方法,即是多段反应、多段冷却的方法进行变换反应。多段冷却的方式可分为:中间换热式、喷水冷激式、蒸汽过热式三种。
变换过程的温度应在催化剂活性温度范围内进行操作。反应开始温度一般应高于催化剂起活温度约20℃,对中变催化剂,反应开始温度一般为320~380℃,热点温度在450~550℃范围。低变操作温度下限应高于该条件下气体露点温度20~30℃,防止出现液滴。
(3)汽/气比(H2O/CO摩尔比)。改变蒸汽比例是工业变换反应中最重要的调节手段。由表11-10可知,增加蒸汽用量,可提高CO的平衡转化率,从而有利于降低CO残余含量,加速变换反应的进行。因过量蒸汽的存在,还保证了催化剂活性组分Fe3O4的稳定而不被还原。另外,过量的蒸汽也起到了热载体的作用,提高蒸汽比例,含湿原料气中CO含量降低,催化剂床层温升减少,如图11-15所示CD线比AB线斜率大,故改变蒸汽用量对调节催化剂床层温度非常有利。
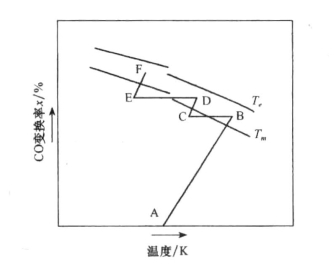
图11-15 CO变换过程的T-x图
反应初期远离平衡,正反应速率起主导作用,增加蒸汽起到了稀释CO的作用,故反应速率随蒸汽比例增大而减小;反应后期接近平衡时,提高蒸汽比例可使平衡反应向正反应方向移动,有利于提高最终转化率。
但是因水蒸气用量是变换过程中的重要消耗指标,工业上应在满足生产要求的前提下尽可能降低蒸汽比例,以降低蒸汽的消耗。因蒸汽比例过高,则催化剂床层阻力增加,CO停留时间减少,余热回收设备负荷增加。一般中(高)变操作适宜的H2O/CO=3~5,经反应后仍能满足低温变换对蒸汽的需要。
蒸汽最低用量的确定还应充分考虑CO最终变换率或残余CO含量(一般中变气含CO为3%~4%,低变气含CO为0.3%~0.4%)、余热回收、原料气中氧含量。
4.变换的工艺流程
CO变换流程的设置一般要考虑三方面的问题。一是原料气中CO含量,CO含量高,则应考虑采用中(高)温变换,因中(高)温变换催化剂操作温度范围较宽,且价廉易得,寿命长,大多数合成氨原料气中CO含量均高于10%,故都选用中(高)温变换以除去大部分的CO。依据系统反应温升,为使催化剂在允许活性温度范围内操作,对CO含量高于15%的一般应考虑将反应器分段;二是根据进入系统原料气温度、湿含量,考虑是否对气体进行几级预热和增湿,合理利用余热;三是将CO变换与脱除残余CO的方法应结合考虑。若脱除方法允许残余CO含量较高,则仅采用中(高)变即可,否则,可将中变与低变串联使用,以降低CO的含量。
图11-16为中小型合成氨厂多段变换工艺流程;图11-17为CO变换中(高)串低变流程示意图。图11-18为全低变流程,此变换工艺采用的是宽温区的钴钼系耐硫催化剂,不需要采用中(高)变催化剂,流程也就不需用中(高)变串低变。
5.变换过程的主要设备
变换过程的主要设备是饱和热水塔(即是饱和塔和热水塔的组合)、变换炉。
(1)饱和塔、热水塔。饱和塔的作用是增热、增湿;热水塔的作用是减热、减湿。两设备联合一起称饱和热水塔,该设备是为了维持系统热平衡和水平衡。饱和热水塔,饱和塔在上,热水塔在下,中间由弓形隔板分开。塔体为16mm不锈钢板制成,内装填料,填料装在工字钢和箅子板上,填料上有一圆形不锈钢喷管。为防止出饱和热水塔气体带水,在塔顶上有一层小瓷环分离段,并设有不锈钢丝网除沫器,饱和热水塔上还设置有入孔和卸料口,以便检修和装卸瓷环时使用,设置的液位计用于监视液位高度。在热水塔为防止破碎瓷环被气流带走,在气体出口管出设有不锈钢制得挡板。

图11-16 中小型合成氨厂多段变换流程
1—饱和热水塔;2—分离器;3—主热交换器;4—电加热器;5—变换炉;6—段间换热器;7—第二水加热器;8—第一水加热器;9—热水塔;10—软水加热器;11—冷凝器;12—热水器
(2)变换炉。变换炉的结构随工艺流程不同而完全不同,但均应满足如下基本要求:变换炉处理气量要尽可能大;气流阻力要小,气体在炉内分布均匀;热损失要小;结构简单,便于制造、安装和维修。图11-19为加压三段变换炉。变换炉为圆柱形,外壳由钢板制成,内砌耐热混凝土衬里或内衬石棉板,再砌一层硅藻土砖一层轻质黏土砖,在每层催化剂下面均有支架支撑,支架上铺箅子板、钢丝网和耐火球,炉壁上多处装有热电偶,炉体上还配置有入孔和装卸催化剂口。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




