(一)乙烯氧氯化反应原理及特点
乙烯氧氯化反应以乙烯、氯化氢、氧(或空气)为原料,工业上采用金属氯化物为催化剂,其中CuCl2活性最高。在催化剂作用下,生成二氯乙烷的主反应为放热反应。
![]()
乙烯氧氯化过程的主要副反应有:
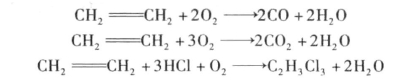
乙烯的氧氯化反应机理,国内外都做了很多研究工作,但未取得一致看法,较多地认为在氯化铜催化剂上,按氧化-还原机理进行,反应历程包括下列三步反应。
吸附的乙烯与CuCl2作用生成二氯乙烷,并使CuCl2还原为Cu2Cl2。
![]()
Cu2Cl2被氧化为两价铜,并生成包含有CuO的络合物。
![]()
络合物被HCl作用,分解为CuCl2和水。
![]()
反应的控制步骤是第一步,乙烯浓度对反应速率影响最大。从反应历程可看出,催化剂是氯化铜而不是氯化氢,催化剂中的氯消耗以后,用空气和氯化氢经过氧氯化反应连续再生。
(二)热力学和动力学分析
乙烯氧氯化反应为物质的量减少的气固相催化反应,据研究,在230℃、CuCl2/AL2O3催化剂上,反应的速率方程为
![]()
式中 γ——氧氯化反应速率;
k——反应速率常数;
[C2H4]、[HCl]——乙烯、氯化氢的浓度。
从反应速率方程可见,反应速率只与乙烯和氯化氢浓度有关,而与氧的浓度无关。工业上使用的氧氯化反应催化剂可分为单铜催化剂、二组分催化剂、多组分催化剂以及非铜催化剂等。
单铜催化剂一般含铜3%~12%,最好是2.5%~7%。载体为微球形氧化铝凝胶,含Al2O396%~97%,其余为水。该种催化剂的缺点是容易流失、磨损大(正常生产中每24h被反应气流带出的催化剂粉末不超过开始装入催化剂的0.5%)、氯化氢转化率低以及由此会引发设备腐蚀。
为了提高单铜催化剂的活性和热稳定性,采用的方法是添加碱金属或碱土金属的氯化物(如氯化钾等),从而降低熔点,增加氯的吸附能力及对二氯乙烷的选择性,抑制完全氧化反应。同时降低反应温度,也可以抑制催化剂的升华及中毒,延长其寿命。
为了寻找低温高活性的催化剂,发展趋势是采用多组分催化剂,即以氯化铜-碱金属氯化物-稀土金属氯化物组成的催化剂,其活性非常高,在反应温度下,CuCl2几乎不挥发、不腐蚀,选择性也高。
非铜催化剂可选用Pt、Mo、W催化剂以及TeO2、TeCl4、TeOCl2等,其中有的已工业化使用,有的还在试验之中。
在工业生产上,氧氯化反应较多使用的催化剂活性组分是CuCl2,载体是高纯度Al2O3,其中Cu含量(5±0.5)%,具有高选择性、多孔,不易中毒等性能。
(三)氧氯化反应的工艺条件选择
1.反应压力
作为气固相催化反应,提高压力有利于物质的量减少的氧氯化反应的平衡移动,也可以提高化学反应速率,但却使选择性下降。从图6-8压力对选择性的影响所示曲线可见,压力增加,生成1,2-二氯乙烷的选择性下降,故压力不宜过高。一般氧氯化反应常压或加压皆可,压力的高低根据反应具体情况即以能克服流体阻力而确定。当采用空气为氧化剂时,存在大量惰性气体,为了使反应气体保持相当的分压,常采用加压操作,流化床反应器正常控制压力为0.32MPa。当降低生产负荷时应相应降低反应器顶部压力,以便有效地控制旋风分离器的正常工作,保持床层的流化速度和旋风的切线速度在理想的状态下操作。
2.反应温度
乙烯氧氯化是强放热反应,因此温度控制十分重要。首先,氧氯化反应速率随温度的变化而变化,如图6-9所示。在270~280℃时有极大值,可获得最大反应速率。又如温度对二氯乙烷的选择性影响(见图6-10),也存在极大值。在230~250℃时,二氯乙烷的选择性最高,低于230℃时生成大量氯乙烷,高于250℃时,除有较多的三氯乙烷生成外,还生成二氯乙烯、氯乙烯等。此外,由图6-11温度对乙烯燃烧反应的影响可见,低于250℃时,几乎不发生乙烯燃烧反应,高于250℃以后,乙烯燃烧明显增加。
图6-9~图6-11是在Cu含量为12%(质量分数)的CuCl2/γ-Al2O3催化剂上以纯氧为氧化剂的实验结果。若以纯氧为氧源时,未反应的乙烯可循环使用,在近于230℃时二氯乙烷选择性高,乙烯的燃烧率可忽略不计。此外,温度高,催化剂活性组分CuCl2流失快,寿命缩短。所以一般在保证HCl接近全部转化的前提下,反应温度低一些为好。原料在进入反应器之前要预热到150℃以上,以免可能有HCl-水冷凝液出现而腐蚀设备。
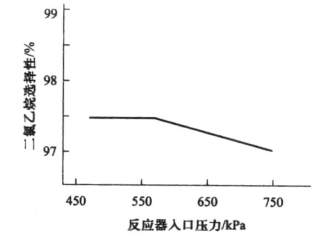
图6-8 压力对选择性的影响(氧化剂:氧)

图6-9 温度对反应速率的影响
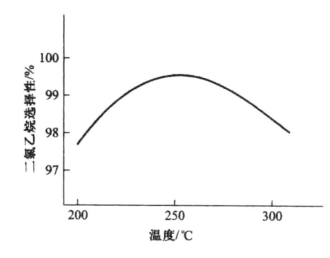
图6-10 温度对选择性的影响(以二氯乙烷计)

图6-11 温度对乙烯燃烧反应的影响
适宜的反应温度与催化剂活性有关,当采用高活性的CuCl2/γ-Al2O3催化剂时,不论是用空气还是纯氧作为氧化剂,适宜温度范围均为220~230℃。
3.原料配比
按乙烯氧氯化反应方程式的计量关系,原料摩尔配比的理论值为nC2H4∶nHCl∶nO2=1∶2∶0.5。由二氯乙烷生成的速率方程可知,氧氯化反应速率与乙烯的浓度成正比,而与HCl浓度的0.3次方成正比,所以乙烯分压大,二氯乙烷生成的速率也快。在实际生产中若乙烯对氯化氢的配比过低,会造成流化床反应不稳定,有可能造成催化剂凝结,旋风分离器大量带出催化剂等危害。其原因是HCl过量则吸附在催化剂表面,使催化剂颗粒胀大,密度减小。若采用乙烯稍微过量,能使HCl接近全部转化。但若乙烯过量太多,又会使烃类的燃烧反应增多,尾气中CO、CO2含量增加,因而选择性下降。在实际生产中,正常情况下控制乙烯略为过量,主要依据尾气中的乙烯含量在0.7%~1%为准,若操作得好,还可以进一步将尾气中的乙烯含量降到0.5%。
氧气的消耗量,其理论值是每2mol氯化氢消耗0.5mol的氧。一般情况下,氧气过量对反应的稳定性是有益的,但过量太多,会造成二氯乙烷损失过多和乙烯在反应器中的燃烧反应增加,从而乙烯消耗量增大。而氧气不足则会消耗催化剂本身的化学结合氧,导致产生贫氧催化剂的接触面,从而丧失其优良的流化特性,还会产生局部过热,HCl又反应不完全,CO2生成量减少而CO生成量增加的后果。原料气的配比必须在爆炸极限以外。
在实际生产中,当以空气为氧化剂时控制氧氯化反应器中的氧气过量30%~100%。原料摩尔配比以满足尾气中的乙烯含量为0.7%~1%,氧含量为6%~9%来调节,一般控制nC2H4∶nHC1∶nO2=(1.05~1.1)∶2∶(0.65~1)。当以纯氧为氧化剂时,原料的摩尔配比为nC2H4∶nHCl∶nO2∶惰性气体=(1.6~1.7)∶2∶(0.6~0.7)∶2。(https://www.xing528.com)
4.空间速率或接触时间
图6-12为乙烯氧氯化反应接触时间对HCl转化率的影响。由图中曲线可以看出,要使HCl接近全部转化,必须有较长的接触时间,但也不宜过长,否则HCl的转化率反而下降。此现象很可能是由于接触时间过长而发生了连串副反应,产物二氯乙烷裂解产生了HCl,故反应应该控制在最适宜的接触时间,即要有适宜的空间速率。不同的催化剂有不同的最适宜空间速率,一般活性较高的催化剂,最适宜空间速率高一些;活性低的催化剂,则最适宜空间速率较低。通常氧氯化反应是在较低的空间速率下操作,生产上常控制混合气体空间速率(标准状态下)在250~350h-1。

图6-12 接触时间对HCl转化率的影响
5.原料气纯度
烷烃、N2等惰性气体的存在对反应并无不良影响,且有利于带走热量,使温度易于控制,所以氧氯化反应可以用浓度较稀(如70%左右)的原料乙烯。但乙烯气中乙炔、C3和C4烯烃含量必须严格控制,因为这些杂质的存在不仅使氧氯化产品二氯乙烷的纯度降低,而且对二氯乙烷的裂解过程会产生不良影响。乙炔的存在会因发生乙炔氧氯化反应生成四氯乙烯、三氯乙烯等,这些杂质存在于二氯乙烷成品中,在加热汽化时易引起结焦。丙烯也会发生氧氯化反应生成1,2-二氯丙烷,它对二氯乙烷的裂解有强抑制作用。原料HCl的纯度也很重要,由二氯乙烷裂解得到的HCl,很可能含有乙炔,需经加氢精制处理,使乙炔含量低于0.002%。
想一想 在化工生产中反应器的选择主要考虑哪些因素?
(四)氧氯化反应器
乙烯气相氧氯化反应采用流化床反应器,流化床具有保持任何部位的温度都均匀的优点。由于催化剂在反应器内处于沸腾状态,床层内又有换热器,可以有效地引出反应热,因此完全消除了热点,反应温度容易控制,流化床适用于大规模生产。
流化床氧氯化反应器是不锈钢或钢制圆柱形容器,高度约为直径的10倍,其构造如图6-13所示。

图6-13 流化床乙烯氧氯化反应器的结构示意图
1—乙烯和氯化氢入口;2—空气入口;3—板式分布器;4—管式分布器;5—催化剂入口;6—反应器外壳;7—冷却管组;8—加压热水入口;9,13,14—第三、二、一级旋风分离器;10—反应气体出口;11,12—净化空气入口;5—入孔;6—高压水蒸气出口
在氧氯化反应器底部水平插入空气进料管至中心处。管上方设置一个向下弯的拱形板式分布器。此分布器上有许多个喷嘴,每个喷嘴由下伸的短管及其下端开有小孔的盖帽所组成,用以均匀分布进入的空气。在分布板上方又有乙烯和HCl混合气的进入管,此管连接一套具有同样多个喷嘴的管式分布器,其喷嘴恰好插入空气板式分布器的喷嘴内,如图6-14所示。
这样就能使两股进料气体在进入催化剂床层之前瞬间在喷嘴内部混合均匀。此反应器采取空气与乙烯-氯化氢气分别进料的方式,可防止在操作失误时有发生爆炸的危险。
在分布器上方至总高度3/5处的一段筒体内,存放CuCl2/Al2O3催化剂,在原料气流的作用下呈沸腾状,此段为流化床反应器的流化段。在流化段内设置了一定数量的直立冷却管组,管内通入加压热水,借水的汽化移出反应热,并产生相当压力的水蒸气。
在氧氯化反应器的上部空间内设置三个互相串联的内旋风分离器,用以分离回收反应气体所夹带的催化剂。自第三级分离器出来的热反应气体中已基本上不含催化剂,残留于气体中的只是少量极细小的催化剂粉末。
催化剂的磨损量每天约为0.1%,需补充的催化剂自气体分布器上方用压缩空气送入反应器内。
由于氧氯化过程有水生成,如果反应器的一些部位保温不好,温度过低,当达到露点温度时,水会凝结,将使设备遭受严重腐蚀,因此反应器各部位的温度必须保持在露点以上。
(五)工艺流程
以用空气作为氧源的古德里奇技术为例,乙烯气相氧氯化制二氯乙烷的工艺流程如图6-15所示。
从裂解得到的氯化氢加热到170℃,与氢气一起送入脱炔反应器1,将氯化氢中所含的乙炔选择加氢生成乙烯。原料乙烯经预热器加热至130℃左右遇脱炔反应器出来的氯化氢混合后,进入氧氯化反应器2。
氧氯化反应器内有附载于微球氧化铝上的氯化铜催化剂。气态乙烯、氯化氢与空气中的氧气在氯化铜催化剂的作用下,于190~240℃的反应温度及250~300h-1的空间速率下进行反应,生成二氯乙烷、水和其他少量的氯化烃类。反应所放出的热量由反应器冷却管内的水直接发生蒸汽而带出。

图6-14 流化床氧氯化反应器
1—入孔;2—喷嘴;3—管式分布器;4—乙烯和氯化氢进入管;5—板式分布器;6—喷嘴;7—空气进入管
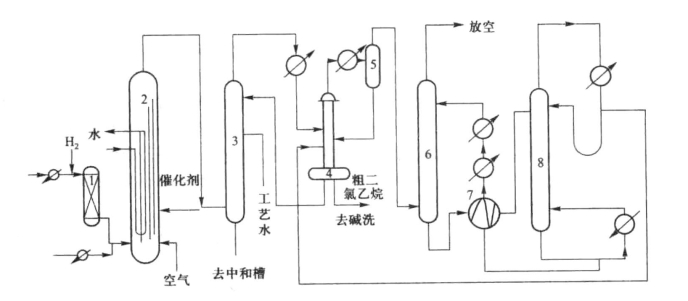
图6-15 乙烯气相氧氯化制二氯乙烷的工艺流程
1—脱炔反应器;2—氧氯化反应器;3—骤冷器;4—粗二氯乙烷分层器;5—气液分离器;6—二氯乙烷吸收塔;7—溶剂热交换器;8—二氯乙烷解吸塔
从氧氯化反应器出来的高温气体,从底部进入骤冷器3,经耐腐蚀的分布器均匀分布。水从塔顶自上而下与进塔的气体逆流接触,从气体中吸收氯化氢,分离掉夹带的催化剂粉末。塔底水溶液含酸为0.5%~1%(质量分数)去中和槽用碱液中和后,送往废水处理工序,以回收二氯乙烷。
从骤冷器顶部出来含二氯乙烷和水的气体,进入粗二氯乙烷冷凝器,大部分二氯乙烷被冷凝,液体收集在粗二氯乙烷分层器4中。从粗二氯乙烷分层器顶部出来的气体,在冷凝冷却器中降温,进入气液分离器5,冷凝的二氯乙烷经气液分离返回粗二氯乙烷分层器4,气体进入二氯乙烷吸收塔6。气体由塔底部进入,与塔上部加入的溶剂逆流相遇,二氯乙烷被溶剂(煤油)吸收,吸收塔顶出来的气体基本上不含二氯乙烷,从吸收塔顶部排入大气。从吸收塔底部出来含二氯乙烷的富溶剂,经过溶剂热交换器7加热,送入二氯乙烷解吸塔8。
二氯乙烷解吸塔在负压下操作,用再沸器加热。塔顶获得不含溶剂的二氯乙烷蒸汽,经二氯乙烷解吸塔冷凝器冷凝,凝液一部分作为回流送回解吸塔,一部分送至粗二氯乙烷分层器4。解吸塔底的贫溶剂含二氯乙烷低于0.01%,与二氯乙烷吸收塔底部出来的富溶剂间接换热而被初步冷却,再进一步降温后进吸收塔循环使用。
粗二氯乙烷分层器中的液体二氯乙烷,经碱洗、水洗后送入贮槽,在二氯乙烷精制系统精制分离后,可得精二氯乙烷。
技能链接
氯乙烯合成岗位的主要职责
氯乙烯合成操作是氯乙烯生产的主体作业。它包括两种气体的流量和转化温度的调节,并进行观察、检查、判断、记录,协调岗位之间、工种内外之间的工作等。它兼管乙炔、氯化氢两种气体的混合、冷却、除雾、预热、氯乙烯合成气的净化(除汞、水洗、碱洗)和压缩等进程。
氯乙烯合成岗位的主要技能要求
1.熟练掌握岗位的正常操作和开、停车,并使各项指标达到先进水平,具备岗位生产过程的分析、判断能力,以及对检修后的设备能进行试车、试生产操作等工艺操作能力。
2.具备正确判断岗位的异常情况并及时处理等应变和事故处理能力。
3.正确使用、维护岗位所用的机、泵、电器和仪表,有参加检修、验收和试车、开车等设备及仪表使用维护能力。
4.具备进行岗位主要设备的物料计算等工艺计算能力。
5.能看懂本装置的带控制点的工艺流程图、设备平面布置图,具备绘制本装置的工艺流程简图等识图制图能力。
空气为氧源的氧氯化法排出以氮气为主的大量尾气,增加了对环境的污染。为了减少物料损失,要用吸收、解吸的联合操作来回收尾气中夹带的二氯乙烷,为此所增加的投资和能耗必将提高产品成本。
相比之下,从日本三井东亚引进的氧氯化技术,以高浓度氧为氧源,不仅惰性气体少,乙烯浓度高,反应速率快,而且过剩的乙烯可循环使用,系统中积累的惰性气体部分放空,对同一生产规模来说,尾气排空量只有空气法的百分之一,减少了对环境的污染,同时对尾气做焚烧处理所耗用的辅助燃料量也减少了很多。但是纯氧法需要空分装置,制备纯氧也会增加成本,而且纯氧法不如空气法安全稳定,需要严格控制操作条件。所以氧氯化法采用空气法还是纯氧法要根据具体情况来确定。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




