乙醛液相氧化生产醋酸的过程是一个气液非均相反应,可分为两个基本过程:一是氧气扩散到乙醛的醋酸溶液界面,继而被溶液吸收的传质过程;二是在催化剂作用下,乙醛氧化为醋酸的化学反应过程。
1.反应机理和催化剂的选用
乙醛氧化生产醋酸的反应机理比较复杂,认识不完全统一。一般都认为自由基链反应机理较为成熟。自由基反应机理认为,乙醛氧化反应存在诱导期,在诱导期时,乙醛以很慢的速度吸收氧气,从而生成过氧醋酸。
![]()
过氧醋酸是一种不稳定的具有爆炸性的化合物,在363~383K下能发生爆炸。当过氧醋酸积累过多时,即使在低温下也能导致爆炸性分解。
作为乙醛氧化生产醋酸的催化剂,应能既加速过氧醋酸的生成,又能促使其迅速分解,使反应系统中过氧醋酸的浓度维持在最低限度。由于乙醛氧化生成醋酸的反应是在液相中进行的,因而催化剂应能充分溶解于氧化液中,才能施展其催化作用。研究发现,可变价金属(如锰、镍、钻、铜)的醋酸盐或它们的混合物均可作为乙醛氧化法生产醋酸的催化剂,其催化活性高低为Co>Ni>Mn>Fe。虽然钴的醋酸盐在乙醛氧化生成醋酸的反应中活性最高,即钴盐催化剂对过氧醋酸的生成有较强的加速作用,但它不能满足过氧醋酸迅速分解的条件,会造成过氧醋酸在反应系统中积累,故而不能适用。采用醋酸锰为催化剂,不仅能使乙醛氧化为过氧醋酸的反应加速进行,而且能保证过氧醋酸生成与分解速度基本相同,其醋酸收率也远远高于其他金属的催化剂。所以,工业上普遍采用醋酸锰作为催化剂,有时也可适量加入其他金属的醋酸盐。醋酸锰的用量约为原料乙醛量(质量分数)的0.1%~0.3%。
醋酸锰发挥催化作用的机理一般认为是经过下面的反应:
![]()
Mn3+存在溶液中,可引发原料乙醛产生自由基。
(1)链引发:
![]()
O2的存在能选择性地加速过氧醋酸自由基的产生:

经过上述链引发后,氧化反应速度加快,由于自由基的存在使分子链增长。
(2)链增长:
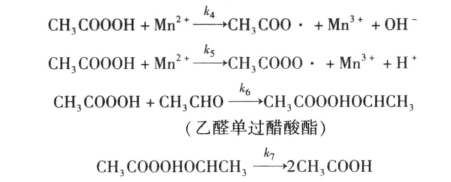
(3)链终止:
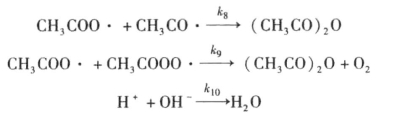
通常情况下,反应速率常数是k1、k2、k3、k8和k9小于k4、k5、k6、k7。因此,乙醛氧化生成醋酸的反应初期存在一引发阶段,即诱导期,这也是生产中必须有催化剂存在下才能顺利进行的原因之一。
采用催化剂不仅能加快链反应的引发,缩短诱导期,加速过氧醋酸的生成,更有利于加快过氧醋酸的分解,避免由于过氧醋酸的积累可能引起的爆炸,从而使乙醛氧化生产醋酸得以工业化。
2.氧化剂的选择
在氧化剂选择方面,原则上采用空气或氧气均可。当用空气时,大量氮气在气液接触面上形成很厚的气膜,阻止氧的有效扩散和吸收,从而降低设备的利用率。若用氧气氧化,应充分保证氧气和乙醛在液相中反应,以避免反应在气相中进行;且在塔顶应引入氮气以稀释尾气,使尾气组成不致达到爆炸范围。目前生产中采用氧气作氧化剂的较多。
3.气液传质(氧的吸收与扩散)的影响
影响氧的扩散与吸收的主要因素有以下三个方面。
(1)氧的通入速度(https://www.xing528.com)
通入氧气速率越快,气液接触面积越大,氧气的吸收率越高,设备的生产能力也就会增大。但是,通氧速率并非是可以无限增加的,因为氧气的吸收率与通入氧气的速率不是简单的线性关系。当通入氧气速率超过一定值后,氧气的吸收率反而会降低,氧气的损耗相应地加大,甚至还会把大量乙醛与醋酸液物料带出。此外,氧气的吸收不完全会引起尾气中氧的浓度增加,造成不安全因素。所以,氧气的通入速率受到经济性和安全性的制约,存在一适宜值。工业生产中氧气的通入速度可用氧化的空速来描述。
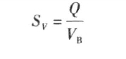
式中 SV——氧化的空速,h-1;
Q——氧气的流量,m3/h;
VB——反应器内液体的滞留量,m3。
(2)氧气分布板的孔径
为防止局部过热,生产中采取氧气分段通入氧化塔,各段氧气通入处还设置有氧气分布板,以使氧气均匀地分布成适当大小的气泡,加快氧的扩散与吸收。氧气分布板的孔径与氧的吸收率成反比,孔径小可增加气泡的数量和气液两相接触面积,但孔径过小则造成流体流动阻力增加,使氧气的输送压力增高。如果孔径过大,不仅会造成气液接触不良,而且会加剧液相物料的带出,破坏正常的操作。
(3)氧气通过的液柱高度
在一定的通氧速率条件下,氧的吸收率与其通过的液柱高度成正比。液柱高,气液两相接触时间长,吸收效果好,吸收率增加。与此同时,液柱越高,液体的静压大,氧气再液相内溶解的量也越多。氧气的吸收率与液柱高度之间的关系如表5-2所示。
表5-2 氧吸收率与液柱高度的关系
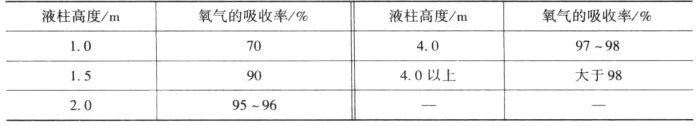
从表5-2中的数据可以看出,当液柱超过4m时,氧的吸收率可达97%~98%以上,液柱再增加,氧气的吸收率无明显变化。因此,在工业生产中,氧气进入反应器的进料口位置应设置在液面下4.0m或更深的位置处,否则氧气的吸收不充分。
4.乙醛氧化速率的影响
乙醛氧化生产醋酸的速率与催化剂的性质和用量、反应温度、反应压力、原料纯度、氧化液的组成等诸多因素有关。
(1)反应温度
温度在乙醛的氧化过程中是一个非常重要的因素,乙醛氧化成过氧醋酸及过氧醋酸分解的速率都随温度升高而加快,但温度不宜太高,过高的温度会使副反应加剧,导致如甲酸等低碳数有机氧化物大量生成,并且尾气中一氧化碳、二氧化碳含量显著增多,严重时甚至可能导致反应失控。但温度也不宜过低,温度过低会降低乙醛氧化为过氧醋酸以及过氧醋酸分解的速率,易导致过氧醋酸的积累,同样存在不安全性。因此,用氧气氧化时,适宜温度控制为343~353K,还必须及时连续地移走反应热,并且在系统内需通入氮气。
(2)反应压力
操作压力对乙醛氧化过程的影响从两个方面体现。
①乙醛氧化反应是一个气体体积减小的反应,增加压力有利于反应向生成醋酸的方向进行。由于乙醛氧化是气液相反应,提高反应压力,既可促进氧向液体界面扩散,又有利于氧被反应液吸收。
②反应物乙醛的正常沸点为21℃,增加压力可使乙醛沸点升高,从而减少乙醛的损失,但是,升高压力会增加设备投资费用和操作费用,实际生产中操作压力控制在0.15MPa(表压)左右。
(3)原料纯度
乙醛氧化生成醋酸反应的特点是以自由基为链载体,所以凡能夺取反应链中自由基的杂质,称为阻化剂。阻化剂的存在,会使反应速度显著下降。水是一种典型的能阻抑链反应进行的阻化剂,故要求原料乙醛含量(质量分数)>99.7%,其中水分含<0.003%。乙醛原料中三聚乙醛可使乙醛氧化反应的诱导期增长,并易被带入成品醋酸中,影响产品质量,故要求原料乙醛中三聚乙醛含量<0.01%。
(4)氧化液的组成
在一定条件下,乙醛液相氧化所得的反应液称为氧化液,其主要成分有乙醛、醋酸、醋酸锰、氧、过氧醋酸,此外还有原料带入的水分及副反应生成的醋酸甲酯、甲酸、二氧化碳等。
氧化液中醋酸浓度和乙醛浓度的改变对氧的吸收能力有较大影响。当氧化液中醋酸含量(质量分数)为82%~95%时,氧的吸收率保持在98%左右,超出此范围,氧的吸收率下降。当氧化液中乙醛含量在5%~15%时,氧的吸收率也可保持在98%左右,超出此范围,氧的吸收率下降。从产品的分离角度考虑,一般在流出的氧化液中,乙醛含量不应超过2%~5%。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




