2.2.1 溶剂提取法
溶剂提取法即选择适宜的溶剂将药材中的化学成分从原料中提取出来的方法,应选取对有效成分溶解度大、对杂质成分溶解度小的溶剂,将天然有效成分从药材组织内溶解出来。
1.提取溶剂的选择
溶剂提取法的关键是选择适当的溶剂。只有溶剂选择适当,才可能顺利地将需要的化学成分提取出来。常用的溶剂有水、有机溶剂、酸性/碱性有机溶剂等。依据“相似相溶”原理,根据待分离药材原料中化合物的极性选取适宜的亲水性或亲脂性溶剂进行提取,就会有较大的溶解度,这是选择提取溶剂的重要依据。如天然药物原料中富含萜类、甾体等脂环类及芳香类化合物等极性小化合物,应采用亲脂性有机溶剂如三氯甲烷、乙醚等进行提取;而糖苷、氨基酸等大极性类成分,应采用亲水性溶剂如水及含水醇等进行提取;至于生物碱、有机酸等碱性、酸性或两性化合物,由于存在状态(结合型或游离型)随溶液pH不同而异,故溶解度将随pH的变化而改变,宜采用酸性/碱性有机溶剂提取。一般可将药材原料根据提取的目标成分,按照提取溶剂的极性递增方式选用不同溶剂,如石油醚、汽油或者环己烷(可提出油脂、蜡、叶绿素、挥发油、游离甾体及萜类等小极性化合物)、苯、三氯甲烷或乙酸乙酯(可提出三萜苷元、游离生物碱、有机酸及黄酮、香豆素的苷元等中等极性化合物)、丙酮或乙醇、甲醇(可提出糖苷类、生物碱盐、木脂素以及类黄酮的多酚类等极性化合物)及水(可提出氨基酸、糖类、无机盐等水溶性成分)进行提取。此外,根据某些天然药物成分的酸碱化学性质,为了增加其溶解度,也可采用酸水及碱水作为提取溶剂。酸水提取可使生物碱等含氮的碱性化合物与酸水反应生成盐而溶出,同样碱水提取可使有机酸、黄酮、蒽醌、香豆素和内酯以及酚酸类成分成盐而溶出。常见溶剂的亲水性或亲脂性强弱见表2-2。
表2-2 常见溶剂的极性顺序
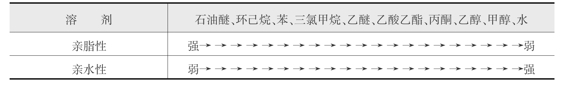
物质的极性用偶极矩μ来表示,溶剂的极性常以介电常数ε来表示,因为μ与ε之间呈正比例关系,可以用ε的大小表示溶剂极性的大小,ε大的溶剂极性强,ε小的溶剂极性弱。常见溶剂的性质见表2-3。在选择提取溶剂时,要充分比较有效成分的分子结构、理化性质和溶剂的分子结构、理化性质。如果有效成分结构中的功能基团以及极性与某一种溶剂分子的功能团、极性或介电常数有相似之处,这种溶剂就有可能作为该种有效成分的提取溶剂。例如含羟基化合物易溶于乙醇、甲醇中,含羰基化合物易溶于丙酮中。
表2-3 某些溶剂的物理性质及介电常数

续 表
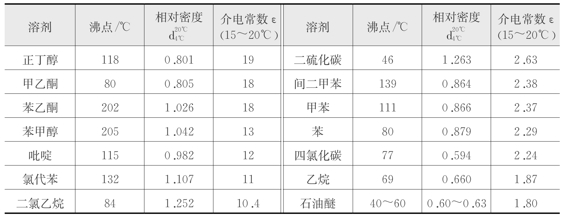
值得注意的是,从药材中提取有效成分时,多种成分之间相互影响,存在相互助溶作用,情况要复杂得多。例如,自古以来多采用水煎煮提取,除能提取水溶性成分,也能从中提取出很多水不溶性成分。因此,从药材中提取有效成分很难有一个固定的模式,需要根据提取要求、目标成分、杂质的性质差异以及溶剂的溶解能力来确定。工业化生产中选取提取溶剂应依据浸出速度快、目标成分纯度高、杂质少、成本低的原则进行。但是在实际生产中经常会遇到相互矛盾的情况,如浸出速度快,但是目标产物纯度低,或者目标产物纯度高,但浸提速度非常慢等状况,因此提取工艺中溶剂的选择需从全局考虑。有时选取某一浸提速度快的提取溶剂,仅从提取工序上考虑成本低、周期短,但是从整个生产工艺来看,提取后目标产物含量低,杂质较多,从而带来了繁琐的后续纯化工序,使整体提取工艺成本并不低、生产周期长。如果先期选择一种浸提速度慢,但是目标产物含量高的提取溶剂,尽管提取工序生产周期延长,成本相应增加,但是会大幅度简化后续的纯化工艺,结果降低了整个提取分离工艺的生产成本,生产周期与前者相比相对缩短。所以衡量或评价某一提取溶剂的优劣不能单纯从提取工序考虑,还要综合考虑和评价整个提取工艺流程。例如从铃兰(Convallaria keiskei)中提取铃兰毒苷,水和稀乙醇提取强心苷的速度较快,特别是以水作提取溶剂时生产成本最低,但提取物强心苷含量低,后续处理工序长,最终生产成本很高。如果使用9∶1或8∶2的苯-乙醇溶剂进行提取,单纯从提取这一工序来看成本较高,但是所得提取物强心苷纯度高、质量好,后续纯化工序少、工艺简单,反而最终降低了成本。所以我国采用苯-乙醇(9∶1)的混合溶剂提取强心苷。
近年随着环保意识的不断增强,保护环境的呼声不断提高,天然药物的提取工作在选取溶剂时还要考虑到是否会对环境带来污染,是否会排放废弃溶剂污染环境。同时利用有机溶剂进行天然药物有效成分的提取时还要考虑到最终提取物或者终端制剂产品中是否会有溶剂残留的问题。因此浸出溶剂的选择对有效成分的整个生产工艺有决定性的影响,但有时难以进行选择。需要把浸出溶剂的选择和生产工艺路线的选择交叉进行,往往需要将多个生产工艺路线进行比较,反复多次实验才能作出正确结论。
2.传统的溶剂提取法
传统的溶剂提取法主要有浸渍法、渗漉法、煎煮法、简单回流提取法及连续回流提取法等。其中浸渍法、渗漉法属于常温提取,提取温度较低,适用于热不稳定原料成分的提取,提取物中所含杂质较少。煎煮法、简单回流提取法及连续回流提取法均属于加热提取,提取温度相对较高,提取物中所含杂质较多。此外,连续回流提取具有操作简单、节省溶剂的优点。根据药材原料中有效成分的稳定性选择适宜的溶剂提取方法。在不了解原材料中所含成分是否稳定的情况下,一般应避免高温提取,以防有效成分发生变化。
(1)浸渍法:浸渍法属于静态提取方法,是将粉碎后药材原料在适宜的溶剂(如三氯甲烷、乙醇、稀醇或水)中浸渍,以溶出其中化学成分的方法。本法操作简便易行,但所需时间长,溶剂用量大,提取率较低。本法广泛用于酊剂、酒剂的生产。适于新鲜、易于膨胀的药材,尤其适用于热敏性药材物料的提取,不适用于贵重药材和毒性药材的提取。
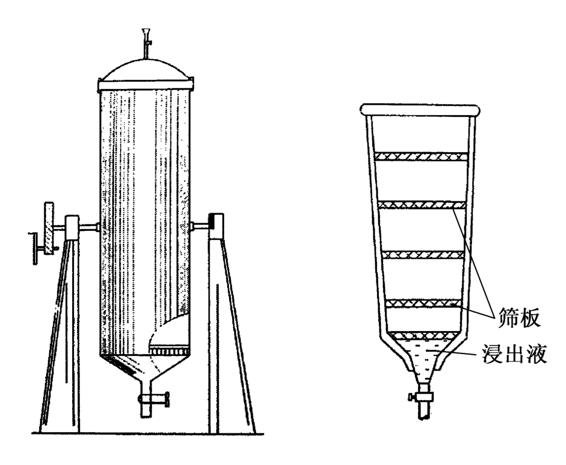
(2)渗漉法:渗漉法是将药材粉碎后装入渗漉罐中,新的溶剂不断自上而下渗透过药材,穿过药材细胞,使药材中的化学成分溶于渗漉液而流出的提取方法。渗漉法是目前国内外普遍采用的方法,提取效率比浸渍法高,且可用以提取较大量的药材原料样品。根据需要可以采用单一溶剂进行渗漉,也可使用几种溶剂依次进行渗漉。在渗漉过程中不断补充渗漉溶剂至药材的有效成分充分浸出,或当流出液颜色极浅或渗漉液的体积相当于药材质量的10倍时,可认为基本上已提取完全。在大生产中可将收集的稀渗漉液作为另一批新原料的溶剂使用。渗漉法适用于提取热敏性、易挥发或剧毒性的药材成分,也适用于提取有效成分含量较低或希望获得高浸出液浓度的药材原料。渗漉法的主要设备是渗漉筒或渗漉罐,一般为圆柱形和圆锥形,如图2-4所示。根据所渗漉药材的膨胀性选择渗漉装置的形状,一般都选择圆柱形,如果是膨胀性强的药材则多采用圆锥形。渗漉筒的材料有玻璃、搪瓷、陶瓷和不锈钢等。工业化生产时采用的渗漉装置流程如图2-5所示,可以长时间、大规模批量渗漉式生产,渗漉结束,通过蒸气加热浓缩使药渣中残留浸提溶剂得以回收,减少溶剂消耗,降低生产成本。
(https://www.xing528.com)
图2-4 小型渗漉设备
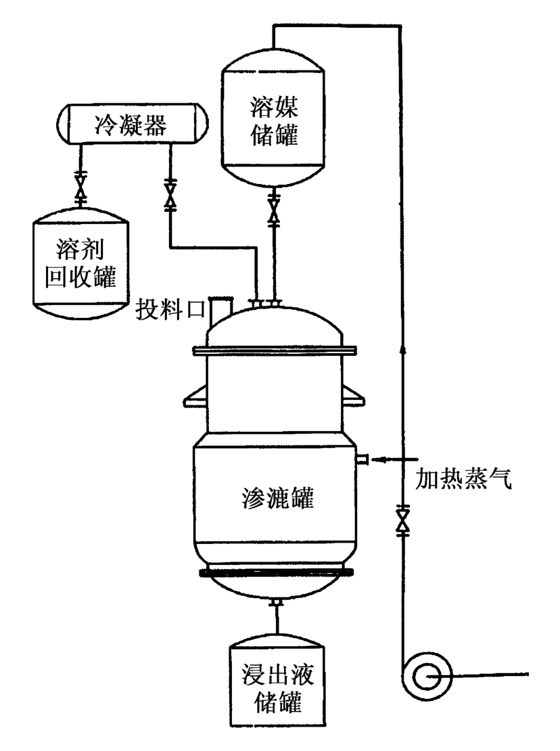
图2-5 大规模连续渗漉装置流程示意图
(3)煎煮法:煎煮法是我国最早使用的传统浸提方法,至今仍是药材提取最常用的方法。煎煮法就是将药材加水煎煮过滤取汁的方法。所用容器一般为陶器、砂罐或铜制器皿,不宜用铁制器皿,以免药液变色。用蒸气加热设备的药厂,多采用反应釜、大铜锅或水泥砌的池子中通入蒸气加热。还可将数个煎煮器通过管道互相连接,从而进行连续煎提。如图2-6所示为可倾式夹层煎煮锅。

图2-6 可倾式夹层煎煮锅
(4)简单回流提取法及连续回流提取法:简单回流提取法及连续回流提取法是选取适宜的有机溶剂通过加热回流的方式浸提原料中有效成分的方法。简单回流提取法及连续回流提取法具有操作简单、节省溶剂、提取效率高等特点。但是该方法是在较高温度下对药材成分进行提取,因此提取物中杂质也相对较多,且不适用于受热易破坏的有效成分提取。
简单回流提取在工业生产中常常使用的设备就是多功能提取罐,如图2-7所示。该提取罐根据提取溶剂的不同选择相应的加热方式。如果用水作为溶剂进行提取,当药材和水均加入罐中,立即向罐内通入蒸汽进行直接加热,当加热温度达到所需温度时,停止进汽加热,改向罐体夹层通蒸汽进行间接加热,以维持罐内温度稳定在规定范围内;如果用醇为提取溶剂时,则始终通过向罐内夹层通入蒸气进行间接加热。在提取过程中,罐内产生大量蒸气,经过泡沫捕集器收集进入冷凝器冷凝,冷却塔冷却,通过气液分离器分离,废气排出,液体回流到提取罐内,实现回流提取直到提取结束。回流提取同时可以用泵对药液进行强制性循环,以提高提取效率,但是对于淀粉含量高的药材不适用于强制循环方式提取。所谓强制循环,是指药液自罐体下部排液口流出,经过过滤器过滤,用泵输送回提取罐内,往往在罐的上部有口流入罐内。提取完毕后,提取液从罐的下方经过过滤器从排液口流出,再继续输送到相应的浓缩装置。
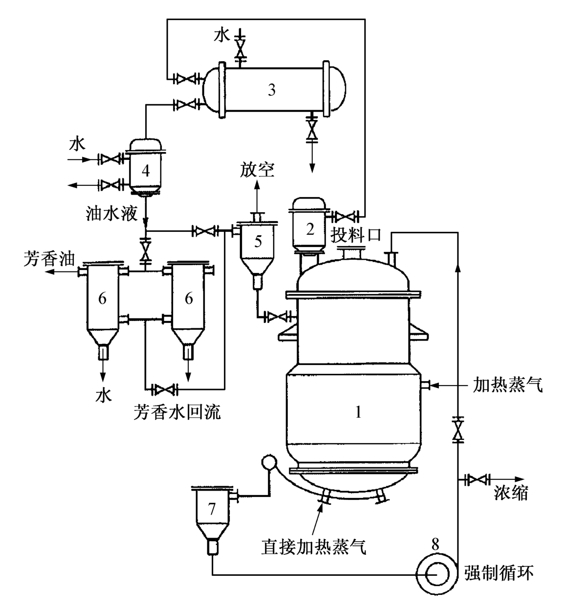
图2-7 多功能提取罐示意图
1.提取罐;2.泡沫捕集器;3.换热器;4.冷却器;5.气液分离器;6.油水分离器;7.过滤器;8.循环泵
3.影响提取的因素
药材原料提取成功与否,关键在选择合适的溶剂和提取方法。当确定了适宜的提取溶剂和提取方法后,在提取过程中,原料的粉碎度、提取温度、提取时间、设备条件等因素也会影响提取效率,必须加以考虑。
(1)粉碎度:药材原料粉碎成细颗粒,表面积增大,加快了浸出过程。但粉碎度过高,样品颗粒表面积过大,反而增强了吸附作用,影响过滤速度。另外,对于富含蛋白质、多糖类成分较多的样品如果粉碎过细,采用水为溶剂提取时,蛋白质、多糖的溶出过多,促使提取液黏度增大,甚至变为胶体,影响其他成分的溶出。原料的粉碎要考虑提取原料的部位和所选用的提取溶剂。用水作溶剂提取时,可采用粗粉(20目)或薄片,用有机溶剂提取时粉碎颗粒可略细点,以过60目为宜。根与茎类可切成薄片或粗粉,全草、叶类、花类、果实类以过20~40目为宜。
(2)提取温度:一般来说,冷浸杂质少,但效率低,热提杂质多,效率高。随着温度的升高,分子运动速度加快,促使渗透、溶解、扩散速度提高,所以提取效果较好。但加热温度也不宜过高,若温度过高某些化学成分易破坏,而且杂质含量也增多,为后续的分离精制带来困难,一般加热在60℃左右为宜,最高不超过100℃。
(3)浓度差:溶剂穿过细胞壁和细胞膜进入细胞内,溶解成分后,因细胞内外存在浓度差,就向外扩散,提取一段时间后,胞内外浓度一定时,达到扩散的动态平衡,成分不再浸出。此时通过更换溶剂,破坏平衡,就开始了新的扩散,反复多次才能实现提取完全。从这一角度分析回流提取法最好,浸渍法最差。
(4)提取时间:随着提取时间的延长,各种化学成分的提取率也相应增大,但是杂质成分的提取率也在增加,因此提取时间不宜过长。如果用水作为溶剂提取,一般以0.5~2小时为宜,最长不应超过3小时,如果用乙醇作为溶剂,提取时间以每次1~2小时为宜,其他有机溶剂可适当延长一点时间。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




