2.1.3 破坏细胞膜和细胞壁的方法
细胞破碎(cell rupture)技术是指利用外力破坏细胞膜和细胞壁,使细胞内物质包括目标成分释放出来的技术。
药材原料绝大部分来源于植物、动物和微生物,细胞是构成生物体最基本的结构单元,植物、微生物细胞外具有细胞壁,细胞壁主要由纤维素及多糖类物质组成,干燥植物体中纤维素占1/3~1/2,其中纤维素形成微细纤维,木素和半纤维素作为微细纤维和纤维细胞间的填充剂或黏合剂,进而形成细胞壁的框架。动物细胞无细胞壁,细胞膜把细胞包裹起来,使细胞能够保持相对的稳定性,维持正常的生命活动。细胞膜由磷脂、膜蛋白、多糖以及糖蛋白构成。细胞膜不单是细胞的物理屏障,也是在细胞生命活动中有复杂功能的重要结构。细胞所必需的养分的吸收和代谢产物的排出都要通过细胞膜。细胞膜具有选择渗透性,这是细胞膜最基本的一种功能。如果细胞丧失了这种功能,细胞就会死亡。而药材中多数生物活性物质存在于细胞壁或者细胞膜内,只有少量存在于细胞间隙。因此,细胞壁和细胞膜是药材有效成分提取的主要屏障,只有针对不同的药材确定适宜的破坏细胞膜和细胞壁的方法才能有效提高药材有效成分的提取率。常用的破壁方法有干燥法、冻融法、机械破碎法、化学破壁法、生物酶解法和压差法等。
1.干燥法
药材原料采收后要进行干燥,干燥也是原料提取前进行破壁的有效方法。药材原料在干燥过程中,细胞壁先失水,细胞液的浓度不断增高,胀压并逐渐萎蔫,终致细胞受到破坏而死亡。在这个干燥过程中由于细胞失水,失去胀压,但细胞质与细胞壁紧紧地黏附在一起进行收缩,虽不产生质壁分离,但形成大量褶皱。由于内外两个不同方向牵引力的作用,使细胞膜和细胞壁受到机械的伤害,改变了细胞膜的超滤性和渗透性,改变了材料的细胞组织,促使细胞内的物质易于被溶剂浸出。但干燥破壁的同时也要尽量避免原料中有效成分的损失,因此干燥的温度常因所含成分而异:一般含有糖苷类和含有生物碱的原料干燥温度为50~60℃,这样可以破坏植物体内酶的活性而避免有效成分的分解;维生素含量高的果实类原料应迅速干燥,如果不能干燥则应进行冷藏;富含挥发油的药材原料干燥温度不宜超过35℃,以免挥发油散失。
药材原料干燥的方法,通常有阳干法、阴干法和直接加热烘干法。阳干法是直接利用日光晒干,可将原料置于搭架的竹帘、竹席上,在日光下晒干,也可以铺于河滨沙砾地,其干燥时间可显著缩短,适用于肉质根类;但主要含有挥发油的药材或者有效成分日晒后易变色变质的药材如大黄、黄连,烈日下晒后易开裂的药材如郁金、白芍等均不宜采用阳干法干燥。阴干法是将药材置于通风良好不见直射阳光的地方,使水分自然散发。阴干法适用于芳香性花类、叶类、全草和某些根皮类原料。阴干法的特点是温度比较低,蛋白质和细胞质没有变性,细胞膜和细胞壁所受到的损害较少,而且这种方法对有效成分的损害较小。阴干法干燥时间长,对于肉质根类和果实类原料,水分含量高,散失慢则易于引起发霉变质。这种原料药材则可以采用直接加热干燥法。直接加热干燥是将新鲜原料切片后加热干燥,在干燥时水分急剧蒸发,细胞内原生质和蛋白质凝固、变性、细胞萎缩,使细胞膜和细胞壁破坏,改变细胞组织的渗透性;但是这种方法不适合用于对热不稳定的物质。
2.冻融法
冻融法就是将细胞冻结后再融化。冻结的作用是破坏细胞膜的疏水键,增加其亲水性和通透性,并因为细胞内的水在低温下结冰而易于刺破细胞壁,从而达到破壁的目的,如果再加其他外力的作用更会促进破壁率的增加,从而提高天然药物成分的溶出。
3.机械破碎法
采用这种方法,药材细胞受到高压产生的高剪切力,与玻璃球一起高速搅拌,破碎速度快、效果好,且处理药材量大。但对大多数热敏物质要采取冷却措施,以除去由于高速搅拌而产生的过多热量,避免生物活性物质的破坏。
(1)球磨法:研磨是一种常用的方法,使用设备是球磨机,如图2-1所示。该方法将细胞组织悬浮液与玻璃小珠、石英砂或氧化铝一起搅拌或研磨,珠子之间以及珠子和细胞之间互相剪切、碰撞,促使细胞壁破碎,释出内容物。在珠液分离器的协助下,珠子被滞留在破碎室内,浆液流出,从而实现连续操作。破碎中产生的热量由夹套中的冷却液带走。

图2-1 WSK卧式高效全能球磨机
破碎作用与球体的直径、进入球磨机的细胞浓度、料液的流速、搅拌器的转速以及温度等有关。这些参数不仅影响破碎程度,也影响所需能量。球体的大小应根据细胞大小和浓度以及在连续流动的操作过程中不使球体带出来选择,球体在磨室中的装量对破碎程度和所需能量有影响。增加搅拌速度能提高破碎效率,但过高的速度反而会使破碎率降低,能量消耗增大,所以搅拌速度应适当。操作温度在5~40℃范围内对破碎物影响较小,但在操作过程中,磨室的温度很容易升高,较小的设备可考虑采用冷水冷却来调节磨室温度,大型设备中热量的除去是必须考虑的一个重要问题。因此,球磨法存在的问题是操作参数多,破壁后球体之间残留的液体较多,原料损失较大。
(2)高压匀浆:高压匀浆是大规模破碎细胞的常用方法,高压匀浆机如图2-2所示。利用高压迫使细胞悬浮液通过针形阀(图2-3),细胞悬浮液自高压室针形阀喷出时,每秒速度高达几百米,高速喷出的浆液又射到静止的撞击环上,被迫改变方向从出口管流出。细胞在这一系列高速运动过程中经历了高速剪切、碰撞及压力骤降,造成细胞破碎。影响破碎的主要因素是压力、温度和通过匀浆阀的次数。升高压力有利于破碎,减少细胞的循环次数,甚至一次通过匀浆阀就可达到几乎完全的破碎,这样就可避免细胞碎片不至过小,但是也有实验表明压力增加超过一定值,破碎率增长反而很慢。工业生产中,通常采用的压强为55~70M Pa。在工业规模的细胞破碎中,对于酵母等难破碎的及浓度高或处于生长静止期的细胞,常采用多次循环的操作方法。

(https://www.xing528.com)
图2-2 高压匀浆机
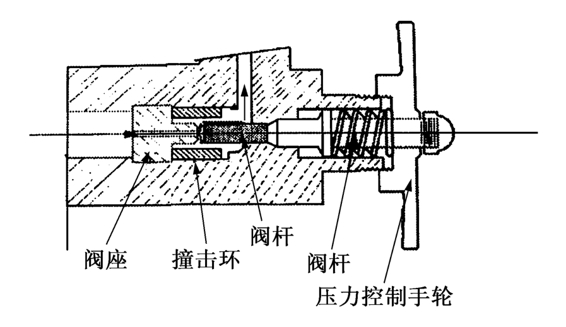
图2-3 APV Manton Gaulin高压匀浆器针形阀结构简图
(3)X-press法:另一种改进的高压方法是将浓缩的菌体悬浮液冷却至—30~—25℃形成冰晶体,利用500M Pa以上的高压冲击,冷冻细胞从高压阀小孔中挤出。细胞破碎是由于冰晶体在受压时发生相变,包埋在冰中的细胞变形引起的。此法称为X-press法或Hughes press法,主要用于实验室中,高浓度的细胞、低温、高的平均压力能促进破碎。该法的优点是适用的范围广、破碎率高、细胞碎片的粉碎程度低以及活性率高,但是对冷冻-融解敏感的天然活性物质不适用。
(4)超声波法:超声波破碎也是应用较多的一种破碎方法。超声波产生空化现象,空泡在液体中产生、长大、压缩、闭合、崩溃、快速重复的运动过程,产生瞬时高温和高压,并伴随强烈的冲击波和高速射流,使药材细胞振荡而发生高速碰撞。微射流和冲击波对边界层和固液界面的清洗、冲击、侵蚀和剥离作用,使边界层变薄,甚至使边界层产生空洞,破坏细胞壁结构,从而提高得率,缩短提取时间。另一方面,局部所产生的高温、高压,断裂了溶出组分分子与原有固体分子间的结合键,也加速了溶出进程,从而提高了液相体积效能。利用显微镜观察发现超声提取可使杜仲叶中细胞壁破裂,加速细胞中总黄酮类物质直接向溶剂中溶解,杜仲叶中总黄酮类物质的提出率可达25.43%。
(5)微波法:微波是频率介于300M Hz和300GHz之间的电磁波,微波作用于药用原料溶剂提取体系,基质材料吸收微波能量而升温。伴随升温的热应力作用,液态水气化产生的压力将细胞膜和细胞壁冲破,形成微小的孔洞,进一步加热,导致细胞内部和细胞壁的水分减少,细胞收缩,表面出现裂纹。孔洞或裂纹的存在使得胞外溶剂容易进入细胞内,溶解并释放出胞内产物。采用透射电镜观察,发现在微波强度为300W、预处理时间达到5分钟或微波功率为600W、预处理时间为2分钟时,细胞壁开始出现褶皱并有部分破裂,随着功率的加大以及微波预处理时间的延长,细胞壁破裂的情况越来越明显,从而使细胞内有效成分的提取分离变得容易。
(6)超微粉碎法:该粉碎方法是以破坏药材细胞壁为目的的粉碎过程。药材原料进行超微粉碎后,一方面细胞的破壁率高,使有效成分溶出阻力减小,另一方面物料粉碎后导致表面积和孔隙率增加。超微粉碎后的物料具有很强的表面吸附力、亲和力、分散性、溶解性,从而提高了有效成分的溶出速度及溶出率。实验证明,使用细胞超微粉碎技术能明显提高天然药物有效成分的提取率,特别对提取大分子成分,提取率提高效果更为显著。对黄芪药材进行纳米级粉碎后经显微特征观察,发现纳米黄芪悬浮液中固体颗粒平均粒径为81.7nm,大部分细胞壁被破碎,黄芪皂苷和多糖直接进入水中。
4.酶解法
酶解法是研究较广泛的一种破壁方法,它利用细胞破壁酶的反应分解破坏细胞壁上特殊的键,打破细胞结构,使内容物从细胞壁释放出来,从而达到提取有效成分的目的。常用的酶有纤维素酶、半纤维素酶、蛋白酶、果胶酶、溶菌酶、蜗牛酶、几丁质酶、复合酶等。酶解的优点是专一性强,发生酶解的条件温和。溶菌酶是应用最多的酶,它能专一地分解细胞壁上糖蛋白分子的β-1,4-糖苷键,使脂多糖解离,经溶菌酶处理后的细胞移至低渗溶液中使细胞破裂。酶法破壁设备简单易行,破壁率高,但时间长,速度慢,不宜长时间保存和长途运输。
自溶作用是酶解的另一种方法,利用生物体自身产生的酶来溶胞,而不需外加其他的酶。此法在微生物原料破壁过程中应用较多。在微生物代谢过程中,大多数都能产生一种能水解细胞壁上聚合物结构的酶,以促进其生长过程。微生物的自溶作用就是改变其生长环境(温度、pH值、缓冲液浓度、细胞代谢途径等),可以诱发产生过剩的水解酶或激发产生其他的自溶酶,以达到自溶目的。酵母菌需在45~50℃下保持12~24小时可以自溶。自溶法在一定程度上能用于工业生产,但是对热不稳定的微生物容易引起蛋白质变性,自溶后细胞培养液黏度增大,降低过滤速度。
5.压差法
压差法也称渗透压冲击法,该方法是较温和的一种破碎方法,将细胞置于高渗透压的介质(如一定浓度的甘油或蔗糖溶液)中,达到平衡后突然迅速减压引起压差变化,如突然稀释介质,或者将细胞转入水或缓冲液中,由于渗透压的突然变化,水迅速进入细胞内引起细胞壁的破裂。
6.化学破壁法
化学破壁法是利用某些化学试剂,如有机溶剂、变性剂、表面活性剂、抗生素、金属螯合剂等,可以改变细胞壁或膜的通透性(渗透性),从而使胞内物质有选择地渗透出来。例如酸碱处理,酸处理可以使蛋白质水解成氨基酸,通常采用6mol/L HCl溶液进行。碱能溶解细胞壁上脂类物质或使某些组分从细胞内渗漏出来。对于胞内的异淀粉酶,可加入0.1%十二烷基磺酸钠或0.4% Triton X-100于酶液中作为表面活性剂,30℃振荡30小时,异淀粉酶就能较完全地被提取出来,所得有效成分较机械破碎得率高。也可以利用有机溶剂如丁醇、丙酮、三氯甲烷及尿素等进行化学处理。但是,这些试剂常引起生化物质破坏,还会带来溶剂分离回收的后续问题。
选择合适的破碎方法需要考虑下列因素:①需要破壁的原料的数量,所需要提取的产物对破碎条件(如温度、试剂和酶等)的敏感性以及要达到破碎程度所需的速度等;②在能够达到预期破碎程度的同时尽可能采用最温和的方法;③同时对于具有大规模应用潜力的天然药物原料还应选择适合于工业化生产的破碎技术。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




