量子思维,认识酶的关键
|量子隧穿|
量子隧穿
quantum tunneling
因为粒子的波粒二象性,它们能够像波绕过墙壁一样穿过能量壁垒,这个量子过程被称为量子隧穿。
你或许还记得引言中提到的量子隧穿,这种特殊的量子过程可以让粒子像声音穿过墙壁一样通过不可穿透的壁垒。德国物理学家弗里德里希·洪特(Friedrich Hund)于1926年第一个发现了该现象,乔治·伽莫夫(George Gamow)、罗纳德·格尼(Ronald Gurney)和爱德华·康登(Edward Condon)紧随其后,用量子力学这种新的数学方法成功地解释了放射性衰变。量子隧穿后来成为核物理学最重要的特征,其在材料科学和化学中更为广泛的应用也使这种现象备受推崇。如我们所见,对地球上的生命来说,量子隧穿效应可谓生死攸关,因为在太阳内部氢核聚变生成氦的反应中,它让一对对带正电的氢原子核得以融合,从而使太阳释放出巨大的能量。然而,直到最近,人们还认为量子隧穿效应并不存在于任何生命过程中。
我们可以这样来思考量子隧穿——它能以一种与常识相左的方式,让粒子从壁垒的一端穿越到另一端。此处的“壁垒”指在物理上没有足够的能量就无法穿越的空间区域,与科幻小说故事中的“力场”类似。这个区域可以是隔绝导体两端的一层绝缘材料,也可以就是一段空间,就像呼吸反应链中两个酶之间的间隙。这个区域还可以是我们之前描述过的那种限制化学反应速率的能量壁垒(如图2-1中的例子)。
假设现在要把一个小球推上或踢上一个小山丘。要想让小球能登上山顶并从山的另一面滑下,就必须结结实实地猛踢一脚。小球沿着山坡向上滚,速度不断减慢,如果没有足够的能量(力量足够大一脚),它就会停下来,然后原路滚回。按照牛顿经典力学,让小球翻越山丘的唯一出路,便是使其获得足够的能量,升高到超过能量壁垒的位置。但是,如果小球是一个电子,山丘是由电磁斥力形成的能量壁垒,那么就存在很小的可能性使电子以波的形式穿越这个壁垒,也就是说,电子可以另辟蹊径,以更高效的方式完成穿越。这就是量子隧穿(见图2-5)。
图2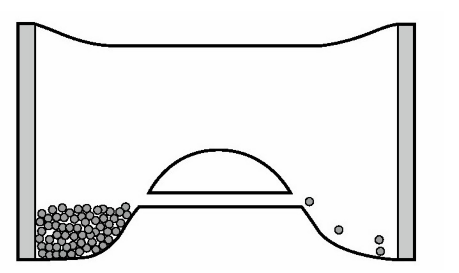 -5 量子隧穿
-5 量子隧穿
粒子越轻,隧穿便越容易,这是量子力学的特性之一。因此,当人们认识到量子隧穿是亚原子世界中的普遍现象后,由于电子是非常轻的基本粒子,电子的隧穿效应最为常见也就不足为奇了。20世纪20年代晚期,从金属放出电子的场致发射便被认为是一种量子隧穿。量子隧穿也可以用来解释放射性衰变——比如,铀等元素的原子核不时地放射出一个粒子。这是第一次成功地用量子力学求解出核物理问题。时至今日,化学领域对电子、质子(氢核)以及更重的原子的隧穿已经有了更深入的理解。
像许多其他的量子现象一样,量子隧穿依赖物质粒子向外传播时的“波”属性。这是量子隧穿的一个重要特点。要想使一个由无数粒子构成的物体完成隧穿,所有粒子的“波”属性必须在“行军”时保持步调一致,波峰波谷要重叠,我们将其称为系统“相干”,简而言之,就是调子要“合拍”。“退相干”的过程与之恰恰相反,所有的量子波各行其是,冲走了整体的相干行为,并最终使整体失去了量子隧穿的能力。一个粒子要以量子隧穿渗透壁垒,就必须保持其“波”的性质。这解释了为什么足球之类的宏观物体无法量子隧穿:这些物体由数以兆计的原子组成,所以粒子无法以协调一致的波形整体行动。
以量子的标准来衡量,活细胞也属于宏观物体。所以乍看上去,由于在活细胞中温热、湿润的环境内,原子和分子的绝大多数在无序运动,量子隧穿效应几乎不可能发生。但是,正如我们所发现的那样,酶的内部却别有洞天:酶的粒子并非群魔乱舞,而是跳着精心编排的舞蹈。这舞蹈到底如何影响生命,我们来一探究竟。
|电子隧穿|
在德沃尔特和钱百敦1966年做的实验中,低温下的实验数据与预期假设不符,直到多年以后实验结果才得到充分的解释。约翰·霍普菲尔德(John Hopfield)是另一位跨界甚广的美国科学家,其研究领域涉及分子生物学、物理学及计算机科学。他因为用计算机技术模拟神经网络而为人们所熟知,而且他对生物学中的物理过程也一直很感兴趣。
1974年,霍普菲尔德发表了题为《生物分子间的电子转移与热能激活的隧穿效应》(Electron Transfer Between Biological Molecules by Thermally Activated Tunneling)的论文,在文中,他建立了一套理论模型来解释德沃尔特和钱百敦的实验结果。霍普菲尔德指出,高温下分子振动的能量即使不用隧穿也足以使其翻越能量壁垒。随着温度降低,分子振动的能量便不再能够支持酶促反应发生。但是,德沃尔特和钱百敦在实验中发现,低温下,反应照样进行。霍普菲尔德认为,较低温度下的电子相当于处在了能量壁垒的半山腰,虽然仍不足以翻越能量壁垒,但相比于山脚下的位置,此处缩短了距壁垒另一端的横向距离,提高了通过量子隧穿跨越壁垒的可能性。他的解释是正确的:正如德沃尔特和钱百敦发现的那样,以隧穿为媒介的电子转移即使在非常低的温度下也能发生。
到了今天,很少有科学家还会怀疑电子在呼吸反应链中穿梭的方式是量子隧穿了。这就将动物及非光合作用微生物细胞中最重要的产能反应纳入量子生物学的研究范围(在下一章中我们将讨论依靠光合作用产能的生物)。但注意,即使以量子世界的标准来衡量,电子也非常轻,其行为模式在很大程度上不可避免要像“波”一样。因此,虽然许多标准的生物化学教科书,依然在沿用原子的“太阳系模型”,但我们不应该单纯地把电子看作可以运动弹跳的袖珍经典粒子。正如我们在引言中讨论过的“概率云”,电子之于原子,更像是一朵飘逸的“电子云”,像波一样变幻起伏又时刻笼罩着微小的原子核。如此一来,电子可以在生物系统中像声音穿过墙壁一样透过能量壁垒也就不足为奇了。(https://www.xing528.com)
但是,像质子或是整个原子那么大的粒子又是什么情况呢?它们也可以在生物系统中量子隧穿吗?乍看一眼,你可能觉得这是天方夜谭。即使是单个质子,其质量也是电子的2 000倍,而量子隧穿对于隧穿粒子的质量极度敏感:小的粒子容易隧穿,而重粒子隧穿时的阻力就要大很多,除非隧穿的距离非常短。不过,最近几个非常精彩的实验表明,即使是质量相对较大的粒子在酶促反应中照样可以量子隧穿。
|移动质子|
你或许还记得,除了促进电子转移,胶原蛋白酶的关键活动还包括移动质子以促使胶原蛋白断裂(见图2-4)。之前已经提过,这类反应是酶操纵粒子最常见的手段。大约有1/3的酶促反应都包含了将“氢原子”从一处移到另一处的环节。注意,此处的“氢原子”可以指代几种不同的东西:它可以是电中性的氢原子(H),由一个电子围绕一个质子构成;也可以是带正电的氢离子(H+),只有一个裸露的原子核而没有电子;或者还可以是带负电的氢负离子(H-),原子中有一个多余的电子。
任何谨慎的化学家或是生化学家都会不假思索地告诉你,分子内部或之间的氢原子(质子)转移并没有什么量子效应,或者说,至少不需要我们煞费苦心地用量子世界中像量子隧穿一样奇怪的过程来解释。确实,在生命可以活动的温度下,在绝大多数化学反应中,质子主要依靠非量子的热动力从一个分子跃迁到另一个分子。但是,质子隧穿也会出现在一些对温度变化相对不敏感的化学反应中,就像德沃尔特和钱百敦实验中的电子隧穿一样。
以量子世界的标准来衡量,允许生命活动的温度其实很高。因此,在生物化学史上,科学家们一直以为质子的酶促转移全靠以热能跨越能量壁垒的(非量子)机理。[27] 1989年,加州大学伯克利分校的朱迪思·克林曼(Judith Klinman)和她的同事们首先发现了酶促反应中存在质子隧穿的直接证据。克林曼是一位生化学家,一直认为质子隧穿在生命的分子机制中扮演了重要角色。实际上,她甚至宣称质子隧穿是整个生物学中最重要也最普遍的机理。她的突破来自对酵母菌中乙醇脱氢酶(ADH)的研究,这种特殊的酶可以将乙醇分子中的一个质子转移到一个叫作NAD+的小分子上,形成NADH。克林曼的小组巧妙地利用一种被称为“动态同位素效应”(kinetic isotope effect)的技术证实了质子隧穿的存在。该技术不仅在化学界很著名,而且为量子生物学提供了一部分最主要的证据。本书中还会多次提及此概念,因此值得我们好好解释一番。
|动态同位素效应|
你是否有过这样的经历:当你骑自行车爬陡坡时,反而被步行的人超过了?在平地上,你可以骑车毫不费力地超过走路的人,甚至跑步的人,那为什么在山坡上骑车就变得如此低效呢?
假设你不再骑车,而是从踏板上下来,推着自行车上坡或是在平路上走。现在,问题便很明显了。在山坡上,你必须把自行车和你自己同时推上斜坡。车身的重量,虽然对平路上的水平运动没什么影响,此时却在阻碍你爬上坡顶:你必须克服地球的引力,将车身抬高几米。正因为如此,赛车制造商一直在极力将他们的车造得更轻。很显然,物体的轻重对移动物体的难易程度有很大影响。不过,这个自行车的例子是想告诉大家,影响到底有多大,还取决于我们想怎样移动物体。
现在,假设有甲、乙两个小镇,你想知道两个小镇之间的地形是平坦还是崎岖,但又不能亲自去走一遭。不过,一个可能的办法很快浮出水面。你发现,甲、乙两镇之间有邮政服务,而往返于两地的邮递员们骑的是轻、重两个不同型号的自行车。为了知道两镇之间的地形到底是平坦还是崎岖,你可以在两镇之间寄出一些完全相同的包裹,一半由骑着轻车的邮递员来送,一半由骑着重车的邮递员来送。如果你发现两个包裹同时送达,那么两镇之间的路很可能是平坦的,但是如果骑重车的邮递员花了更长的时间才将包裹送到,那甲、乙两镇之间的路则可能是崎岖不平的。此例中,骑自行车的邮递员就扮演了地形探测器的角色。
像自行车一样,不同化学元素的原子质量也不同。因为氢原子的结构最简单,而且此处我们又对它最感兴趣,所以,让我们以氢原子为例来说明。一种元素是由其原子核中质子的数量来决定的(核外电子数与核内质子数相等,因而也由绕核运动的电子数决定)。因此,氢原子核中有一个质子,氦有两个,锂有三个,以此类推。但是,原子核内还有另一类粒子——中子。引言讨论太阳内部的氢核聚变时,我们曾提到过这种粒子。在原子核中加入中子使原子变得更重,因而改变了原子的物理性质。质子数相同而中子数不同的同一元素的不同核素互为同位素。最常见的氢的同位素是最轻的一种,由一个质子和一个电子构成,称为氕(H)。氕是氢元素最广泛的存在形式。但是,氢元素还有其他两种更重也更稀有的同位素:氘(D)和氚(T)。氘核中有一个质子、一个中子,氚核中有一个质子、两个中子。
元素的化学性质主要由其核外电子数决定。同一元素的不同核素,虽然具有相同的核电荷数,但核内中子数不同,因而具有极其相似但不尽相同的化学性质。动态同位素效应测量的是某种元素轻重不同的同位素在某化学反应中不同的敏感度,其定义为较重同位素的反应率与较轻同位素的反应率的比值。比如,如果某反应中有水(H2O)参与,那么水中的氢原子就可以被它的同位素氘或氚替代,形成重水(D2O)或超重水(T2O),然后通过比较水、重水、超重水在反应中的活跃程度,就可以知道氢元素的动态同位素效应。就像骑车的邮递员一样,该反应对反应中原子质量的变化敏感或不敏感,取决于反应物转化为反应产物的反应路径。
动态同位素效应的背后有几项重要的机理,其中之一便是量子隧穿。像骑车的例子一样,量子隧穿对隧穿粒子的质量极度敏感。增加质量让粒子的行为更像粒子而更不像“波”,同时更难穿透能量壁垒。因此,如果原子的质量加倍,比如将普通的氢原子换成氘,将使其量子隧穿的概率直线下降。
因此,如果发现某反应有显著的动态同位素效应,说明量子隧穿可能参与了反应,即反应物到反应产物的转化过程。当然,就此下结论还为时尚早,因为该效应也可能归因于一些经典(非量子驱动)的化学机理。不过,如果量子隧穿确实参与了化学反应,那么反应对温度应该有特殊的反馈:在低温下,即使温度继续下降,反应速率也会维持在一个平台期,就像德沃尔特和钱百敦实验中的电子隧穿一样。这恰是克林曼和她的小组在研究乙醇脱氢酶时的发现。克林曼小组的实验结果为反应机理中存在量子隧穿提供了强有力的证据。
克林曼小组继续跟进研究,并积累了重要的证据:在允许生命活动的温度下,质子隧穿普遍存在于许多酶促反应中。其他研究小组,比如曼彻斯特大学的奈杰尔·斯克鲁顿(Nigel Scrutton)小组,也针对其他酶做了类似的实验,实验中的动态同位素效应同样直指量子隧穿。然而,酶究竟是如何保持量子相干性来保证隧穿发生的呢?这一直是个很有争议的话题。一直以来,学界认为反应中的酶并非静态,而是在持续振动。比如,胶原蛋白酶的“大颚”每分解一个胶原蛋白的肽键就会开合一次。通常认为,酶的运动要么是反应机制中顺带引起的,要么是为了捕捉底物,将待反应的原子进行了正确的匹配。然而,量子生物学者们如今发现,这些振动其实是所谓的反应“驱动力”,主要功能是将原子和分子拉到足够近的距离,使它们的粒子(电子和质子)能够进行量子隧穿。这是量子生物学界最令人激动也是发展最快的研究课题。本书结语部分会重回这一话题。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




